Clear Sky Science · sv
Pan‑cancer klassificering av frysta snitt med en mjuk mixture‑of‑experts vision transformer under svag övervakning
Varför detta spelar roll i operationssalen
När kirurger avlägsnar en misstänkt tumör har de ofta bara några minuter på sig för att ta reda på om all cancer tagits bort. Patologer rusar för att undersöka ett snabbt fryst vävnadssnitt och ge ett svar medan patienten fortfarande ligger på bordet. Denna högtryckssituation kan försvåras av suddiga preparat, svårupptäckta tumörer och enkla tidsbegränsningar. Studien som beskrivs här undersöker hur ett artificiellt intelligens (AI)-system kan hjälpa patologer att snabbt och pålitligt skilja ofarlig från farlig vävnad över många olika organ, med utrustning som är realistisk för vanliga sjukhus.
Testet är snabbt men fullt av utmaningar
Analys av frysta snitt är en stapelvara i modern kirurgi: en tunn bit vävnad fryses, skivas, färgas och betraktas i mikroskop för att bedöma om den är benign eller malign och om kirurgiska marginaler är fria från tumör. Till skillnad från permanenta laboratoriepreparat lider frysta snitt ofta av sprickor, veck och ojämn färgning. Olika patologer kan göra olika bedömningar i gränsfall, och klockan tickar alltid. Dessa problem är särskilt allvarliga i mindre eller trånga sjukhus, där bara ett fåtal specialister måste täcka många typer av cancer. Författarna menar att en robust datorstödd assistent skulle kunna göra besluten kring frysta snitt mer konsekventa, snabbare och mer tillgängliga.
Bygga en bred, verklighetsnära bilduppsättning
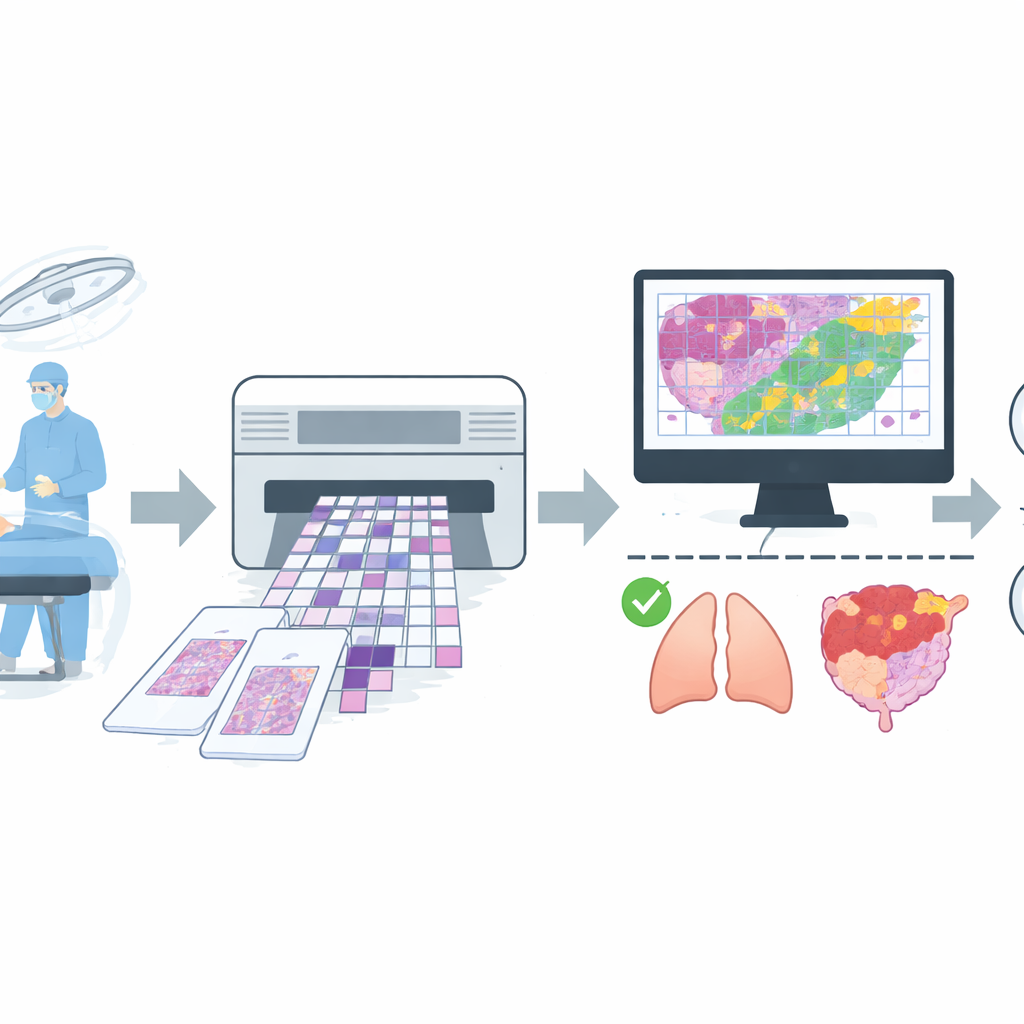
För att träna en sådan assistent samlade teamet en stor samling digitala bilder från rutinoperationer på ett större sjukhus. De satte ihop 4 754 helbilds‑slajder (whole‑slide images) av fryst vävnad från mer än 2 600 patienter och tillämpade strikta kvalitetsregler för att ta bort preparat med svåra artefakter eller osäkra diagnoser. Den slutliga datasetet innehöll 4 667 slajder, vardera enkelt märkta som benign eller malign baserat på överenskommelse mellan den snabba frysta läsningen och den senare, mer noggranna permanenta sektionens rapport. Slajderna täckte vanliga lokalisationer såsom lungor, bröst, sköldkörtel, lymfkörtlar och kvinnliga reproduktionsorgan, plus en blandad grupp av mindre frekventa platser som magsäck, lever och hud. Data delades upp i separata grupper för träning, finjustering och slutlig testning, med omsorg så att bilder från samma patient aldrig förekom i mer än en grupp.
Hur AI lär sig från svaga ledtrådar
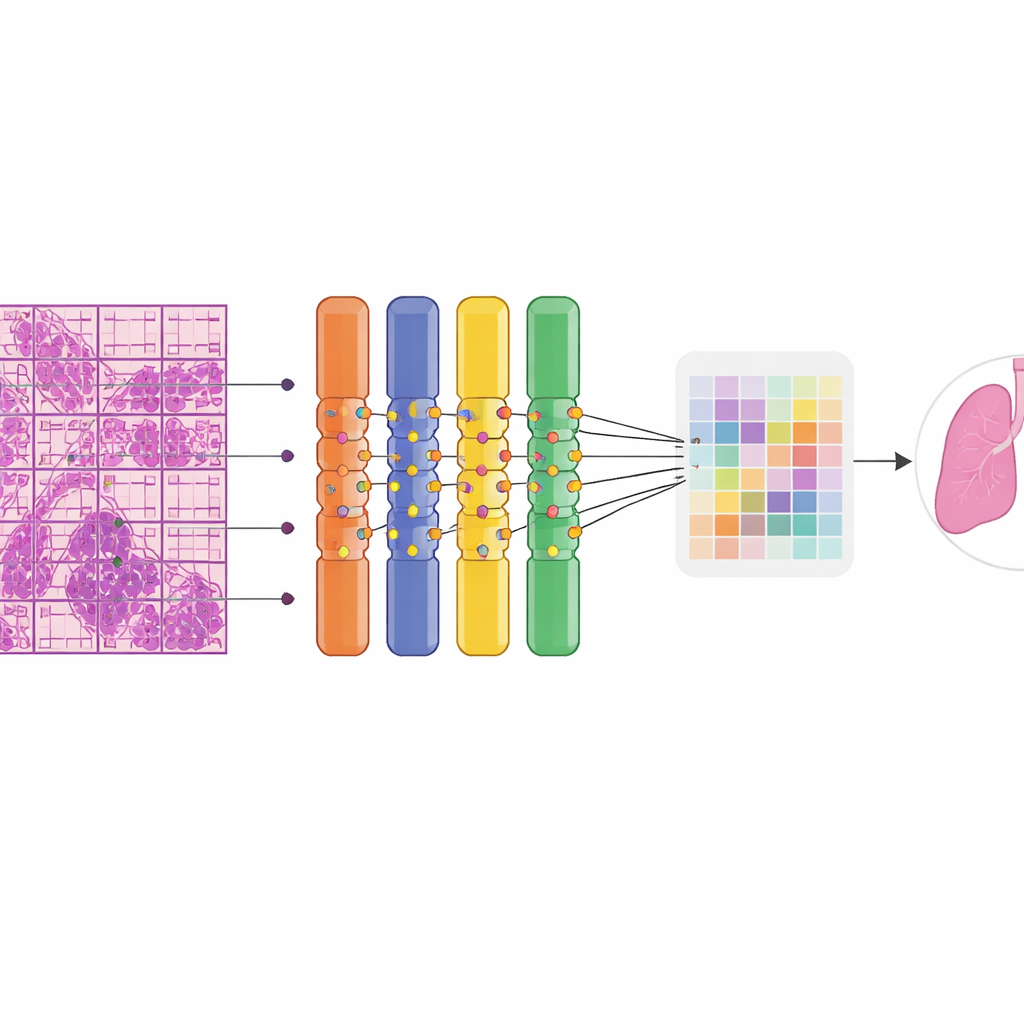
Forskarna byggde sin modell på en klass av neurala nätverk kallad Vision Transformer, som är utmärkt på att hitta mönster i stora bilder. Varje jättelikt vävnadsbild delades automatiskt upp i många mindre tiles och patchar så att den kunde bearbetas på standardgrafikhårdvara. En viktig innovation var att ersätta en del av nätverket med en "soft mixture of experts", en uppsättning många små specialiserade grenar som var och en fokuserar på olika visuella mönster. Istället för att slå av och på experter blandar systemet deras bidrag mjukt, vilket stabiliserar träningen och gör bättre användning av begränsade data. Eftersom patologerna inte ritade ut tumörgränser var modellen tvungen att lära sig från svag övervakning: den visste endast om en hel slajd var benign eller malign. En multiple‑instance learning‑strategi främjade de mest misstänkta patcharna inom en malign slajd för att fungera som positiva exempel, vilket gjorde det möjligt för nätverket att gradvis fokusera in sig på de mest informativa regionerna.
Hur väl systemet fungerar i praktiken
När det testades på 669 tidigare osedda slajder skilde AI:n benign från malign vävnad med hög noggrannhet. Det klassificerade korrekt omkring 90 % av fallen totalt och visade en utmärkt förmåga att separera de två grupperna över sannolikhetströsklar. Sensitivitet, sannolikheten att flagga en verkligt malign slajd, var omkring fyra av fem, medan specificitet, sannolikheten att tryggt kalla en benign slajd benign, var ännu högre. Viktigt är att prestandan förblev stark över olika organ: det upptäckte felfritt alla maligna lung‑ och bröstfall i testserien och presterade väl även på ovanligare grupper som kvinnliga adnexala tumörer och blandade "övriga" organ. Färgade värmekartor överlagrade på slajderna visade att modellens uppmärksamhet koncentrerades till regioner som expertpatologer kände igen som tumör, inklusive metastatiska fokier i lymfkörtlar, medan normala strukturer i hög grad ignorerades. Systemet kördes effektivt och behövde mindre än 5 GB minne, vilket gör det lämpligt för användning på vanligt förekommande grafikkort snarare än dyra kluster.
Begränsningar, felsteg och utrymme för förbättring
Författarna undersökte också var AI:n snubblade. Falskt negativa resultat involverade ofta mycket sparsamma cancerceller, suddiga skanningsområden eller kraftig inflammation som dolde maligna cellkluster. Falskt positiva tenderade att uppstå vid benigna tillstånd som imiterar cancer i mikroskopet, såsom reaktiva överväxter eller distorterade frysta preparat. Eftersom rutinmässiga kirurgiska arbetsflöden inte inkluderar detaljerade konturer av tumörområden kunde teamet inte kvantifiera exakt hur väl värmekartorna matchade expertmarkeringar, utan förlitade sig istället på kvalitativ granskning. Vissa organstyper, som tunga (tongue) eller vissa mjukdelstumörer, var fortfarande underrepresenterade, vilket antyder att större, multicentriska samlingar kommer att behövas för att utöka systemets räckvidd.
Vad detta kan betyda för patienter och sjukhus
Sammanfattningsvis visar studien att ett omsorgsfullt utformat AI‑system kan noggrant och tolkbart assistera i en central uppgift för kirurgisk patologi: att i realtid avgöra om vävnad är benign eller malign över många organsystem. Genom att arbeta endast med slajd‑nivåetiketter, köras på allmänt tillgänglig hårdvara och markera misstänkta områden för mänsklig granskning erbjuder modellen en praktisk väg mot mer konsekventa beslut vid frysta snitt. För patienter kan detta innebära bättre underbyggda beslut i samma operation; för sjukhus, särskilt de med begränsad specialistbemanning, pekar det mot en framtid där avancerade digitala verktyg hjälper till att leverera högkvalitativ cancervård mer jämlikt.
Citering: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Nyckelord: fryst snitt, digital patologi, cancerdiagnos, vision transformer, svagt övervakad inlärning