Clear Sky Science · sv
Implementering av ett likvidbiopsitest med 1021 gener för realvärldsprofilering av tumörgenom i onkologisk praxis
Varför ett blodprov för cancer spelar roll
De flesta vet att läkare ofta behöver ta bort en bit av en tumör för att förstå en patients cancer. Men denna traditionella biopsi är invasiv, kan vara smärtsam och fångar kanske inte hela bilden av en sjukdom som redan spridit sig. Denna studie undersöker en annan metod: att använda ett enkelt blodprov för att skanna efter genetiska förändringar i mer än tusen cancerrelaterade gener. Genom att visa hur väl detta stora blodtest fungerar i vardagliga onkologkliniker belyser forskarna en framtid där behandlingsval, övervakning och till och med ärftlig risk kan styras av ett rör med blod snarare än en skalpell.
Från nål i tumören till nål i venen
Cancer släpper ut små fragment av sitt DNA i blodomloppet när tumörceller dör och bryts ner. Dessa fragment, kallade cirkulerande tumör‑DNA, blandas med normalt DNA från friska celler. Teamet studerade 1 110 personer med metastaserad (avancerad) cancer av många typer, inklusive lung-, bröst-, kolorektal-, pankreas-, prostata-, äggstocks- och andra cancerformer. De använde ett omfattande test som läser 1 021 gener från ett blodprov och jämförde, när material från tumörvävnad fanns tillgängligt, dessa blodresultat med DNA från patientens tumörvävnad. De sekvenserade också vita blodkroppar tagna från samma blodprov för att skilja verkliga tumörsignaler från åldersrelaterade förändringar i blodbildande celler. 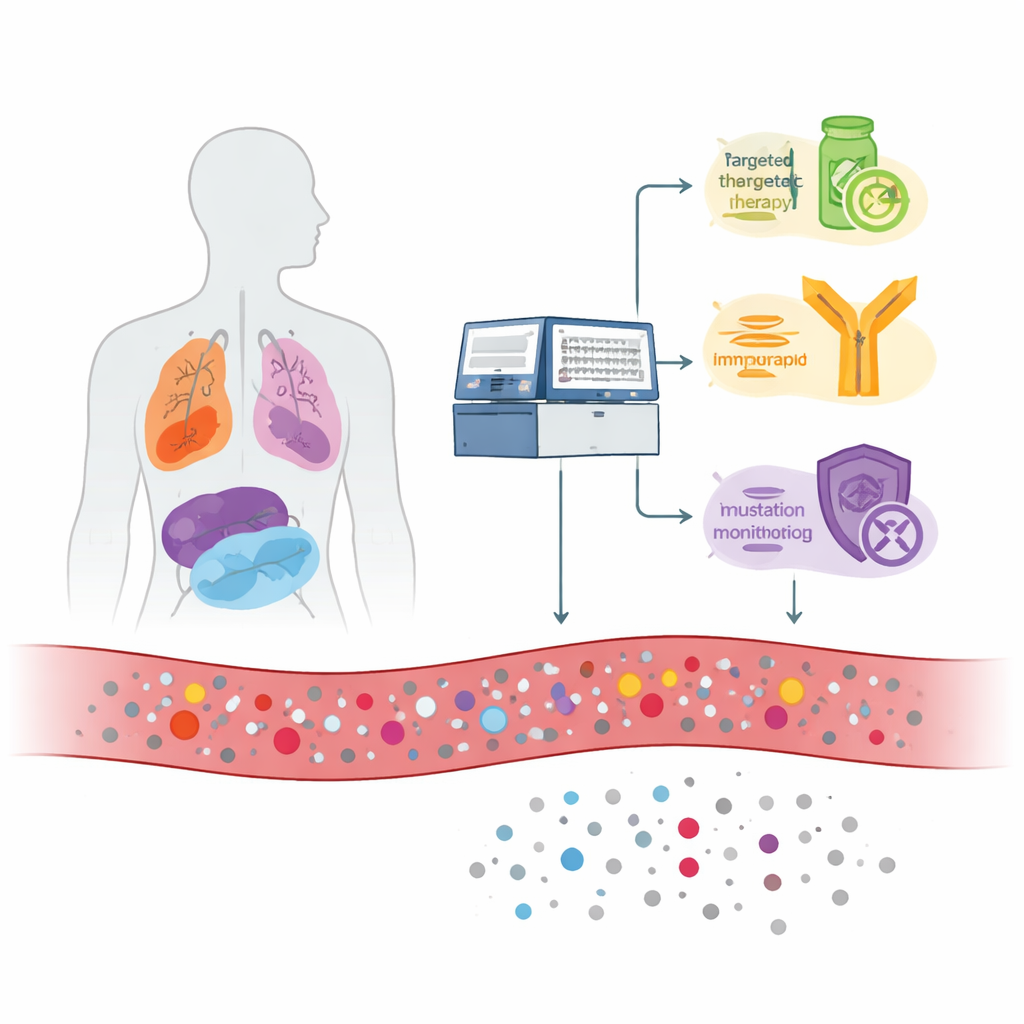
Vad blodet avslöjade om tumörer
Blodtestet upptäckte cancerrelaterade DNA‑förändringar hos ungefär två tredjedelar av patienterna. Många av dessa förändringar pekade direkt på behandlingsmöjligheter. Hos cirka 16 % av patienterna hittade testet «on‑label»-mål—mutationer kopplade till läkemedel som redan är godkända för den specifika cancerformen, såsom vissa förändringar i EGFR vid lungcancer eller PIK3CA och ESR1 vid bröstcancer. När forskarna även räknade «off‑label»-mål (mutationer med läkemedel godkända för andra cancerformer), förändringar som studerades i kliniska prövningar och mutationer kända för att ge läkemedelsresistens, hade mer än hälften av alla patienter minst en potentiellt användbar fyndighet. Testet beräknade också två bredare DNA‑egenskaper—tumörmutationsbörda och mikrosatellitinstabilitet—som kan indikera patienter som kan svara på hämmare av immunkontrollpunkter; nästan 9 % av patienterna verkade vara kandidater för sådan immunterapi baserat på blodet ensam.
Olika cancerformer, olika signalstyrka
Alla tumörer släpper inte ut DNA i blodet i samma grad. Cancerformer som kolorektal, prostata och bröst avger ofta tillräckligt med DNA så att testet lätt kan upptäcka flera förändringar, medan hjärntumörer och många sarkom avger mycket lite, delvis på grund av fysiska barriärer som blod‑hjärnbarriären eller eftersom deras DNA‑förändringar är av typer som är svårare att upptäcka. Forskarna uppskattade för varje patient andelen cellfritt DNA i blodet som kom från tumören. Denna «tumörandel» var generellt låg—ungefär 2 % i genomsnitt—troligen eftersom många patienter redan fick behandling, vilket minskar tumörbördan och mängden tumör‑DNA i cirkulation. Ändå hjälpte den breda genpanelen till att bekräfta när tumör‑DNA verkligen fanns närvarande, vilket gjorde ett «negativt» resultat mer tillförlitligt i cancerformer som avger DNA i måttlig grad.
Följa cancer över tid och upptäcka ärftlig risk
En delmängd av patienterna testades med blodprov mer än en gång. För några som initialt var negativa blev senare tester positiva när tumör‑DNA‑nivåerna steg, vilket tyder på sjukdomsprogress snarare än plötslig uppkomst av resistens. Hos andra dök nya mutationer upp vid senare tester som är kända för att orsaka resistens mot målinriktade eller hormonella behandlingar, vilket visar hur seriemässiga blodprov kan fånga tumörens flyktrutter tidigare än enbart bilddiagnostik. Samtidigt gjorde sekvensering av vita blodkroppar att teamet kunde upptäcka ärftliga (germline) mutationer i cancer‑riskgener såsom BRCA1 och BRCA2. Runt 11 % av patienterna bar sådana ärftliga förändringar, vilket kan påverka både deras egen behandling—som möjlig rätt till PARP‑hämmare—och screeningsrekommendationer för deras familjer. 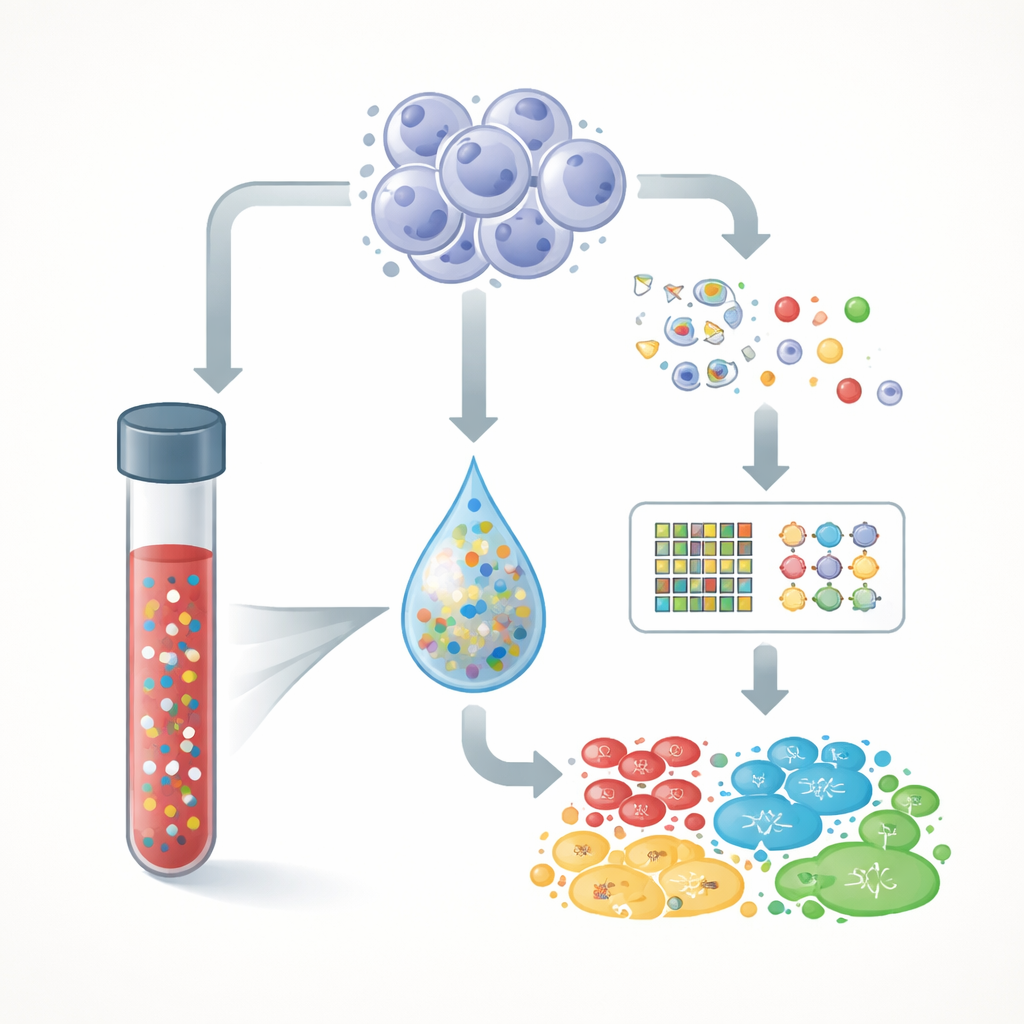
Hur blodtest och vävnad kompletterar varandra
För 145 patienter kunde forskarna jämföra blodresultaten direkt med tumörvävnad. För de viktigaste läkemedelskopplade mutationerna var överensstämmelsen mellan blod och vävnad stark: ungefär 90 % av gångerna var de ense om huruvida ett nyckelmål förekom eller inte. I vissa fall fångade blodtestning upp resistensförändringar som den tidigare vävnadsprovet missat, troligen eftersom tumören utvecklats under behandling. I andra fall avslöjade vävnad förändringar som inte var detekterbara i blod, ofta vid cancerformer som avger lite DNA. Detta mönster tyder på att blod och vävnad inte är rivaler utan partner: vävnadsprov förblir nödvändiga när lite tumör‑DNA cirkulerar, medan likvidbiopsi erbjuder snabbhet, mindre invasivitet och möjlighet att upprepa tester när sjukdomen förändras.
Vad detta betyder för patienter
För en lekmannapublik är budskapet i denna studie att ett enda blodprov nu kan ge en förvånansvärt komplett genetisk bild av många avancerade cancerformer. Genom att kasta ett brett nät över mer än tusen gener och noggrant separera tumörsignaler från bakgrund och ärftliga förändringar, upptäckte testet behandlingsalternativ och tecken på resistens hos majoriteten av patienterna, och identifierade nästan en av tio som möjliga kandidater för immunterapi. I kombination med traditionell vävnadsanalys ökar detta tillvägagångssätt chansen att hitta ett åtgärdbart mål, hjälper onkologer att snabbare välja och anpassa behandlingar och kan avslöja ärftliga risker som är viktiga för hela familjer. Även om det inte ersätter alla biopsier—särskilt vid cancerformer som frigör lite DNA i blodet—visar det hur likvidbiopsi håller på att bli en kraftfull, praktisk följeslagare till standardvården i verklig onkologisk praxis.
Citering: Florou-Chatzigiannidou, C., Papadopoulou, E., Metaxa-Mariatou, V. et al. Implementation of a 1021-gene liquid biopsy assay for real-world tumor genomic profiling in oncology practice. Sci Rep 16, 10064 (2026). https://doi.org/10.1038/s41598-026-40923-7
Nyckelord: likvidbiopsi, cirkulerande tumör‑DNA, cancergenomik, målinriktad terapi, hämmare av immunkontrollpunkter