Clear Sky Science · sv
En splicing‑härledd mikroRNA från amelogenin exon4 reglerar emaljbildning via kontroll av exon4‑splicing och amelogenin‑uttryck
Varför ett litet RNA spelar roll för starka tänder
Tandemalj är det hårdaste ämnet i människokroppen, men kan bli överraskande skört när dess bildning går fel. Denna studie avslöjar hur en mycket liten del av det genetiska materialet, en mikroRNA kallad miR‑exon4, hjälper tandbildande celler att bygga korrekt förhärdad emalj. Genom att visa att denna mikroRNA finjusterar både det huvudsakliga emaljproteinet och tidpunkten för mineralavsättning länkar arbetet subtil RNA‑bearbetning inne i celler till synliga emaljdefekter liknande dem som ses vid den ärftliga sjukdomen amelogenesis imperfecta.
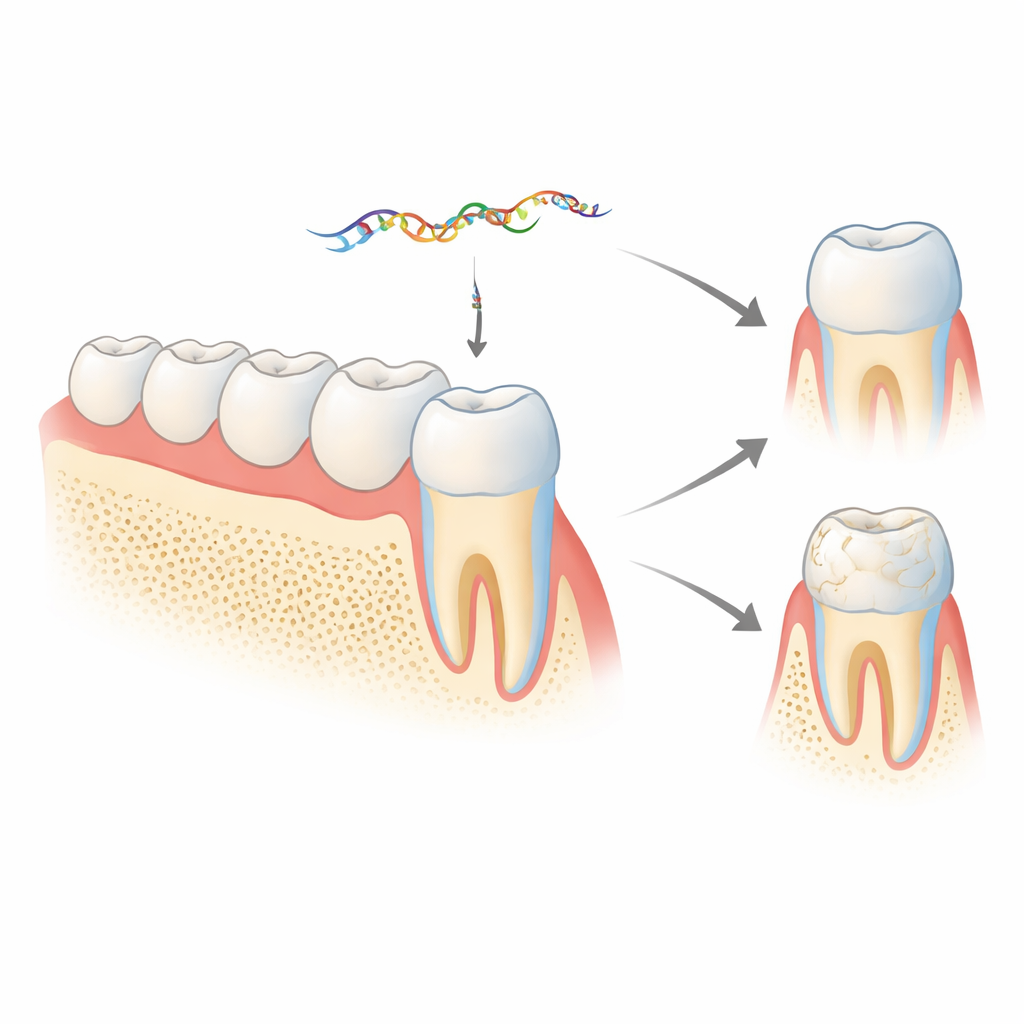
Ett dolt budskap inuti ett emaljgen
Emalj byggs till stor del av ett protein kallat amelogenin, som produceras av celler som kallas ameloblaster. Amelogenin‑genen (Amelx hos möss) kan klippas och klistras på olika sätt och skapa flera proteinvarianter som behövs i olika stadier av tandsutvecklingen. Ett kort segment, kallat exon 4, tas vanligtvis bort från det slutliga protein‑kodande budskapet. Tidigare arbete från gruppen visade att det bortkastade exon 4 inte är avfall: det bearbetas till en mikroRNA, miR‑exon4, som kan reglera andra gener viktiga för ben och emalj. Den nya studien undersöker vad som händer i levande djur när denna mikroRNA minskas eller blockeras, och om den också ger återkoppling för att kontrollera hur amelogenin själv sätts ihop.
En reglerande kedja inne i tandbildande celler
Forskarna bekräftade först i musbett att miR‑exon4 deltar i en regleringskedja som de tidigare kartlagt i celler odlade i labbet. I normala emaljorgan håller miR‑exon4 två upstream‑gener, Nfia och Prkch, i schack. När dessa hålls låga stiger nivåerna av en nyckel‑transkriptionsfaktor, RUNX2. Med hjälp av möss som antingen saknade amelogenin‑genen, fick extra miR‑exon4 eller behandlades med en miR‑exon4‑blockerare visade teamet att sänkning av miR‑exon4 ökar Nfia och Prkch och minskar RUNX2, medan tillförsel av miR‑exon4 har motsatt effekt. Detta bekräftade att miR‑exon4–Nfia/Prkch–RUNX2‑vägen fungerar in vivo inom utvecklande tänder.
Från störda signaler till svagare emalj
För att se hur dessa molekylära förändringar påverkar faktisk emalj inhiberade forskarna miR‑exon4 hos museungar under en vecka under aktiv tandbildning. Tredimensionell röntgenavbildning visade att behandlade djur hade en tydlig minskning av kraftigt mineraliserad emalj i både framtänder och kindtänder. Värmekartor och färgade snitt visade att starten av mineraluppbyggnad längs emaljlagret fördröjdes och att den tidiga mineraliseringsfasen förkortades, vilket ledde till grövre ytor och otydliga gränser mellan emalj och underliggande vävnader. Samtidigt föll RUNX2‑proteinnivåerna i ameloblaster, medan amelogenin‑protein — inklusive varianter som innehåller exon 4 — ökade. Detta mönster speglar tidigare modeller där överproduktion av en lång amelogeninform med exon 4 leder till emaljdefekter, vilket antyder att för mycket av denna isoform, utlöstad av förlust av miR‑exon4, kan störa normal mineralisering direkt.
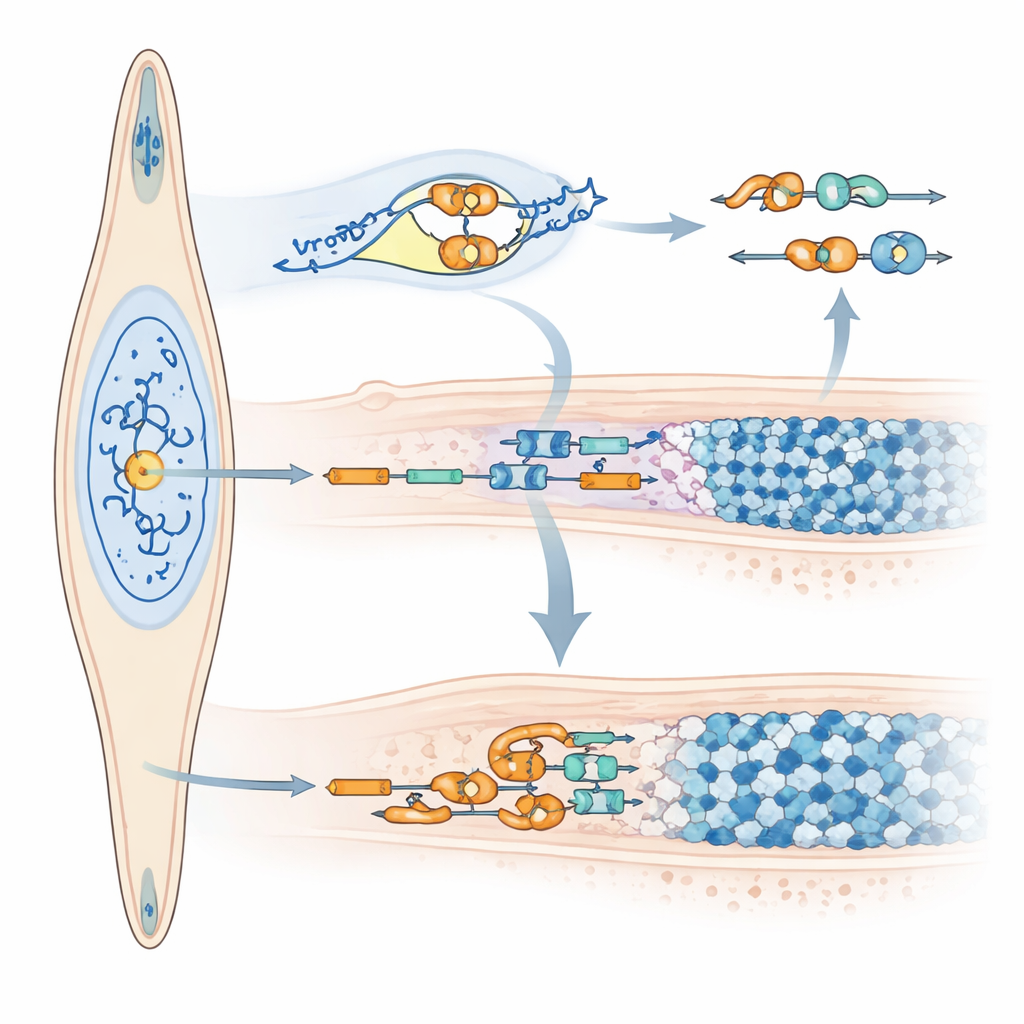
Hur mikroRNA:t omformar emaljbudskapet
Utöver att ändra hur mycket amelogenin som tillverkas påverkar miR‑exon4 också hur amelogenin‑budskapet klipps och splicas. Kortvarig blockering av miR‑exon4 minskade RNA‑molekyler som fortfarande innehöll exon 4 utan att förändra totala amelogeninnivåer, vilket indikerar att exon 4 oftare togs bort. Teamet kopplade denna förskjutning till förändringar i flera splicing‑regulatorgener (SRSF), där några ökade och andra minskade när miR‑exon4 reducerades. I cellmodeller som bär en specialkonstruerad version av amelogenin‑genen som producerar mindre miR‑exon4 hoppades exon 4 likaledes över oftare. Avgörande nog hittades mikroRNA:t självt inne i cellkärnan, där splicing sker, och biokemiska tester visade att det associerar med amelogeninets prekursor‑RNA vid en specifik kontrollpunkt i den intilliggande intronen. Dessa fynd stödjer en dubbelroll för miR‑exon4: att indirekt forma exonval genom att justera splicingfaktorer, och att direkt binda nära exon 4 för att påverka om det bevaras eller tas bort.
Vad detta betyder för emaljh�lsa
Tillsammans framställer studien miR‑exon4 som en liten men central koordinator av emaljbildning. När den finns i rätt nivå stöder den korrekt RUNX2‑aktivitet, håller amelogeninproduktionen i balans och hjälper till att säkerställa att exon 4 inkluderas eller exkluderas i rätt skeden. När miR‑exon4 saknas eller minskas skiftar denna balans: signalvägar störs, exon 4 hanteras felaktigt, amelogeninisoformer blir skeva och tidig emaljmineralisering försvagas. Dessa insikter hjälper till att förklara hur vissa mutationer i amelogenin‑genen kan orsaka ärftliga emaljsjukdomar, och de lyfter fram nukleära mikroRNA som viktiga aktörer i formandet av kroppens hårdaste vävnad.
Citering: Shemirani, R., Duong, T., Kim, R. et al. A splicing-derived microRNA from amelogenin exon4 regulates enamel formation via control of exon4 splicing and amelogenin expression. Sci Rep 16, 11044 (2026). https://doi.org/10.1038/s41598-026-40706-0
Nyckelord: tandemalj, amelogenin, mikroRNA, RNA‑splicing, amelogenesis imperfecta