Clear Sky Science · sv
ABE9 sammanfogat med SpRY Cas9-nickas möjliggör precis generering av musemodeller utan förbipasserande mutationer
Skarpare verktyg för att bygga bättre sjukdomsmodeller
Många allvarliga sjukdomar orsakas av enstaka bokstavsfel i vårt DNA. För att förstå och så småningom behandla dessa tillstånd skapar forskare ofta möss som bär samma mutationer som mänskliga patienter. Men att skriva om DNA med sådan precision är överraskande svårt: äldre metoder kan lämna ärr i genomet, införa extra mutationer och förvanska experimentella resultat. Denna studie presenterar ett förfinat genredigeringsverktyg, kallat ABE9-SpRY, utformat för att ändra en specifik DNA-bokstav samtidigt som intilliggande baser — och resten av genomet — i stort sett lämnas orörda.
Från kraftfulla snitt till skonsamma DNA-justeringar
Traditionell CRISPR-Cas9-redigering fungerar som ett molekylärt saxpar och klipper båda DNA-strängarna. Celler reparerar dessa brott ofullständigt, vilket ofta lämnar små insättningar eller borttagningar som stör gener på oförutsägbara sätt. Det är användbart för att stänga av gener, men inte för att efterlikna en exakt sjukdomsuppevande mutation. Basredigerare däremot klipper inte DNA:t. Istället skjuter de kemiskt en bokstav till en annan — här från A till G — samtidigt som dubbelhelixen förblir intakt. Denna metod minskar dramatiskt stora deletioner och omsorteringar, men tidigare adeninbasredigerare led av tre huvudproblem: de redigerade ibland närliggande ”bystander”-baser, de kunde bara nå DNA‑ställen intill specifika korta sekvenstaggar, och de orsakade då och då förändringar på oavsiktliga platser i genomet.
Utformning av en mer selektiv molekylär penna
Forskarna satte som mål att angripa alla tre begränsningarna samtidigt. De började med ABE9, en nyare variant av basredigerare som riktar sin aktivitet mot ett mycket snävt DNA‑område och krymper ”redigeringsfönstret” så att betydligt färre intilliggande baser råkar förändras av misstag. De fäste sedan ABE9 vid en ingenjörsproducerad Cas9‑nickas kallad SpRY. Till skillnad från standard‑Cas9, som kräver en strikt ”NGG”-tagg intill målet, kan SpRY känna igen en mycket bredare uppsättning DNA‑sekvenser. Det gör det möjligt att nå sjukdomsrelaterade positioner i genomet som tidigare var otillgängliga. Den resulterande fusionen, ABE9‑SpRY, är avsedd att vara både mycket precis och betydligt mer flexibel i var den kan verka.
Att testa den nya redigeraren i celler och embryon
För att se om ABE9‑SpRY motsvarade sin design jämförde teamet den med en vida använd, mer aggressiv redigerare kallad ABE8e‑SpRY. De riktade in sig på fyra sjukdomsrelevanta positioner i gener som kodar för jonkanaler (TPC1, TPC2 och TRPM4), vilka spelar viktiga roller i hjärt- och leverfunktion. I musneuroner odlade i labbet redigerade ABE8e‑SpRY målbokstaven mer effektivt men ändrade också många närliggande baser. ABE9‑SpRY producerade däremot färre redigeringar totalt men en mycket större andel ”rena” utfall — sekvenser där endast den avsedda bokstaven ändrats, utan extra mutationer i det lokala området. Samma mönster sågs i musembryon. När forskarna injicerade redigeringskomponenter i befruktade ägg konverterade ABE8e‑SpRY ofta nästan alla kopior av målgenen men med många förbipasserande förändringar. ABE9‑SpRY redigerade färre kopior totalt, men där den verkade var DNA‑sekvensen vanligtvis korrigerad exakt enligt plan.
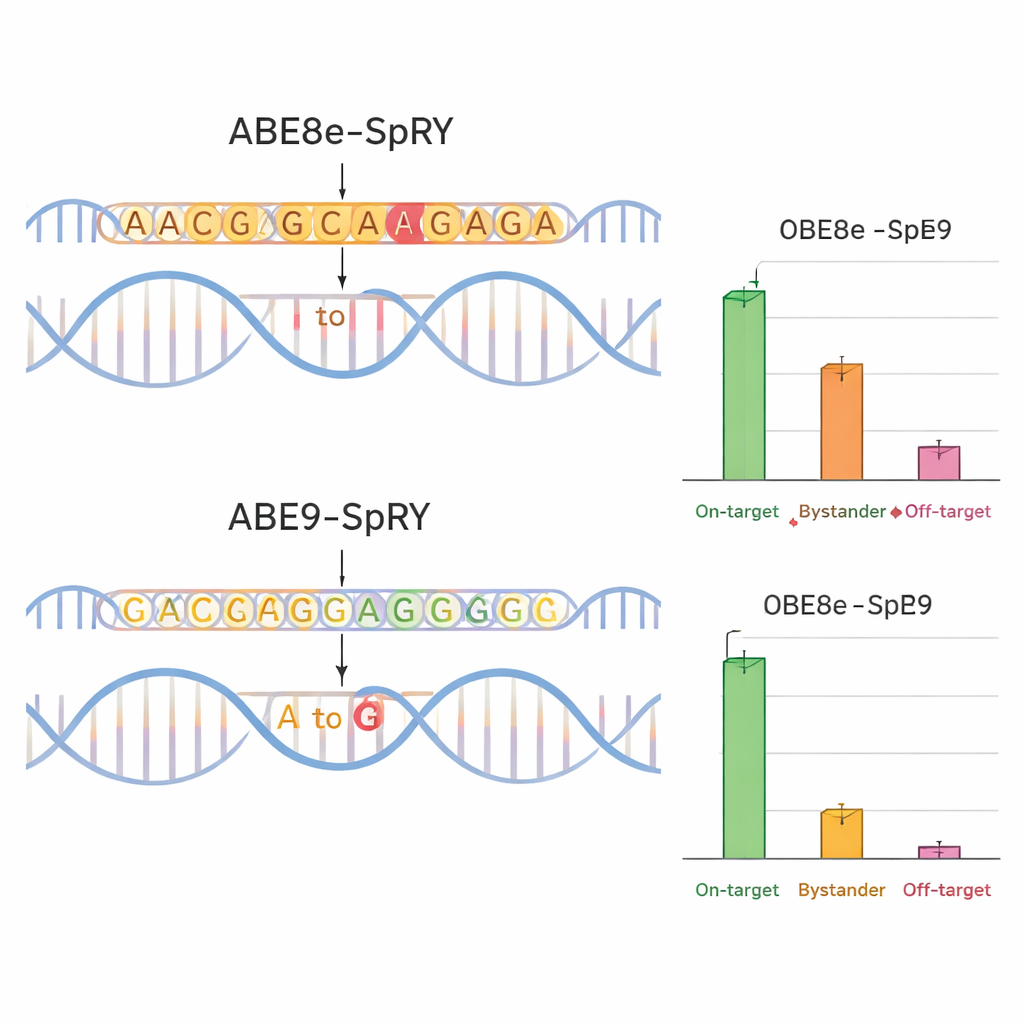
Renare redigeringar, färre biverkningar
Precision handlar inte bara om den lokala DNA‑omgivningen. Teamet undersökte också om deras redigerare förändrade avlägsna regioner i genomet. Genom att använda beräkningsmässiga förutsägelser och riktad sekvensering mätte de off‑target‑förändringar vid sannolika liknande platser i musembryon. ABE8e‑SpRY införde ofta oavsiktliga A‑till‑G‑förändringar på dessa lokaler, ibland på förvånansvärt höga nivåer. ABE9‑SpRY visade långt färre sådana händelser, med endast sällsynta off‑target‑redigeringar och ingen upptäckt aktivitet i ett specialiserat test för Cas9‑oberoende DNA‑skada. Viktigt är att när ABE9‑SpRY användes ensamt — inte i poolade tester — för att införa två specifika mutationer i möss, genererade det många grundarindivider där den önskade redigeringen fanns på höga nivåer och fördes vidare till avkomman på ett tillförlitligt sätt, återigen med minimala förbipasserande förändringar eller små insättningar och deletioner.
Att utöka precisionsredigering till mänskliga stamceller
Eftersom patient‑specifika stamceller i ökande grad används för att studera sjukdomar och testa läkemedel, testade forskarna även ABE9‑SpRY i mänskliga inducerade pluripotenta stamceller. De riktade den mänskliga versionen av TPC1‑genen vid en position motsvarande en av musplatserna. Med hjälp av en fluorescerande reporter för att berika för redigerade celler fann de att ABE8e‑SpRY gav högre råa redigeringsnivåer men återigen modifierade flera intilliggande baser. ABE9‑SpRY redigerade färre alleler totalt, men andelen perfekt redigerade sträckor — en avsedd förändring och inget mer — var markant högre, med färre störande insättningar eller deletioner. I stamcellsarbete, där individuella kloner expanderas för detaljerade studier, är denna typ av ”rengjord” redigering oftast mer värdefull än rå effektivitet.
Varför detta är viktigt för framtida sjukdomsforskning
För forskare som försöker förstå hur en enda DNA‑bokstavsförändring leder till sjukdom kan extra oavsiktliga mutationer vara djupt missvisande. Denna studie visar att ABE9‑SpRY, även om den är något mindre kraftfull i termer av rå redigeringshastighet, kan skriva in enstaka bokstavsförändringar i genomerna hos möss och mänskliga stamceller med slående noggrannhet och bred målinriktad flexibilitet. Det gör den till en lovande arbetshäst för att bygga trogna djur‑ och cellmodeller av mänskliga genetiska sjukdomar, särskilt i situationer där även en enda felaktig mutation skulle kunna förvirra biologin eller stjälpa en potentiell terapi.
Citering: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Nyckelord: adeninbasredigering, CRISPR-sjukdomsmodeller, musgenetik, off-target-effekter, hiPSC-genredigering