Clear Sky Science · sv
Pancreatitassocierad chymotrypsin C (CTRC)-variant p.R240Q försämrar selektivt nedbrytningen av trypsinogen genom att störa långdistans elektrostatisk interaktion
Varför detta är viktigt för pankreashälsa
Kronisk pankreatit är en smärtsam, långvarig inflammation i bukspottkörteln som kan leda till diabetes, matsmältningsproblem och en allvarlig försämring av livskvaliteten. Denna studie undersöker varför vissa människor är mer sårbara på grund av små ärvda förändringar i sina matsmältningsenzymer. Genom att zooma in på en enskild genetisk variant i ett skyddande enzym visar forskarna hur en subtil molekylär förändring kan rubba balansen från skydd till självdestruktion inne i bukspottkörteln.
Ett inbyggt säkerhetssystem i matsmältningen
Vår bukspottkörtel producerar kraftfulla proteinspjälkande enzymer som normalt släpps ut i tarmen i en inaktiv form. En av dessa föregångare, trypsinogen, kan ibland aktiveras för tidigt, inne i själva pankreas. När det händer kan det börja bryta ner organet inifrån och utlösa inflammation. För att hålla detta under kontroll använder kroppen skyddsmekanismer, inklusive en hämmande protein (SPINK1) och ett annat matsmältningsenzym, chymotrypsin C (CTRC). CTRC har en dubbel roll: det hjälper till att aktivera matsmältningsenzymer när och där de behövs, men det klipper också sönder överskott av trypsinogen innan det kan omvandlas till aktivt trypsin och orsaka skada. Personer som ärver försvagade former av CTRC har visat sig ha högre risk för kronisk pankreatit.
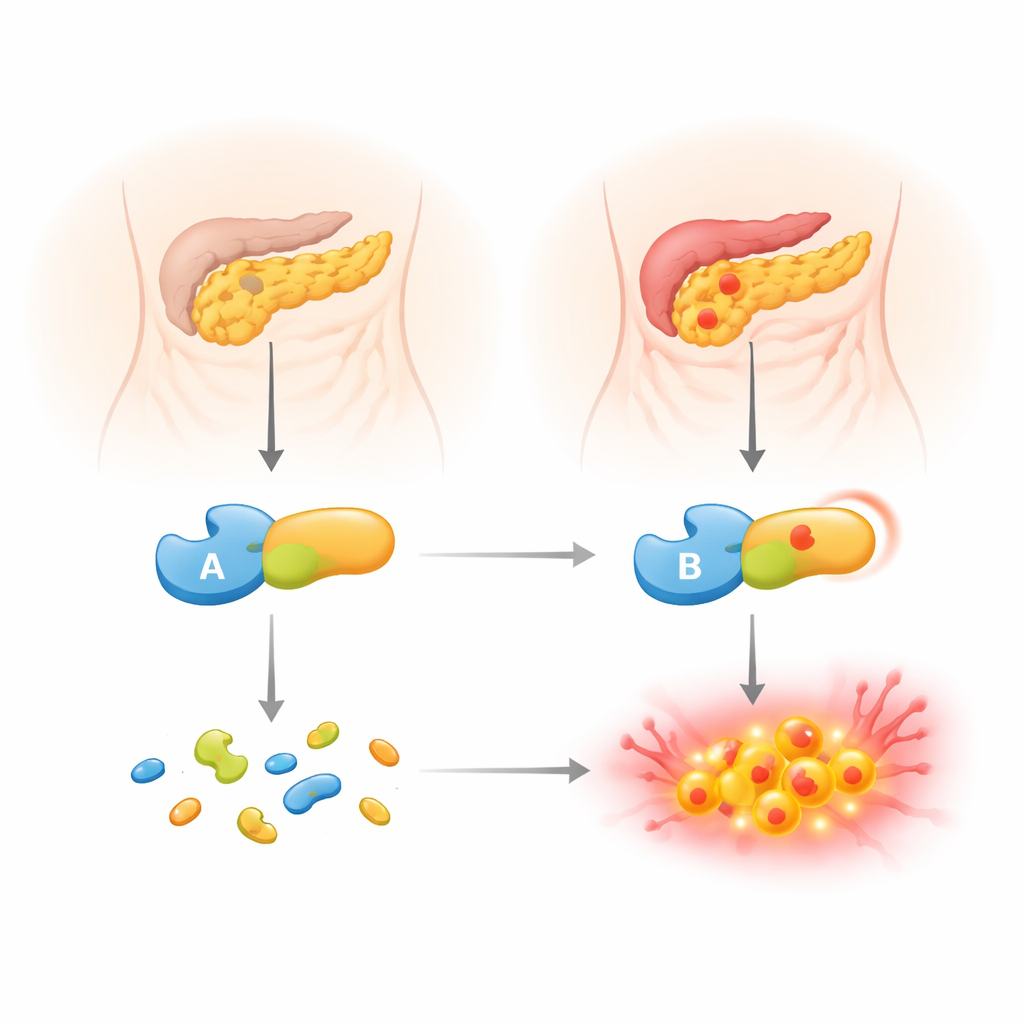
En ovanlig genetisk förändring under mikroskopet
Teamet fokuserade på en ovanlig CTRC-variant kallad p.R240Q, påvisad hos en pojke från Slovakien med barnbörjan av kronisk pankreatit och hos hans drabbade far. Denna variant ändrar ett enda byggblock på enzymets yta och byter ut en positivt laddad enhet mot en neutral. Stora genetiska databaser klassificerar den som sannolikt ofarlig, men den har dykt upp i flera unga patienter med sjukdomen. För att ta reda på vad den verkligen gör kombinerade författarna familjens genetiska information med detaljerade laboratorieexperiment. De jämförde variantenzymet sida vid sida med normalt CTRC, och undersökte hur väl det produceras av celler, hur aktivt det är på standardtestsubstrat och hur det interagerar med trypsinogen, det centrala ämnet det ska kontrollera.
Normal styrka, men felriktat sikte
Först visade forskarna att celler tillverkar och sekrerar p.R240Q-enzymet lika väl som den normala versionen, så varianten orsakar inte missfällning eller produktionsfel. I test-tube-assays med en liten syntetisk peptid och ett mjölkprotein (beta-kasein) fungerade varianten lika bra eller till och med något bättre än normalt CTRC. Det betyder att dess klyvningsförmåga är intakt. Överraskningen kom när de undersökte den reaktion som betyder mest för pankreatit: nedbrytningen av humant kationiskt trypsinogen. Här var variantenzymet mycket mindre effektivt—ungefär fyra till fem gånger långsammare på att klyva trypsinogen och betydligt sämre på att förhindra att trypsinogen autoaktiveras till trypsin. I autoaktiveringsförsök krävdes mycket mer variant-CTRC för att hålla trypsinnivåerna i schack jämfört med det normala enzymet.
En störd elektrostatisk "traktorstråle"
För att förstå varför detta sker använde författarna strukturella modeller av CTRC. Runt fåra där CTRC greppar sina substrat finns en ring av positiv elektrisk laddning bildad av flera laddade aminosyror, inklusive den plats som förändras i p.R240Q. Trypsinogens regioner som CTRC måste klyva är starkt negativa, så denna positivt laddade ring fungerar som en långdistans "traktorstråle" som styr trypsinogen till rätt position. Genom att neutralisera en av dessa positiva platser försvagar p.R240Q-varianten denna distansattraktion. Enzymet är fortfarande skarpt, men det skadade styrsystemet gör att trypsinogen inte binder lika effektivt, så mindre av det bryts säkert ner. Andra substrat som inte är lika beroende av detta laddningsmönster bearbetas normalt, vilket förklarar den mycket selektiva defekten som observerades i experimenten.
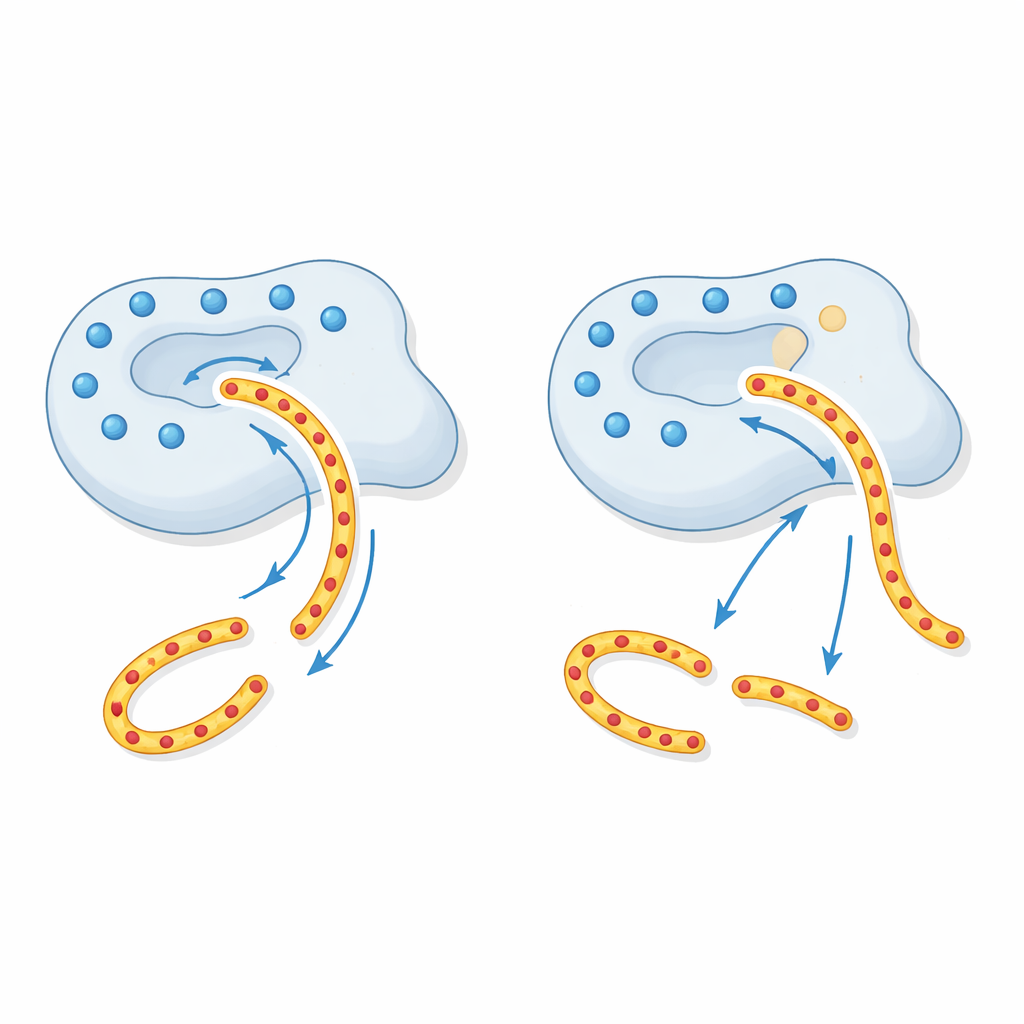
Vad detta betyder för patienter och testning
Kliniskt bar den drabbade pojken och hans far också en andra skadlig CTRC-variant, och fadern hade ytterligare livsstilsrisker såsom omfattande alkoholkonsumtion. Detta stämmer med idén att kronisk pankreatit ofta är ett resultat av flera genetiska och miljömässiga påverkansfaktorer som adderas. Arbetet visar att en variant som ser ofarlig ut enligt vanliga prediktionsverktyg ändå kan vara farlig på ett mycket specifikt sätt. För genetisk testning är budskapet tydligt: när man bedömer om en CTRC-variant ökar risken för pankreatit måste forskarna testa den mot det verkliga målet, trypsinogen, och inte bara mot generiska laboratoiresubstrat. I vardagliga termer visar denna studie hur en liten förändring i enzymets "styrande yta" i det fördolda kan undergräva ett av pankreas viktigaste säkerhetslås och föra känsliga individer närmare kronisk inflammation.
Citering: Nagy, Z.A., Sándor, M., Hegyi, E. et al. Pancreatitis-associated chymotrypsin C (CTRC) variant p.R240Q selectively impairs trypsinogen degradation through disruption of long-range electrostatic interactions. Sci Rep 16, 8937 (2026). https://doi.org/10.1038/s41598-026-40633-0
Nyckelord: kronisk pankreatit, chymotrypsin C, trypsinogen, genetisk variant, matspjälkningsenzymer