Clear Sky Science · sv
Svag bindning av anti-B7-H3-klon MJ18 till murint B7-H3 misslyckas med att inducera tumörregression
Varför detta är viktigt för cancerforskningen
Cancerimmunterapi bygger ofta på antikroppar — laboratorietillverkade proteiner utformade för att fästa vid tumörceller och hjälpa immunsystemet att förstöra dem. Ett lovande mål är molekylen B7-H3, som är riklig på många mänskliga cancerformer men sällsynt i frisk vävnad. Denna artikel granskar en flitigt använd forskningsantikropp, MJ18, som påståtts blockera B7-H3 i musstudier. Författarna finner att MJ18 knappt binder till sitt avsedda mål och inte hämmar tumörtillväxt, vilket väcker frågor om hur tidigare djurexperiment som använt detta verktyg bör tolkas.
Löftet om en cancerflagga på tumörceller
B7-H3 har väckt stort intresse eftersom den fungerar som en molekylär sköld: tumörer rika på detta protein tenderar att ha färre aggressiva immunceller inuti och är kopplade till sämre patientutfall. I flera musmodeller frigör borttagning av B7-H3-genen i tumörceller en kraftfullare immunattack och kan få tumörer att krympa eller försvinna. Dessa iakttagelser har drivit fram ansträngningar att utveckla läkemedel, ingenjörsmodifierade immunceller och antikropp-läkemedelskonjugat som siktar på B7-H3 på humana tumörer. Hur B7-H3 exakt dämpar immuniteten — och vilken receptor den interagerar med på immunceller — är dock fortfarande oklart, inte minst eftersom mus- och människovarianterna av B7-H3 skiljer sig strukturellt.
Ett ofta använt verktyg under lupp
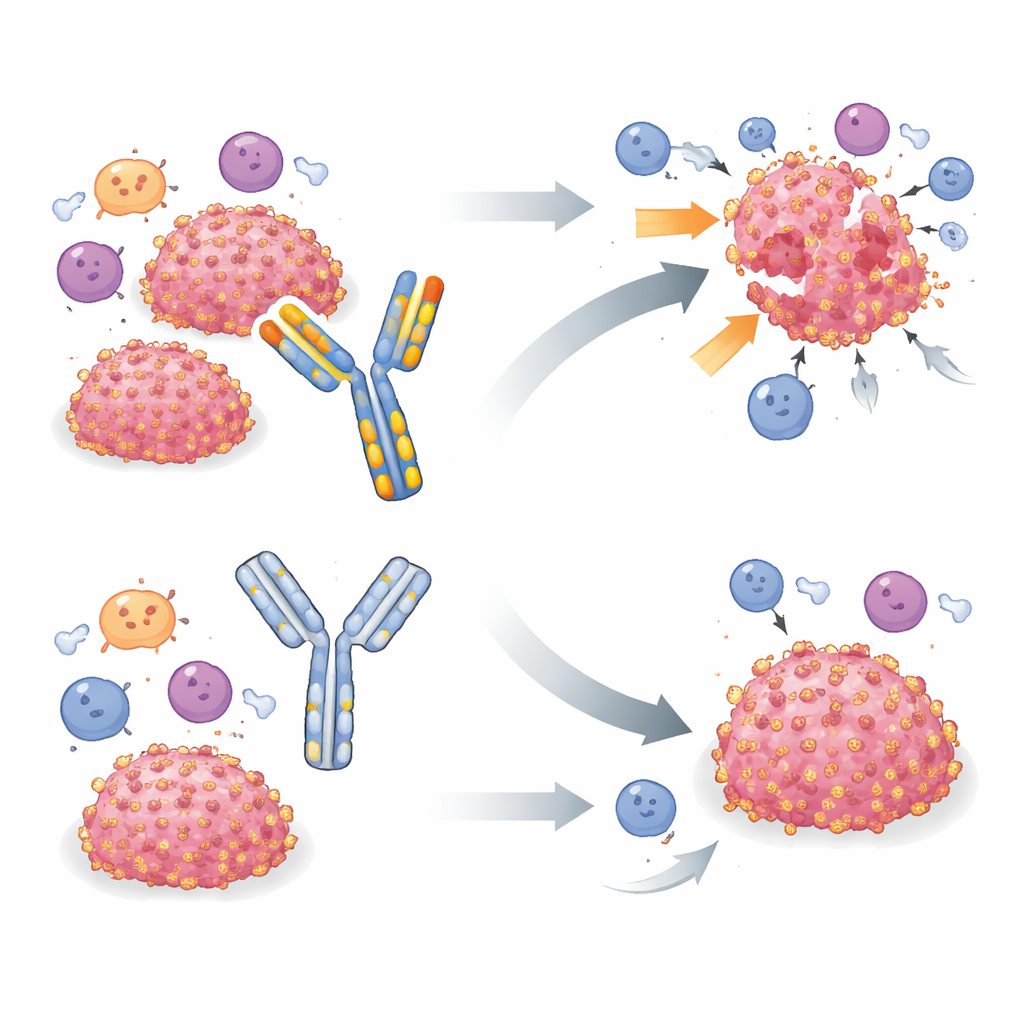
För att studera B7-H3 i levande möss har många grupper förlitat sig på en enda rått-deriverad antikropp kallad MJ18, som rapporterats känna igen mus-B7-H3 och blockera dess immundämpande aktivitet. Tidigare studier som använde MJ18 i olika sjukdomsmodeller, inklusive cancer, rapporterade ofta långsammare tumörtillväxt och bättre överlevnad. Det nuvarande teamet testade inledningsvis MJ18 i en musmodell av rhabdomyosarkom, en barndomssarkom där B7-H3 redan pekats ut som en viktig undanflyktsmekanism. När MJ18 misslyckades med att förbättra tumörkontrollen utvidgade forskarna sina tester till två andra B7-H3-positiva tumörtyper — pankreas- och bröstcancer — som tydligt är känsliga för borttagning av B7-H3-genen. I alla tre modellerna fördröjde eller eliminerade utslag av B7-H3 i tumörcellerna effektivt tumörer, men behandling av möss med MJ18 vid doser och scheman liknande dem i litteraturen gav ingen påtaglig effekt på tumörtillväxt eller överlevnad.
Test av om MJ18 verkligen träffar sitt mål
Författarna ställde sedan en grundläggande fråga som överraskande nog aldrig tidigare rigoröst adresserats: binder MJ18 verkligen till mus-B7-H3, och hur starkt? Med hjälp av flödescytometri jämförde de MJ18 med en annan antikropp, EPNCIR122, som var känd för att detektera B7-H3. På flera mus-tumörcellinjer gav EPNCIR122 en tydlig signal som försvann när B7-H3-genen knockades ut, vilket bekräftade dess specificitet. MJ18 visade däremot ingen övertygande bindning även vid hög koncentration. När de undersökte immunceller från mjälten band MJ18 visserligen, men mönstret matchade inte B7-H3, och EPNCIR122 upptäckte ingen B7-H3 alls på dessa celler, vilket tyder på att MJ18 fäster vid något annat.
Grävande i bindningspartnerna
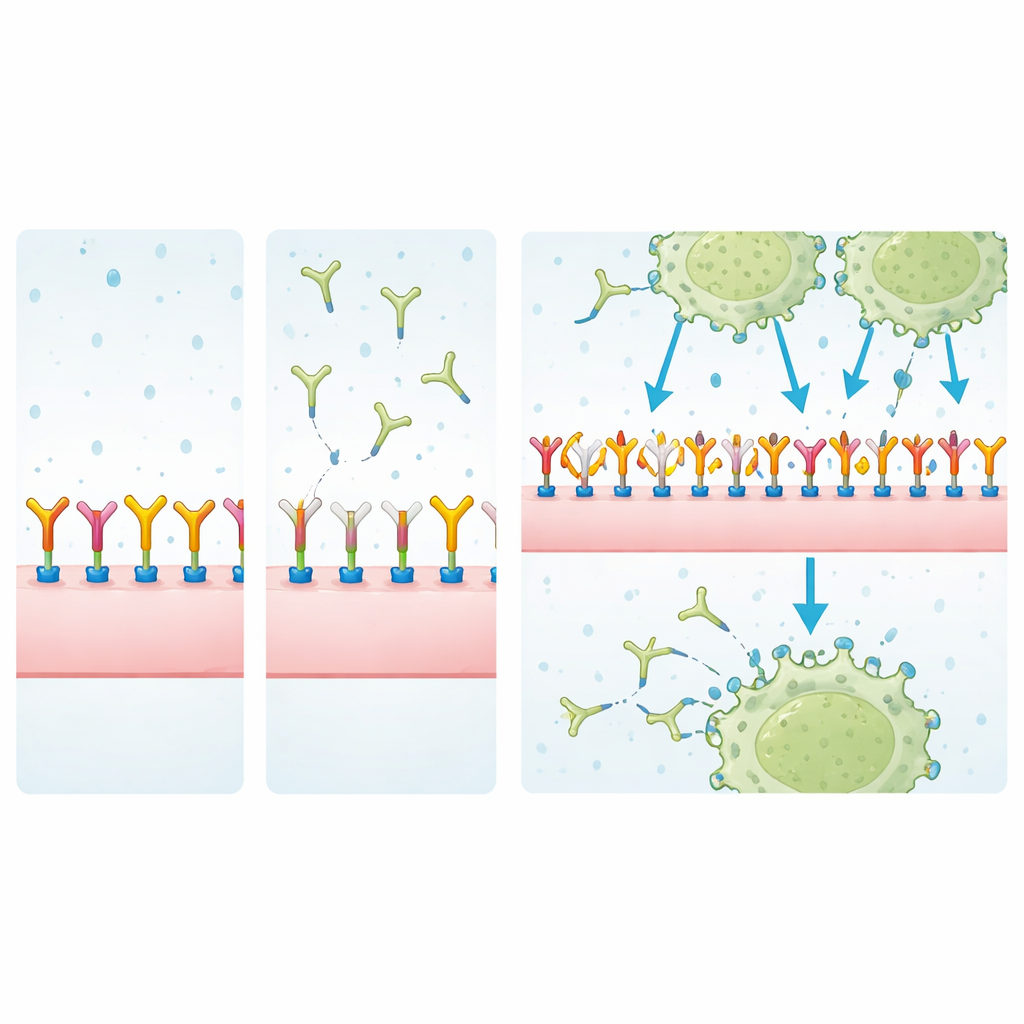
För att identifiera vad MJ18 egentligen kan känna igen drog forskarna ner cell-yta-proteiner med hjälp av MJ18 eller EPNCIR122 och analyserade dem med masspektrometri, samtidigt som de filtrerade bort vanliga bakgrundskontaminanter. I tumörceller berikade EPNCIR122 starkt B7-H3 över andra proteiner, vilket bekräftar att det är ett mycket specifikt reagens. MJ18 drog däremot ner en blandning av proteiner där B7-H3 bara förekom svagt och på nivåer som liknade icke-specifika bindare. Mätningar med ytplasmonresonans, en känslig teknik för att kvantifiera molekylära interaktioner, underströk poängen: MJ18:s affinitet för mus-B7-H3 var ungefär 7 000 gånger svagare än EPNCIR122 — långt under vad som är typiskt för terapeutiska antikroppar.
När antikroppar fångas upp av fel celler
Berättelsen slutade inte med svag bindning. I mjältceller visade ytterligare tester att MJ18 och liknande råttantikroppar erkändes av musens Fc-receptorer — molekyler på immunceller som naturligt binder antikroppars svansdel. Blockering av dessa receptorer reducerade kraftigt MJ18-signalen, vilket antyder att stor del av dess till synes specifika bindning härrörde från immunceller som grep antikroppen själv, snarare än att MJ18 riktade en specifik ytmolekyl. Försök att peka ut en unik proteinpartner för MJ18 på immunceller gav endast kandidater på nivåer omöjliga att skilja från bakgrundsbrus. Sammanlagt tyder data på att MJ18 till stor del beter sig som en låg-affinitets, icke-specifik antikropp vars interaktioner domineras av Fc-receptorinbindning snarare än exakt igenkänning av B7-H3.
Vad detta innebär framöver
För icke-specialister är huvudbudskapet enkelt: medan B7-H3 förblir ett övertygande måltavla på många cancerformer, är MJ18-antikroppen inte en pålitlig pil. Den binder B7-H3 i möss endast svagt och återskapar inte den kraftfulla tumörkontrollen som ses när B7-H3-genen tas bort. Tidigare musstudier som rapporterat dramatiska fördelar med MJ18 kan därför återspegla andra effekter — såsom hur antikroppens svans interagerar med immuncellsreceptorer — snarare än verklig blockad av B7-H3. Författarna hävdar att fältet akut behöver väl validerade, högaffinitiva antikroppar mot mus-B7-H3, och att forskare rutinmässigt bör bekräfta specificitet och bindningsstyrka för sådana verktyg. Endast med tillförlitliga reagenser kan insikter från djurmodeller ges förtroende att vägleda utvecklingen av nästa generations B7-H3–inriktade terapier för patienter.
Citering: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Nyckelord: B7-H3, cancerimmunterapi, antikroppsvalidering, immunkontroller, tumörmodeller