Clear Sky Science · sv
Teoretisk analys av lågenergetisk optogenetisk dämpning av aktionspotentialer i mänskliga ventrikulära kardiomyocyter uttryckta med kaliumselektiva kanalrhodopsiner
En mildare ljusbaserad metod för att lugna ett rusande hjärta
Snabba, kaotiska hjärtrytmer kan leda till svimning, stroke eller plötslig död. Dagens behandlingar — kraftfulla läkemedel, implanterade defibrillatorer eller högenergetiska stötar — kan rädda liv men är också smärtsamma och oprecisa. Denna studie utforskar en helt annan idé: att med svaga ljusblixtar och specialkonstruerade proteiner varsamt föra hjärtceller tillbaka till ett säkert, stabilt rytmläge, samtidigt som mycket mindre energi används än i nuvarande metoder.
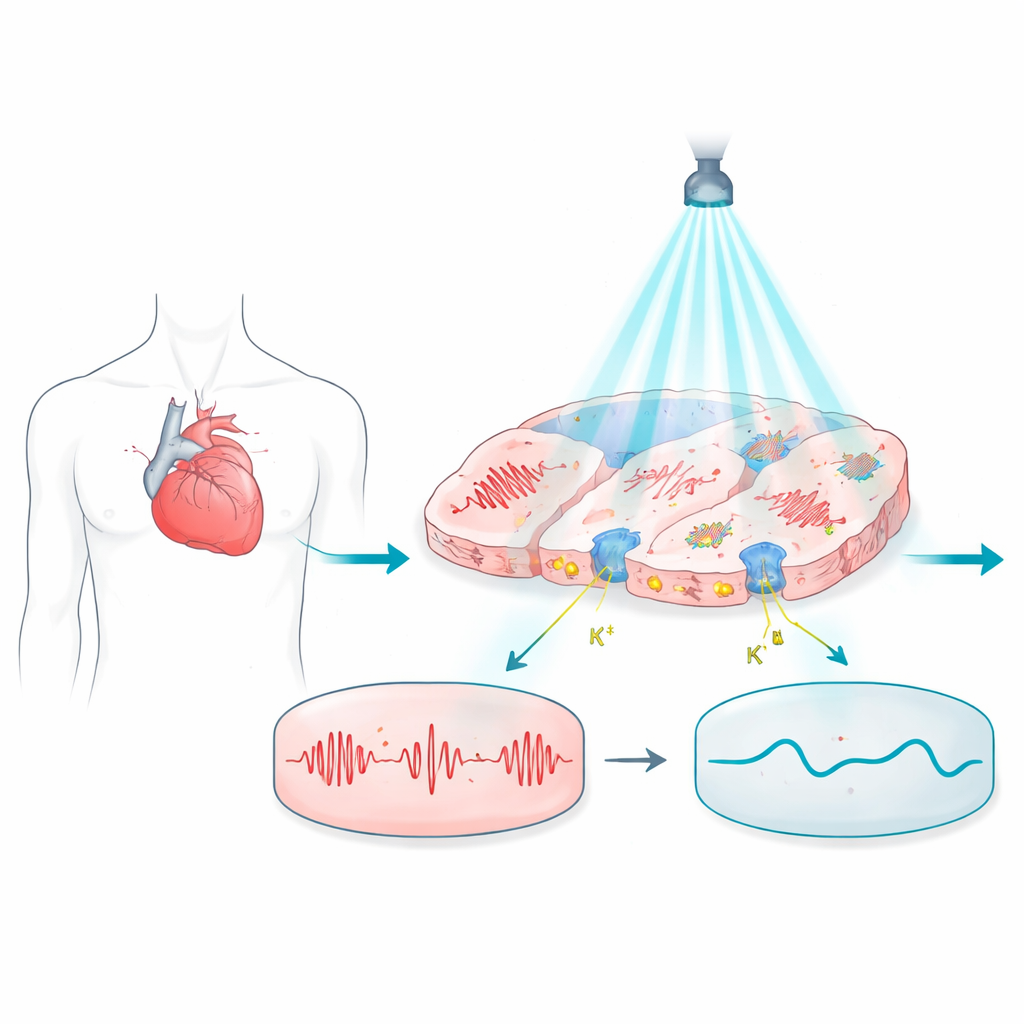
Att kasta ljus över problematiska hjärtslag
Arbetet bygger på optogenetik, en teknik där celler utrustas med ljuskänsliga proteiner så att deras elektriska aktivitet kan styras med ljusblixtar. I hjärtat kan dessa proteiner i princip ersätta metallelektroder och erbjuda kontaktfri, smärtfri kontroll. Men de flesta ljusstyrda proteiner som använts hittills tenderar att skjuta cellens spänning åt det positiva hållet, mot ett exciterat tillstånd, vilket gör det svårt att hålla cellerna tyst i vila eller att finjustera hur länge varje hjärtslag varar. Det begränsar deras användbarhet för att säkert stänga av farliga rytmer eller korrigera elektriska störningar som är beroende av subtil timing.
Nya ljusbrytare inställda på hjärtats "viloläge"
Nyligen upptäckta proteiner kallade kaliumselektiva kanalrhodopsiner, inklusive WiChR och HcKCR1, lovar att rätta till denna obalans. Till skillnad från äldre proteiner som släpper igenom en blandning av laddade joner, föredrar dessa kanaler starkt kalium och drar naturligt cellens spänning mot samma negativa nivå som vid vila. Författarna byggde detaljerade datormodeller av mänskliga ventrikulära hjärtceller som uttrycker dessa nyare kanaler och jämförde dem med två välkända, mer exciterande opsiner, ChR2(H134R) och ChRmine. Genom att simulera hur dessa celler svarar på olika ljusfärger och intensiteter kunde de säkert utforska förhållanden som skulle vara svåra eller tidskrävande att testa i verkliga hjärtan.
Mjukt ljus, stark kontroll
Simuleringarna visar att kaliumselektiva kanaler ger betydligt mer ekonomisk och stabil kontroll. WiChR, i synnerhet, kunde helt stänga av aktionspotentialer — de korta elektriska spikarna som triggar varje hjärtslag — med ljusintensiteter hundratals till tusentals gånger lägre än vad många tidigare verktyg kräver. Vid kontinuerligt ljus höll WiChR och HcKCR1 cellens spänning nära dess normala vilonivå och höll effektivt cellen i ett tyst, säkert tillstånd. Däremot tenderade ChR2 och ChRmine att driva spänningen mot mer positiva värden, ibland blockera aktivitet men bara efter att ha tvingat cellen in i ett stressat, överexciterat tillstånd. WiChR fungerade också väl med korta ljuspulser och förhindrade pålitligt hjärtcellerspikar slag för slag, vilket tyder på att den skulle kunna följa snabba hjärtrytmer utan att överhetta vävnad eller slösa energi.
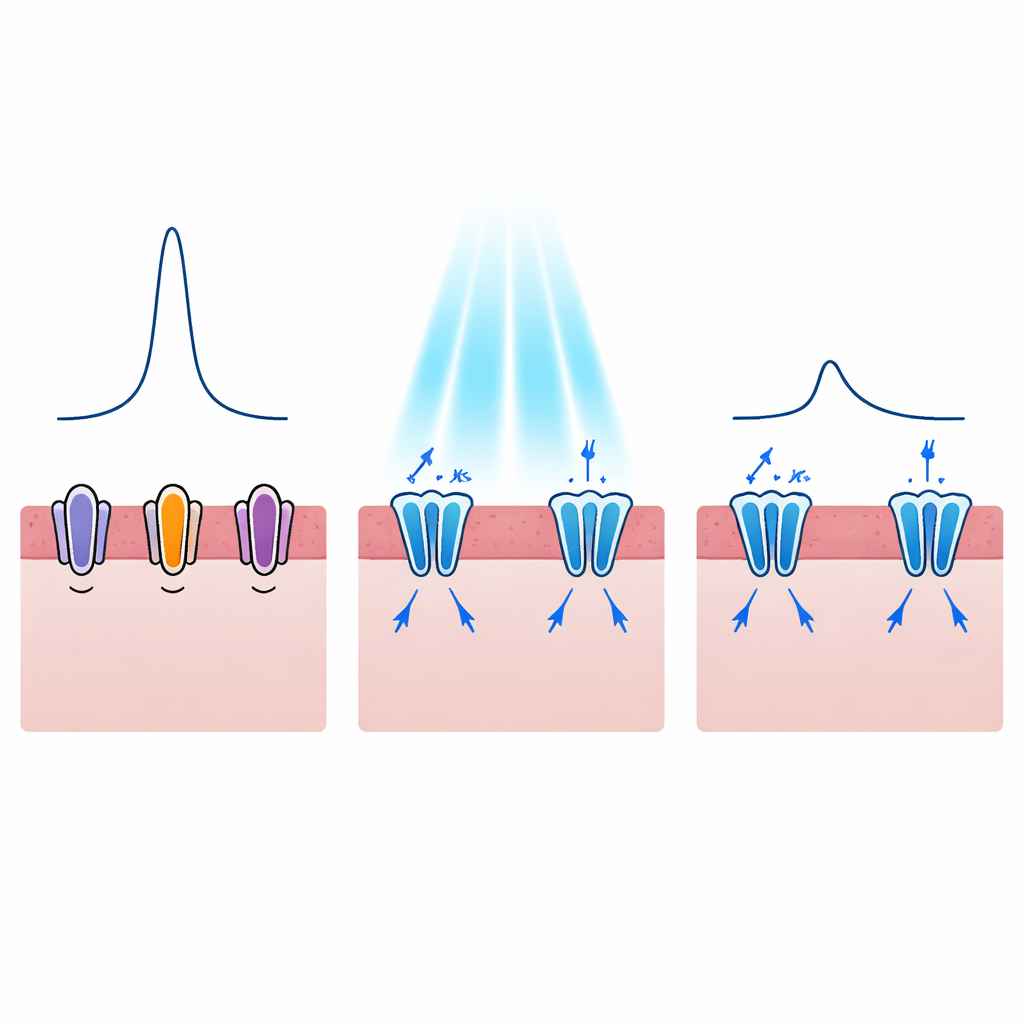
Omforma varje hjärtslag, inte bara stoppa det
Farliga arytmier hänger ofta inte bara ihop med om en hjärta cell avfyrar, utan också med hur länge den förblir exciterad. Vid sjukdomar som långt QT‑syndrom förlängs den elektriska pulsen för varje slag, vilket ökar risken för att utveckla dödliga rytmer. Författarna undrade därför om ljusaktiverade kaliumkanaler kunde förkorta denna puls på ett kontrollerat sätt. Deras modeller visade att aktivering av WiChR eller HcKCR1 under aktionspotentialens platåfas skapade starka utåtgående kaliumströmmar som drog ner spänningen tidigare. När ljusnivåerna ökade minskade varaktigheten av den elektriska pulsen från ungefär 300 millisekunder till cirka hälften, och denna effekt kunde uppnås även med mycket korta ljusblinkar. WiChR tenderade att ge längre varaktiga tysta perioder, medan HcKCR1 gav snabbare återhämtning när ljuset stängdes av, vilket antyder olika potentiella kliniska användningsområden.
Från datormodeller till framtida behandlingar
Sammanfattningsvis drar studien slutsatsen att kaliumselektiva ljusstyrda kanaler, särskilt WiChR, är lovande verktyg för skonsam, låg‑energi kontroll av hjärtat. De kan både tysta okontrollerad elektrisk aktivitet och korta av alltför långa hjärtslag, samtidigt som de håller cellens spänning nära dess naturliga viloläge. Även om resultaten bygger på detaljerade simuleringar av enskilda celler snarare än hela hjärtan, ger de kvantitativ vägledning om hur mycket ljus som kan behövas, när det bör appliceras och vilka proteinvarianter som passar bäst för olika mål. I längden pekar denna forskningsinriktning mot en framtid där kardiologer kan använda fint inställda ljusstrålar, i stället för smärtsamma stötar, för att förebygga eller stoppa livshotande arytmier.
Citering: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Nyckelord: hjärtoptogenetik, arytmi-dämpning, kaliumkanalrhodopsiner, aktionspotentialens varaktighet, långt QT‑syndrom