Clear Sky Science · sv
Kombinerade proteomik- och metabolomikanalyser avslöjade molekylära signaturer kopplade till proliferativ diabetisk retinopati
Varför detta är viktigt för personer med diabetes
Diabetisk ögonsjukdom är en av de ledande orsakerna till förebyggbar blindhet, men många patienter förlorar fortfarande synen trots moderna behandlingar. Denna studie skymtar in i den ”kemiska soppan” inne i ögat för att hitta tidiga varningssignaler och nya behandlingsmål för den svåraste formen av sjukdomen, kallad proliferativ diabetisk retinopati. Genom att mäta hundratals proteiner och små molekyler samtidigt lyfter forskarna fram ett fåtal som verkar driva skadlig blodkärlsväxt och inflammation i det diabetiska näthinnan.
Att titta in i ögats inre ocean
Den klara gelén som fyller ögat, känd som glaskroppen, ligger tätt intill den ljuskänsliga näthinnan och speglar tyst vad som händer i den känsliga vävnaden. Forskargruppen samlade odiluerade glaskroppsprover från åtta personer med avancerad proliferativ diabetisk retinopati och sex icke-diabetiska patienter som genomgick operation för ett annat, icke-inflammatoriskt ögentillstånd. Därefter använde de två kraftfulla ”omik”-metoder parallellt: proteomik för att katalogisera proteiner och metabolomik för att följa små metaboliska molekyler. Statistiska verktyg användes för att se hur de diabetiska och icke-diabetiska proverna klustrade sig och vilka komponenter som förändrades mest mellan grupperna. 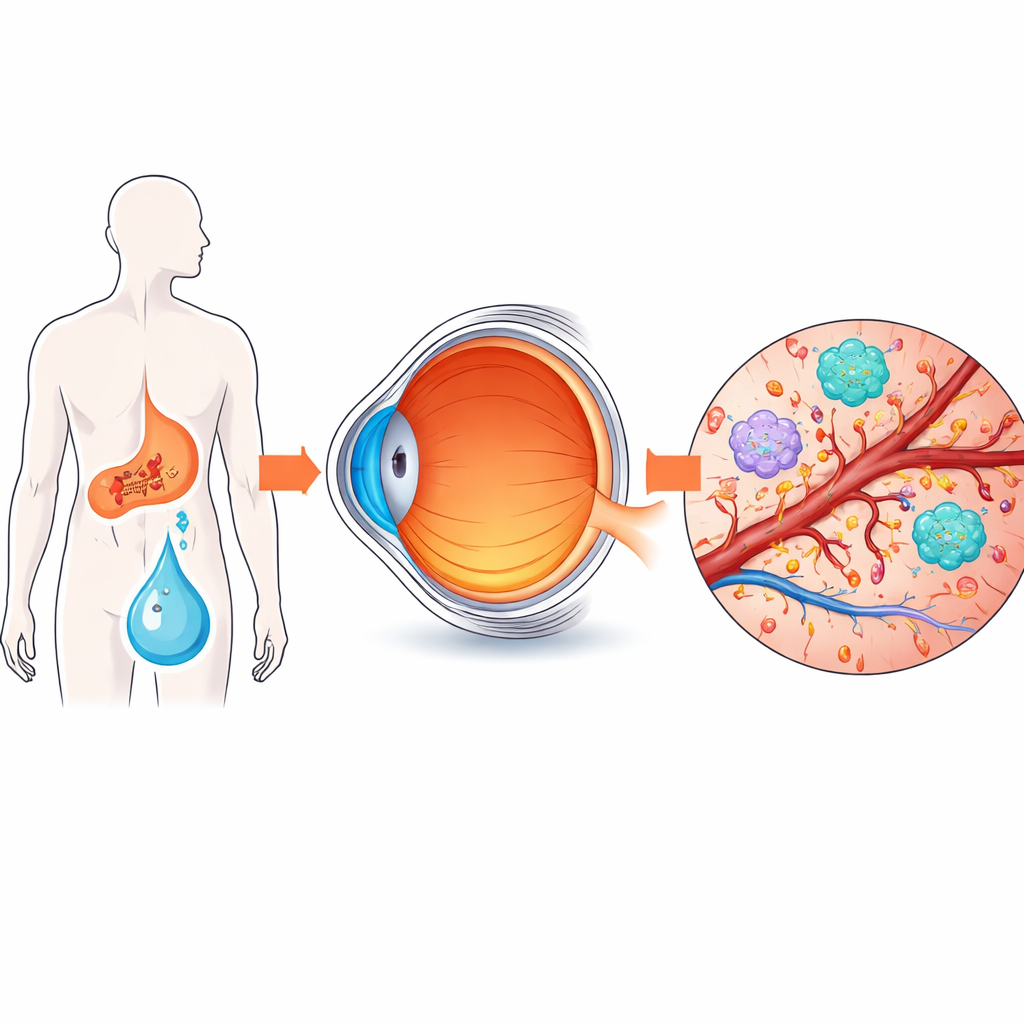
Nyckelstörningsmakare och saknade skyddare
Den kombinerade analysen avslöjade 81 proteiner och 26 metaboliter som skiljde sig mellan diabetiska och kontrollögon. Av dessa fokuserade forskarna på sju proteiner och sex metaboliter som var mest tätt sammankopplade. Tre proteiner stack ut. CD5L, ett immunrelaterat protein, var högre i diabetiska ögon, medan CLU (clusterin) och SERPINF1 (som producerar en skyddande faktor ofta kallad PEDF) var lägre. Uppföljande tester i patientprover och i en råttmodell av diabetisk retinopati bekräftade detta mönster både i ögonvätskan och i själva näthinnan. Enkelt uttryckt var faktorer som vanligtvis dämpar inflammation och håller kärlen stabila uttunnade, medan en faktor som kan driva celler mot tillväxt och aktivering ökade.
Energi-stress och läckande blodkärl
Metabolitdata lade till ytterligare ett lager i berättelsen. Många av de förändrade molekylerna hörde till fettsyre- och organiska syragrupper, med flera kopplade till cellernas energihantering. Kreatin, en välkänd energireserv för hårt arbetande vävnader som nerver och kärlbeklädnad, var reducerad. Det tyder på att näthinnans celler vid diabetes kan gå på en instabil energiförsörjning, vilket kan förvärra stress och skada. När forskarna kombinerade protein- och metabolitresultaten såg de att dessa förändringar koncentrerades i vägar som styr blodkoagulation, komplement (en del av immunsystemet) och svar på skada. Tillsammans pekar de mot ett scenario där kroniskt högt socker tippar balansen mot inflammation, mikrotromber och läckande, sköra mikrokärl.
Inzoomning på en nyckelsignal
För att testa om något av de förändrade proteinerna aktivt driver sjukdomsliknande beteende vände sig teamet till cellkultur. De tillsatte extra CD5L till musblodkärlsceller och observerade vad som hände. Med denna enda förändring började cellerna dela sig snabbare och röra sig lättare — två grundläggande beteenden som krävs för att nya kärlutsprång ska bildas. Detta stöder idén att ett överskott av CD5L i diabetiska ögon kan hjälpa till att driva den onormala blodkärlsväxt som kännetecknar proliferativ diabetisk retinopati. Samtidigt tar förlusten av CLU och SERPINF1 sannolikt bort viktiga bromsar på inflammation och kärlöverväxt, vilket förvärrar problemet. 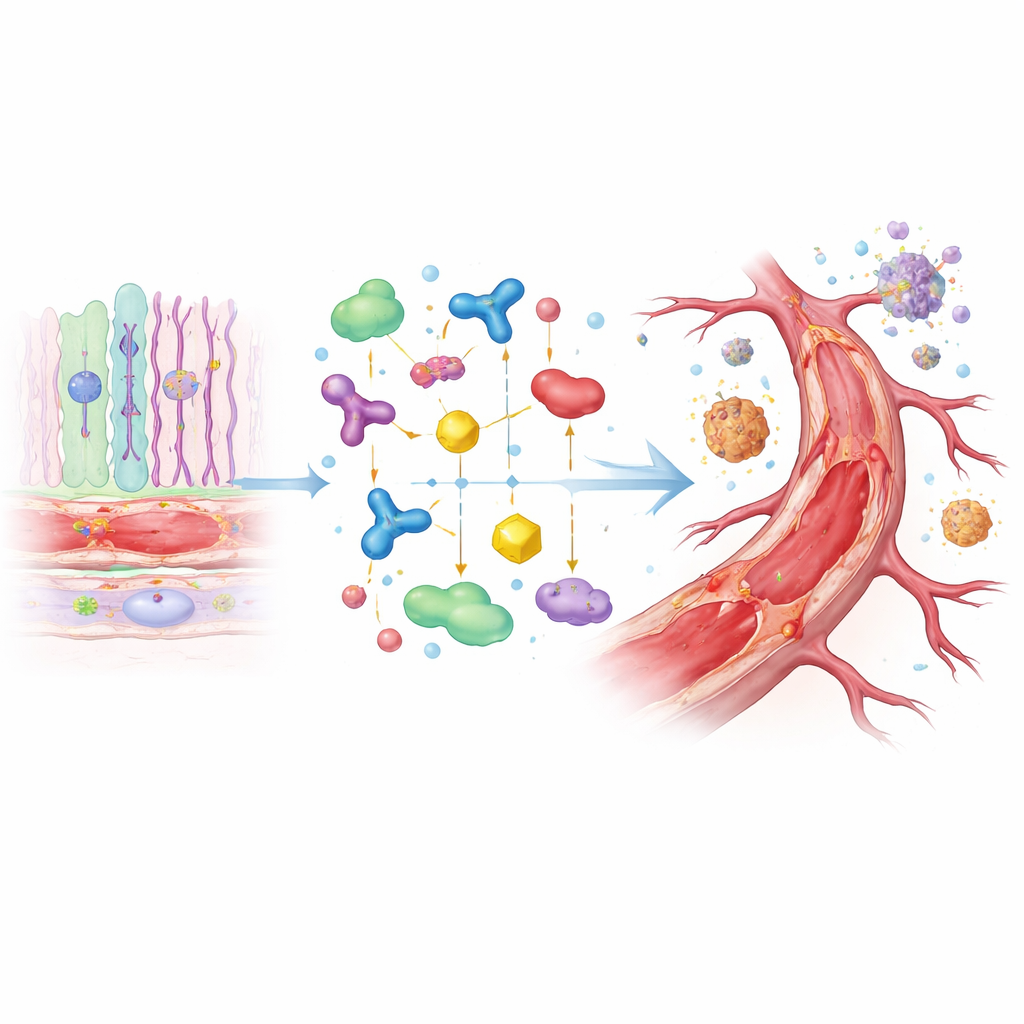
Vad detta kan innebära för framtida vård
Tillsammans skissar fynden en mer komplett bild av proliferativ diabetisk retinopati: inte bara som en sjukdom av högt blodsocker och överaktiva tillväxtsignaler som VEGF, utan som ett samordnat sammanbrott i immunbalans, kärlstabilitet och cellulär energianvändning. De framhävda proteinerna och metaboliterna skulle kunna fungera som biomarkörer för att flagga patienter med högre risk innan allvarlig skada uppstår. De antyder också nya behandlingsvägar, såsom läkemedel som dämpar CD5L:s pro-tillväxtpåverkan eller återställer skyddande molekyler som SERPINF1 och CLU. Även om studien är liten och delvis bygger på djurmodeller, erbjuder den en karta för att omvandla komplex molekylär data till praktiska strategier för att bättre skydda synen hos personer som lever med diabetes.
Citering: Cui, Y., Rao, L., Shen, L. et al. Combined proteomics and metabolomics analyses revealed molecular signatures associated with proliferative diabetic retinopathy. Sci Rep 16, 9755 (2026). https://doi.org/10.1038/s41598-026-40551-1
Nyckelord: diabetisk retinopati, retinala blodkärl, multi-omik, ögoninflammation, biomarkörer