Clear Sky Science · sv
Upptäckt av hydroxytriazol som potentiell glyoxalase‑I‑hämmare med datorstödda läkemedelsdesignmetoder
Varför att stoppa en liten cellulär städare kan bekämpa cancer
Cancerceller växer ofta så snabbt att de drunknar i sitt eget avfall. Ett av deras överlevnadstrick är en inbyggd rengöringspatrull som avgiftar skadliga biprodukter från sockerförbränning. Denna studie undersöker hur man kan stänga av en nyckelmedlem i den patrullen, ett enzym kallat glyoxalase‑I, genom att använda datorer för att sålla igenom tiotusentals molekyler och laboratorieexperiment för att testa de bästa kandidaterna. Målet är att hitta nya läkemedels"startpunkter" som en dag skulle kunna hjälpa läkare att selektivt förgifta cancerceller inifrån.
Ett dolt avfallssystem inne i våra celler
Varje cell bryter ständigt ner socker för att skapa energi, och denna process producerar en reaktiv avfallskemikalie kallad metylglyoxal. I normala mängder omvandlar kroppen metylglyoxal till ofarlig mjölksyra via glyoxalasesystemet, en tvåstegsprocess som är beroende av hjälpmolekylen glutation. Glyoxalase‑I är det första och mest avgörande steget i denna kedja. Cancerceller, som förbrukar socker i ett rasande tempo, är starkt beroende av glyoxalase‑I för att hålla metylglyoxal under giftiga nivåer. Om detta enzym blockeras byggs metylglyoxal upp och kan driva skadade celler mot programmerad celldöd. Det gör glyoxalase‑I till ett tilltalande mål för anticancerläkemedel som riktar in sig på en grundläggande svaghet i tumörmetabolismen.
Söker i kemiskt rymd med kisel och statistik
I stället för att testa slumpmässiga ämnen i labbet använde forskarna datorstödd läkemedelsdesign för att söka igenom en stor kommersiell samling på mer än 50 000 små molekyler. Specialiserad programvara rengjorde och standardiserade först varje molekyl, förutspådde sedan dess 3D‑form och beteende vid kroppsliknande pH. Ett snabbt virtuellt screenssteg rankade hur väl varje kandidat kunde passa in i glyoxalase‑I:s aktiva säte. Teamet tillämpade därefter enkla regler om storlek, löslighet och andra läkemedelsliknande egenskaper för att sålla bort molekyler som troligen inte fungerar i kroppen. Ett mer detaljerat dockningsprogram undersökte hur de mest lovande molekylerna kunde orientera sig inne i enzymet, särskilt hur de kan nå och gripa om zinkmetallatomen som sitter i hjärtat av glyoxalase‑I:s kemi.
Ett nytt sätt att greppa enzymets metallkärna
Tidigare försök att blockera glyoxalase‑I fokuserade på välkända kemiska grupper, såsom karboxylsyror och hydroxaminsyror, som är bra på att binda metaller men ofta lider av dålig stabilitet eller oönskade biverkningar. Denna studie upptäckte istället en annan typ av "metallgripande" enhet: en hydroxytriazolring. Bland sexton topprankade molekyler som valdes för inköp och laboratorietester framstod en bärande denna ring—kodad SPB07393SC—som den mest framstående. I virtuell dockning nådde dess hydroxytriazolgrupp ned till zinkatomen, medan dess två aromatiska ringar vecklade in sig i närliggande oljiga fickor i enzymet. Datorsimuleringar av komplexet över tiotals nanosekunder föreslog att molekylen förblev tätt bundet, med stabila avstånd, kompakt proteinform och ett bestående nätverk av vätebindningar.
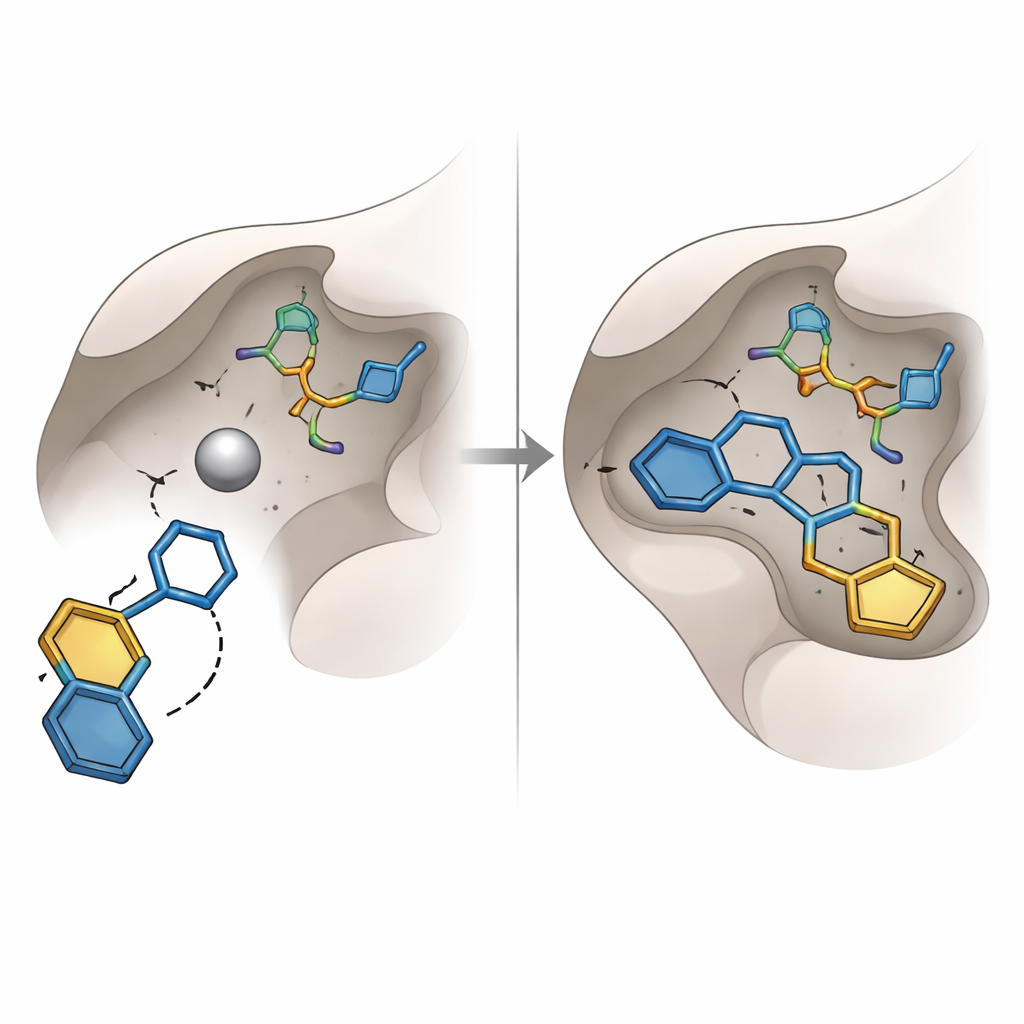
Att pröva förutsägelserna i verkligheten
För att se om datormodellerna översattes till verkliga effekter mätte teamet hur väl de utvalda molekylerna saktade ner aktiviteten hos renat mänskligt glyoxalase‑I i en plattformsbaserad analys. Femton av de sexton kandidaterna visade endast svag eller försumbar hämning under de testade förhållandena, vilket understryker fallgroparna med att förlita sig enbart på statiska dockningspoäng. I motsats hämmade SPB07393SC enzymet kraftigt, med en mitt‑mikromolär potens som gör det till ett stabilt tidigt "träff" snarare än ett färdigt läkemedel. Ytterligare programvaruverktyg förutspådde att denna molekyl bör ha acceptabel löslighet, god absorption, förmåga att nå hjärnan om så behövs, och låg sannolikhet att orsaka vissa genetiska eller leverrelaterade toxiciteter, även om dessa säkerhetsförutsägelser fortfarande kräver experimentell bekräftelse.
Vad detta betyder för framtida cancerläkemedel
Arbetet introducerar hydroxytriazol som ett nytt sätt att förankra läkemedelskandidater vid zinkatomen i glyoxalase‑I:s kärna, vilket utökar kemikernas verktygslåda för läkemedelsdesign. Medan SPB07393SC i sig endast är en utgångspunkt, gör dess kombination av enzymblockerande effekt, förutspett läkemedelslikt beteende och stabil bindning i rörelsesimuleringar det till ett lovande skelett för vidare finslipning. Mer allmänt visar studien både styrkorna och begränsningarna hos datorstyrd screening: den kan snabbt minska enorma kemiska bibliotek till ett fåtal realistiska kandidater, men noggranna laboratorieexperiment är fortfarande nödvändiga för att avslöja vilka molekyler som verkligen inaktiverar det enzym som cancerceller förlitar sig på för att hantera sitt giftiga avfall.
Citering: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
Nyckelord: glyoxalase I, cancermetabolism, datorstödd läkemedelsdesign, zinkbindande hämmare, molekylär dockning