Clear Sky Science · sv
Stimuli-responsiva chitosan‑belagda ferrit‑nanobärare för riktad capsaicinleverans och kärnberoende HepG2‑selektiv bioaktivitet
Krydda med dold kraft
Chilipeppar tillför mer än hetta till maten: dess sveda kommer från capsaicin, en naturlig förening som också kan döda cancerceller. Att använda capsaicin som läkemedel har dock visat sig svårt eftersom det löser sig dåligt i vatten, försvinner snabbt från kroppen och irriterar friska vävnader vid höga doser. Denna studie undersöker ett sätt att tygla den eldfängda molekylen genom att stoppa in den i små, smarta partiklar som kan föra capsaicin säkert genom blodomloppet och släppa ut det främst inne i levertumörer.
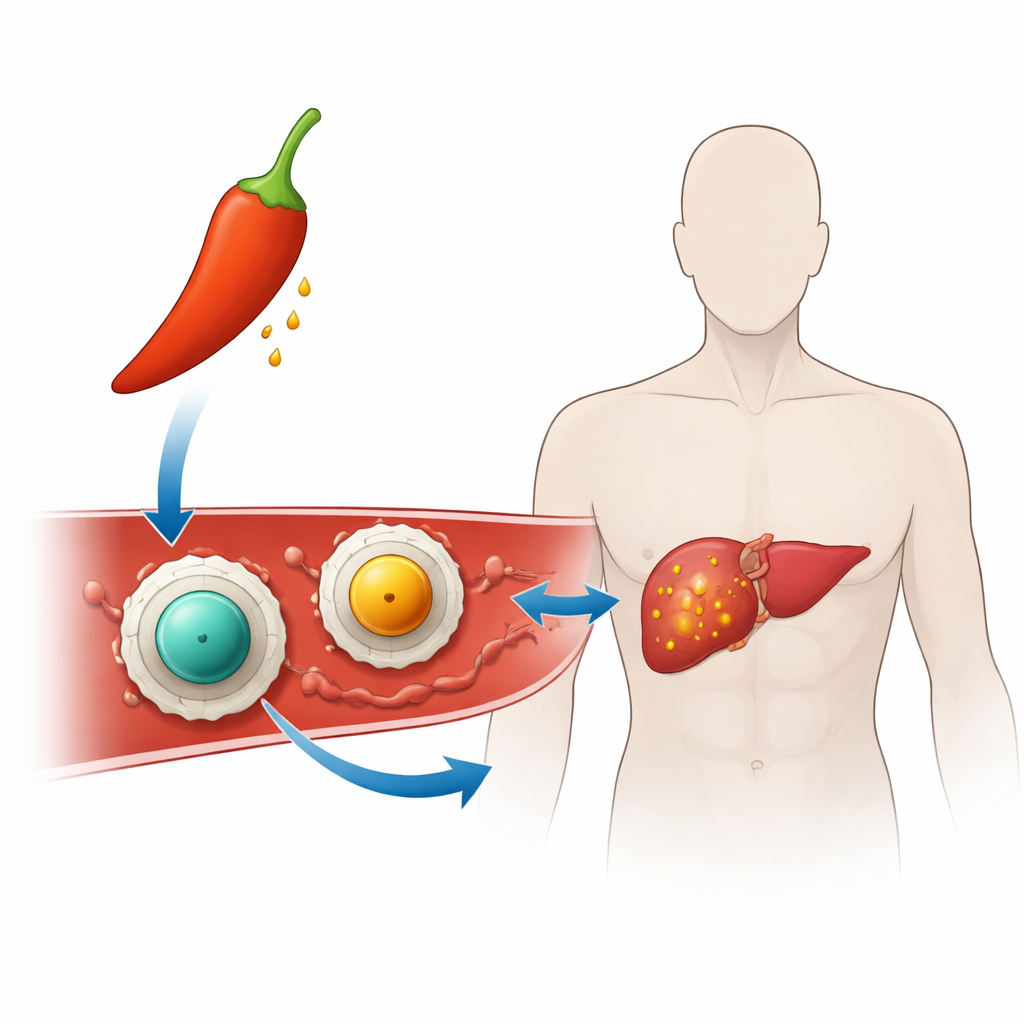
Att förvandla chili till riktad terapi
Forskarna byggde ”nanobärare” – partiklar tusentals gånger mindre än ett sandkorn – för att föra capsaicin till cancerceller. Varje nanobärare har en fast kärna av ett magnetiskt mineral kallat ferrit (antingen zinkferrit eller manganferrit) omsluten av ett tunt skikt av chitosan, ett sockerliknande ämne framställt från skaldjur som redan används i medicinska och livsmedelsprodukter. Det här skyddsskiktet gör partiklarna lättare att suspendera i vatten och hjälper dem att fästa vid cellytor och DNA, vilket är viktigt för cancerbekämpning. Genom att ladda capsaicin i detta chitosanskikt hoppades teamet hålla läkemedlet stabilt och dolt tills det når den hårda miljön inne i en tumör.
Smart frisättning i tumörmiljö
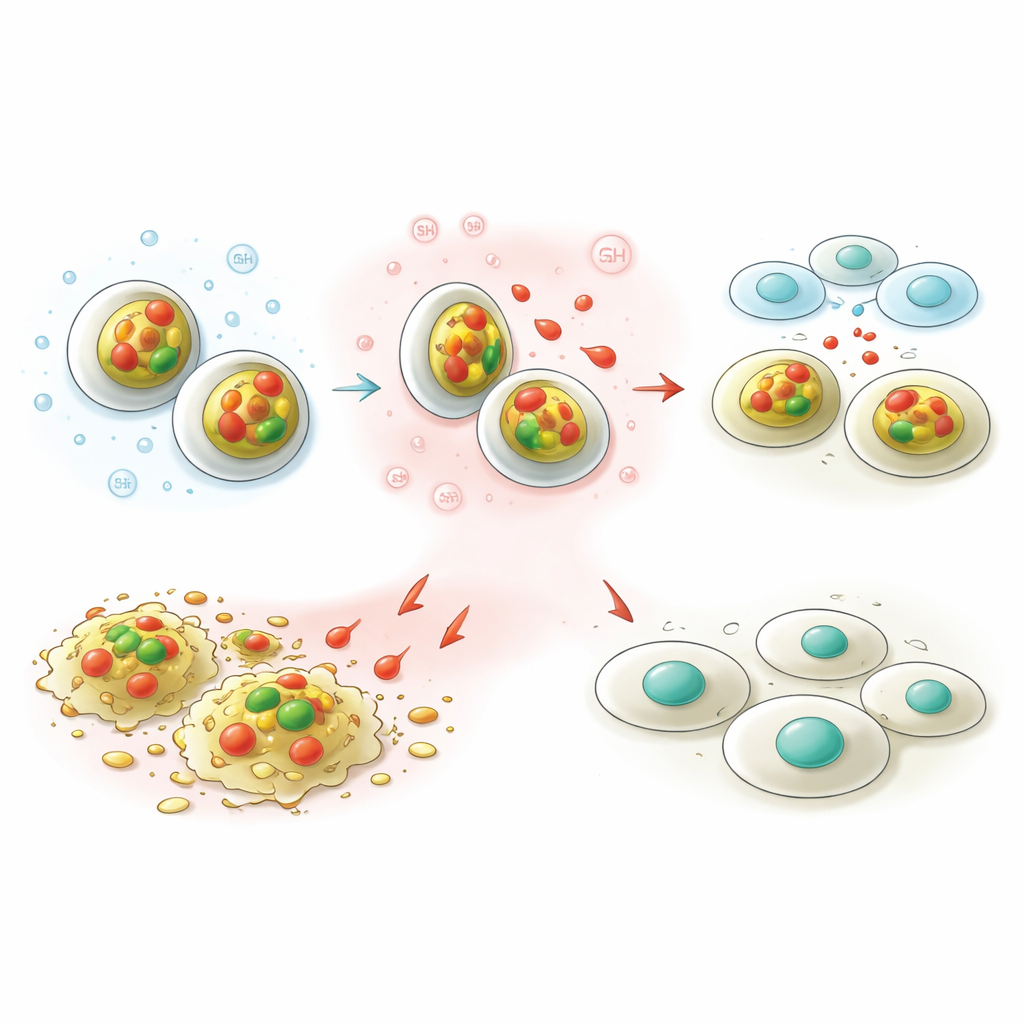
Ett kännetecken för tumörer är att de ofta är mer sura och rikare på vissa antioxidanter, som glutathion, än friska vävnader. Teamet designade sina nanobärare för att känna av dessa förhållanden. I laboratorietester vid normalt blod‑pH läckte mindre än 10 procent av det lagrade capsaicinet ut under två dagar, vilket tyder på att partiklarna skulle bära sitt last säkert under cirkulation. Under tumörlika förhållanden – mer sura och med rikligt glutathion – frigjorde partiklarna ungefär en tredjedel av sitt capsaicin. Detta ”på‑/av‑” beteende innebär att läkemedlet mer sannolikt släpps inne i cancerceller snarare än längs vägen, vilket potentiellt ökar nyttan samtidigt som biverkningar minskar.
Hur partikelingredienser påverkar säkerhet och verkan
Även om de två nanobärarna såg lika ut från håll gjorde deras inre kärnor verklig skillnad. Zinkbaserade partiklar tenderade att vara mindre och höll kvar capsaicin hårdare, medan manganbaserade partiklar var mer porösa och släppte ut läkemedlet lättare. Båda typerna hade en stark positiv ytladdning, vilket hjälper dem att interagera med cellers och DNA:s negativt laddade ytor. Tester med mänskligt blod visade mycket låg skada på röda blodkroppar, och tomma partiklar var skonsamma mot normala lungceller, vilket stödjer deras grundläggande säkerhet. När de laddades med capsaicin blev båda systemen mer potenta mot levercancerceller, men manganvarianten uppnådde den bästa balansen: den skadade cancerceller mer kraftfullt samtidigt som den var relativt snäll mot normala celler.
Utöver cancer: extra skyddande effekter
Nanobärarna gjorde mer än att leverera capsaicin. De hämmande också tillväxten av flera sjukdomsalstrande bakterier lika effektivt som ett standardantibiotikum i vissa tester, och de bidrog till att neutralisera skadliga fria radikaler som är kopplade till inflammation och vävnadsskada. Noggranna ljusbetsmätningar visade att när capsaicin packades in i ferrit‑chitosan‑partiklarna fäste det starkare och mer stabilt till DNA. Snabba kinetiska experiment avslöjade en tvåstegsprocess: DNA fäster först vid den positivt laddade partikelytan, sedan omarrangeras komplexet till en tätare, mer långvarig association. Dessa förstärkta interaktioner hjälper sannolikt till att förklara varför de laddade partiklarna visar starkare anticancer-, antibakteriella och antioxidativa effekter än capsaicin eller ferritpartiklar ensamma.
Vad detta kan innebära för patienter
Hittills kommer dessa fynd från laboratoriediskar, inte från patienter. Ändå antyder de att noggrant konstruerade nanobärare kan förvandla en kryddingrediens till ett mer precist cancerverktyg. Genom att välja rätt kärnmaterial och skal skapade forskarna små paket som håller capsaicin stabilt, för det säkert i blodet och lossar det preferentiellt under tumörlika förhållanden, särskilt i levercancerceller. Bland de testade konstruktionerna erbjöd manganbaserade partiklar den mest lovande kombinationen av riktad cancerdöd, låg skada på normala celler och extra antibakteriella och antioxidativa fördelar. Med vidare djurstudier och säkerhetsprövningar skulle sådana ”smarta” peppar‑inspirerade partiklar en dag kunna bidra till mildare, mer fokuserade behandlingar för levercancer och möjligen andra sjukdomar.
Citering: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
Nyckelord: capsaicin, levercancer, nanopartiklar, riktad läkemedelsleverans, stimuli‑responsiva bärare