Clear Sky Science · sv
MOV10, en ny immunoterapi och prognostisk biomarkör, bidrar till gliomutveckling genom att reglera autofagi
Varför denna studie om hjärncancer är viktig
Glioblastom, en aggressiv form av hjärncancer, är notoriskt svårbehandlad. De flesta patienter överlever bara några månader efter diagnos, även med operation, strålning och cytostatika. Denna studie fokuserar på en enda molekyl kallad MOV10 som är ovanligt aktiv i dessa tumörer. Genom att visa hur MOV10 hjälper cancerceller att växa, undvika immunsystemet och motstå celldöd identifierar forskarna en ny potentiell måltavla för effektivare behandlingar — och en möjlig markör för att förutse patienters prognos.
En dold medhjälpare i dödliga hjärntumörer
Teamet började med att gräva i stora offentliga cancer-databaser med genetisk och klinisk information från hundratals personer med gliom, en bred grupp hjärntumörer som inkluderar glioblastom. De fann att MOV10, ett protein involverat i hantering av RNA i cellerna, är påslaget i högre grad i gliomtissue än i normal hjärnvävnad. Patienter vars tumörer producerade mer MOV10 tenderade att leva kortare tid, och denna koppling höll i sig även efter att man tagit hänsyn till ålder, tumörgrad och viktiga genetiska egenskaper. Med hjälp av dessa faktorer byggde forskarna en matematisk modell som visar att MOV10-nivåer kan hjälpa till att förutsäga en patients överlevnadschanser, vilket tyder på att MOV10 kan fungera som en prognostisk biomarkör.
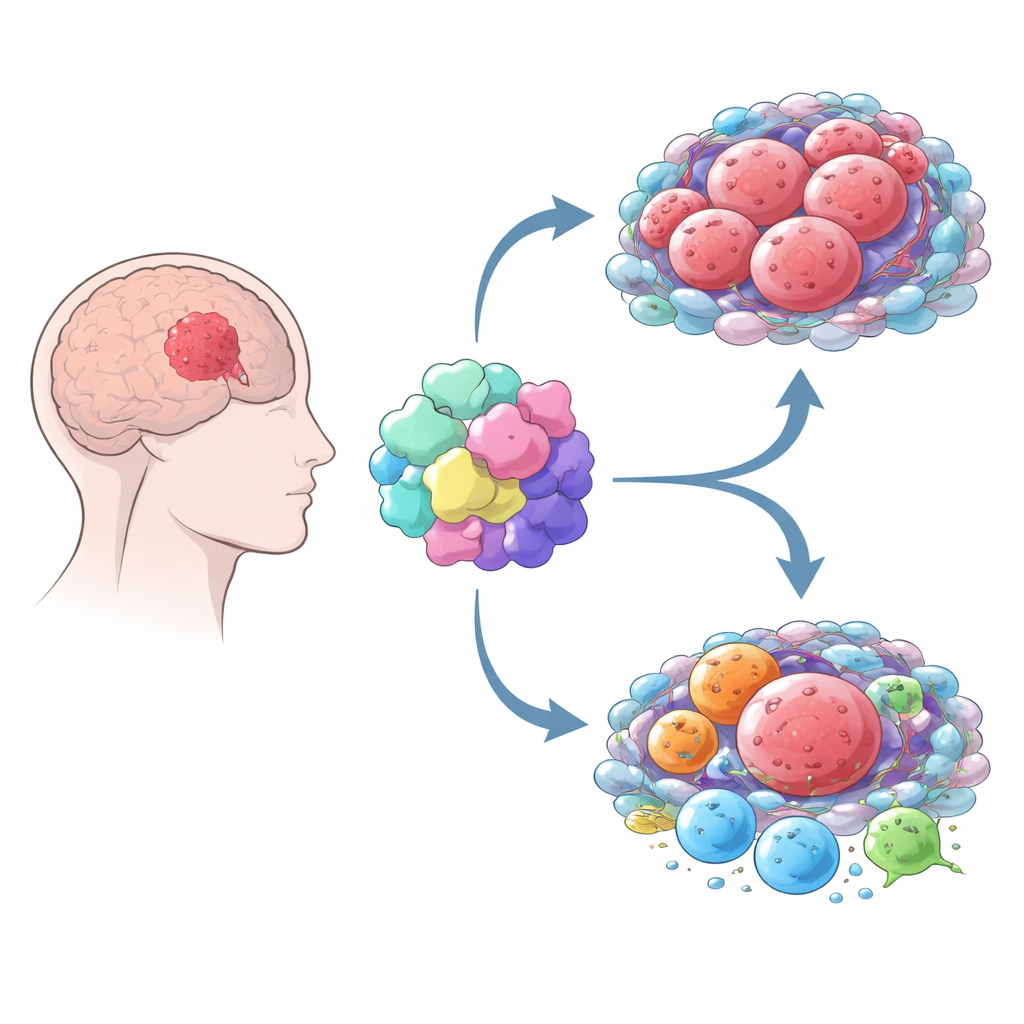
Hur MOV10 omformar tumörens omgivning
Cancer växer inte isolerat — den kapar den omgivande “grannskapet” av immunceller och stödjeceller. Genom att kombinera flera beräkningsverktyg visade författarna att gliom med höga nivåer av MOV10 omges av en rikare blandning av immunceller och stromala celler än tumörer med låg MOV10. Men detta är inte en effektiv immunattack. Istället innehåller tumörer med hög MOV10 fler makrofager, särskilt en undergrupp ofta kallad M2, som vanligtvis stödjer tumörtillväxt och dämpar immunsvar. Dessa tumörer visar också starkare tecken på uttröttade T‑celler och högre aktivitet i immunologiska ”bromsar” som är måltavlor för populära immunterapiläkemedel, såsom PD‑1 och CTLA‑4. Sammantaget tyder mönstret på att MOV10 är kopplat till en immunsuppressiv miljö där kroppens försvar är försvagade.
Från stordata till celler i labbet
För att gå bortom korrelationer undersökte forskarna MOV10 direkt i patientprover och odlade celler. De bekräftade att MOV10 är mer rikligt förekommande i gliomtissue än i normal hjärna, och att flera allmänt använda gliomcellinjer också visar höga nivåer. När de använde små interfererande RNA för att skruva ner MOV10 i gliomceller odlade i plattor delade cellerna sig långsammare, bildade färre kolonier och förlorade en del av sin förmåga att röra sig och invadera genom artificiella membran. Proteiner som driver cellcykelprogression och invasion minskade i mängd, vilket stöder idén att MOV10 aktivt främjar aggressivt beteende snarare än att vara en passiv åskådare.
Att koppla MOV10 till immunceller och självrensningsvägar
Studien undersökte också hur MOV10 samspelar med två centrala processer: beteendet hos tumörassocierade makrofager och cellens egna ”självrensnings”-system känt som autofagi. I mänskliga tumörprover återfanns MOV10 i samma regioner som M2-liknande makrofager. I ett samodlingssystem, när gliomceller konstruerades för att producera mindre MOV10, migrerade färre M2-liknande makrofager genom en barriär mot dem, vilket antyder att MOV10 i tumörceller hjälper till att lokka eller stödja dessa tumörfrämjande immunceller. Samtidigt kopplade genetiska analyser MOV10 till flera gener involverade i autofagi. Med hjälp av fluorescerande markörer som lyser upp cellulära återvinningsstrukturer visade teamet att nedreglering av MOV10 ökade autofagisk aktivitet i gliomceller och utlöste mer programmerad celldöd. Förändringar i typiska proteiner för autofagi och apoptos bekräftade dessa observationer.
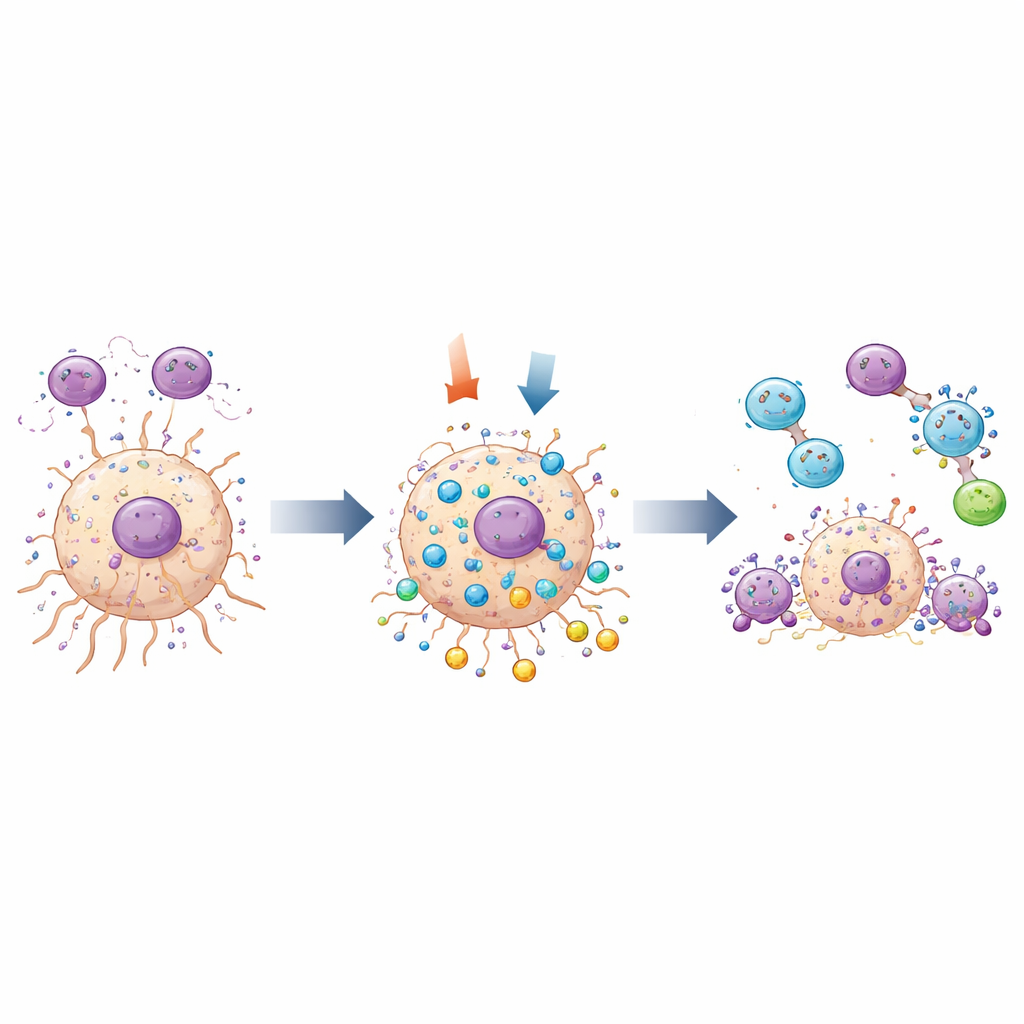
Vad detta innebär för framtida behandlingar
Sammantaget målar fynden upp MOV10 som en mångsidig allierad åt gliom: det ökar tumörcellernas tillväxt och invasion, hjälper till att bygga en immunsuppressiv mikromiljö rik på tumörstöddande makrofager och håller cellens självdestruktiva och återvinningssystem under kontroll. När MOV10 tystas växer gliomceller mindre, dör lättare och verkar mindre benägna att rekrytera skadliga immuncellstyper. För icke-specialister är huvudbudskapet att MOV10 är både en ”termometer” och en ”strömbrytare”: dess nivå i tumörer kan hjälpa förutsäga patienters utfall, och att sänka den skulle i princip kunna göra hjärntumörer mer sårbara för behandling. Medan ytterligare djurstudier och slutligen kliniska prövningar krävs framstår MOV10 nu som ett lovande mål i jakten på bättre terapier mot en av de dödligaste hjärncancerformerna.
Citering: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
Nyckelord: glioblastom, immunoterapi mot hjärntumörer, MOV10-protein, tumörmikromiljö, autofagi och apoptos