Clear Sky Science · sv
Kopparkatalyserad syntes av tiozolderivat från enaminoner, aminer och CS₂
Varför denna nya reaktion är viktig
Kemister söker ständigt snabbare och renare sätt att bygga de komplexa molekyler som driver modern medicin och elektronikmaterial. Denna studie presenterar ett förenklat recept för att framställa en familj små ringformade föreningar kallade tiozoler, som förekommer i många läkemedel och avancerade material. Genom att kombinera tre enkla ingredienser i en enda reaktionsflaska och låta en vanlig metall, koppar, styra omvandlingen visar forskarna hur man kan förvandla grundläggande byggstenar till en mängd potentiellt användbara molekyler med minimalt spill och krångel. 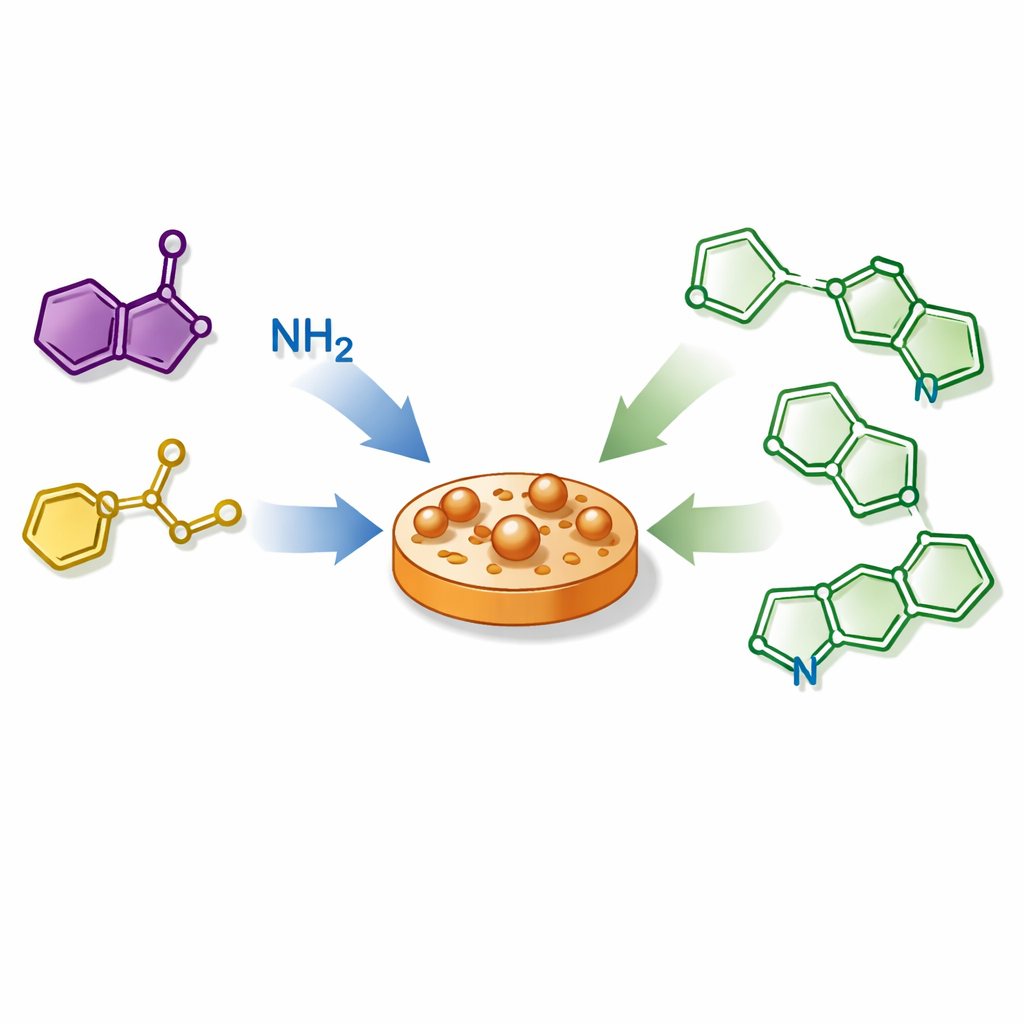
Små ringar med stor effekt
Tiozoler är kompakta ringar som innehåller både kväve- och svavelatomer. Denna lilla förändring i struktur ger dem ovanliga elektriska och biologiska egenskaper. Tiozolbaserade föreningar har undersökts som antibiotika, antiinflammatoriska medel, anticancerleadförbindelser och behandlingar för tillstånd som diabetes och neurologiska sjukdomar. Besläktade strukturer återfinns även i organisk elektronik, där de hjälper till att leda laddning i enheter som lysdioder och ledande polymerer. På grund av detta breda användningsområde är kemister angelägna om generella, pålitliga metoder för att bygga olika tiozolvarianter på begäran.
Begränsningar hos äldre syntesvägar
Traditionella metoder för att sammanfoga tiozoler börjar ofta från redan framställda svavelrika komponenter eller kräver flera separata steg, specialanpassade reagens eller hårda betingelser. Många av dessa vägar är inriktade på en underklass som kallas benzotiozoler och är mindre flexibla när det gäller att göra andra ringvarianter. Vissa angreppssätt förlitar sig också på extra tillsatser, ligander eller oxiderande medel, vilket ökar kostnaderna och genererar mer kemiskt avfall. Dessa begränsningar försvårar snabb utforskning av nya tiozolstrukturer för läkemedelsupptäckt eller materialscreening.
Enkelkopparstyrd monobehållaruppbyggnad
Författarna presenterar en annan strategi som bygger på tre lättillgängliga byggstenar: enaminoner (enkla kolbaserade fragment med inbyggd reaktivitet), vanliga aminer och koltetrasulfid, en billig vätska som här förser både svavel och kol. Under påverkan av ett kopparsalt och en basisk tillsats i en enda reaktionskärl länkar dessa ingredienser ihop sig och veckas in i den önskade tiozolringen. Processen kräver inga särskilda hjälpmolekyler och ingen tillsatt oxidant; vanlig syrgas från luften hjälper till att återställa kopparkatalysatorn. Genom systematiska tester av lösningsmedel, temperaturer, baser och metalsalter identifierar gruppen betingelser som effektivt omvandlar utgångsmaterialen till tiozoler, ofta i hög utbyte. 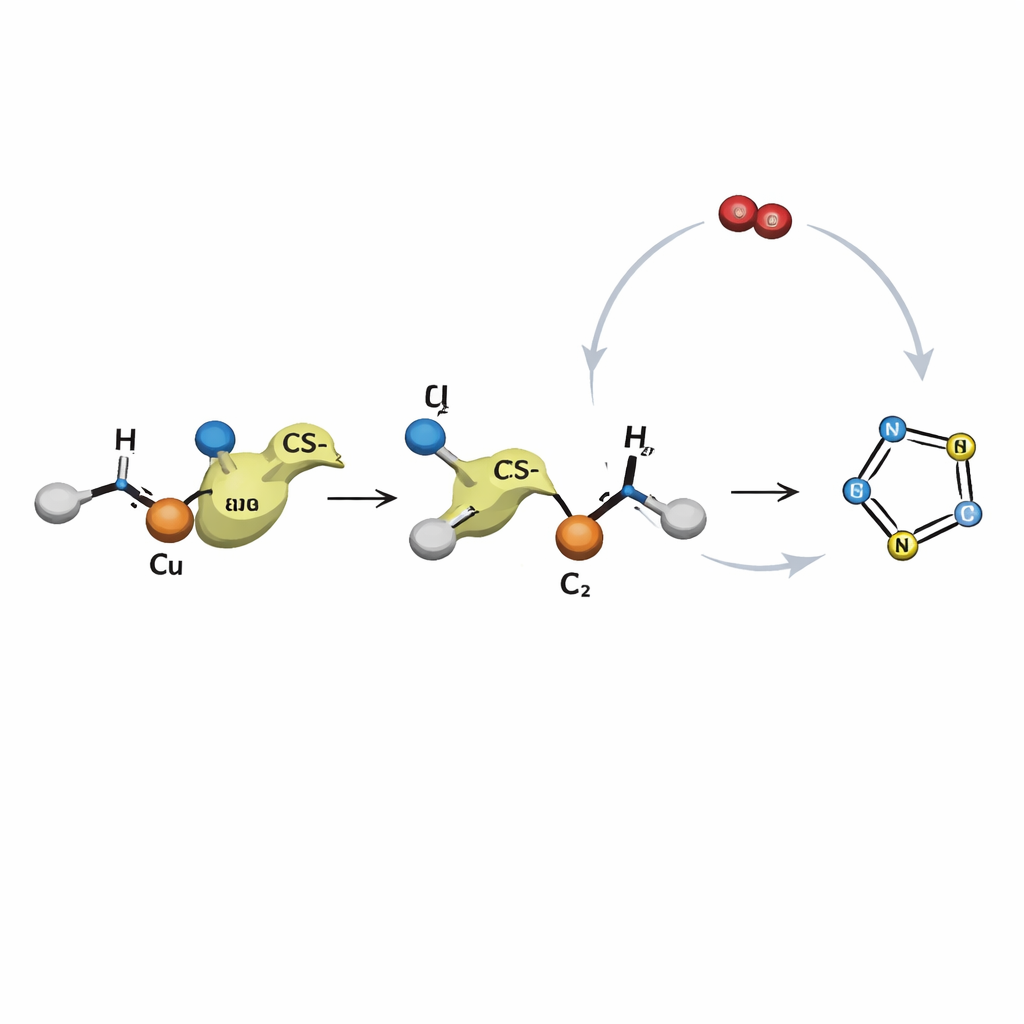
Stor variation från enkla ingångar
När betingelserna optimerats undersökte forskarna hur generell reaktionen är genom att mata in många olika aminer och enaminoner. Ett brett spektrum sekundära aminer, inklusive både flexibla kedjeformade och styva ringformade exempel, gav de önskade tiozolerna i goda till utmärkta utbyten. Primära aminer fungerade också, om än i allmänhet mindre effektivt. Reaktionen tolererade olika dekorativa grupper på aromatiska ringar, och även skrymmande "orto"-substituenter hade liten negativ effekt, vilket tyder på att trängsel nära den reaktiva platsen inte är en stor begränsning. Vissa starkt elektronacceptorer eller kväverika aminer misslyckades dock med att reagera, sannolikt eftersom de försvagade den viktiga svavelbaserade partnern som krävs för ringstängning.
Hur kopparkatalysatorn utför jobbet
För att undersöka hur denna omvandling fortskrider genomförde författarna kontrollförsök och föreslog en steg-för-steg-mekanism. Först kombinerar aminen och koltetrasulfiden sig under basiska förhållanden till ett svavelrikt fragment. Samtidigt binder enaminonen till koppar, vilket aktiverar den för reaktion. Svavel–kväve-fragmentet attackerar sedan denna aktiverade partner och formar nya kol–svavel- och kol–kväve-bindningar. Denna koppling omarrangeras till en partiell ring som sluts, varvid vätesulfid avges och den slutliga tiozolkärnan bildas. Koppar växlar mellan två oxidationssteg under sekvensen, och syre från luften hjälper till att återföra den till den aktiva formen så att katalysatorn kan användas många gånger i samma reaktionsblandning.
En okomplicerad väg till användbara molekyler
Sammanfattningsvis levererar arbetet en praktisk och flexibel metod för att framställa tiozolderivat från enkla, lättbehandlade utgångsmaterial. Eftersom reaktionen sker i en enda behållare, utan tillsatta ligander eller oxidationsmedel, förenklar den laboratoriearbetsflöden och minskar kemiskt avfall. Möjligheten att generera många olika tiozolstrukturer genom att byta ut olika aminer och enaminoner gör denna metod till ett värdefullt verktyg för kemister som designar nya läkemedel eller funktionella material baserade på detta viktiga ringsystem.
Citering: Arman, A., Nowrouzi, N. & Abbasi, M. Copper catalyzed synthesis of thiazole derivatives from enaminones, amines and CS₂. Sci Rep 16, 9184 (2026). https://doi.org/10.1038/s41598-026-40393-x
Nyckelord: tiozolsyntes, kopparkatalys, heterocyklisk kemi, enaminoner, koltetrasulfid