Clear Sky Science · sv
Alternativ splitsning och differentierad genuttryck vid förändringar i endometriets mottaglighet hos patienter med upprepade implantationsmisslyckanden
Varför vissa embryon inte implanteras
Många par som genomgår in vitro‑befruktning möter ett frustrerande mysterium: även när högkvalitativa embryon överförs kan graviditet utebli. Denna studie granskar noggrant livmoderns slemhinna — endometriet — för att förstå varför vissa kvinnor upplever upprepade misslyckade implantationer. Genom att undersöka hur gener slås på och av, hur deras budskap klipps och omordnas, och hur immunceller beter sig under det korta fönster då livmodern är redo att ta emot ett embryo, avslöjar forskningen nya molekylära ledtrådar som en dag kan vägleda mer precisa tester och behandlingar.
Livmoderns korta välkomnande fönster
Implantation kan ske endast under en kort period i varje cykel när livmoderslemhinnan blir ”mottaglig”. Forskarna jämförde vävnadsprover från 90 fertila kvinnor och 73 kvinnor med upprepade implantationsmisslyckanden, alla tagna vid tre nyckeltidpunkter: precis innan slemhinnan blir mottaglig, under det mottagliga fönstret och strax efter att det stängt. Med hjälp av höggenomströmmande RNA‑sekvensering mätte de vilka gener som var aktiva och hur deras RNA‑budskap bearbetades. Denna design gjorde det möjligt att följa hur en frisk slemhinna förbereder sig för ett embryo och hur den förberedelsen går fel hos kvinnor som upprepade gånger misslyckas att implantera trots bra embryon. 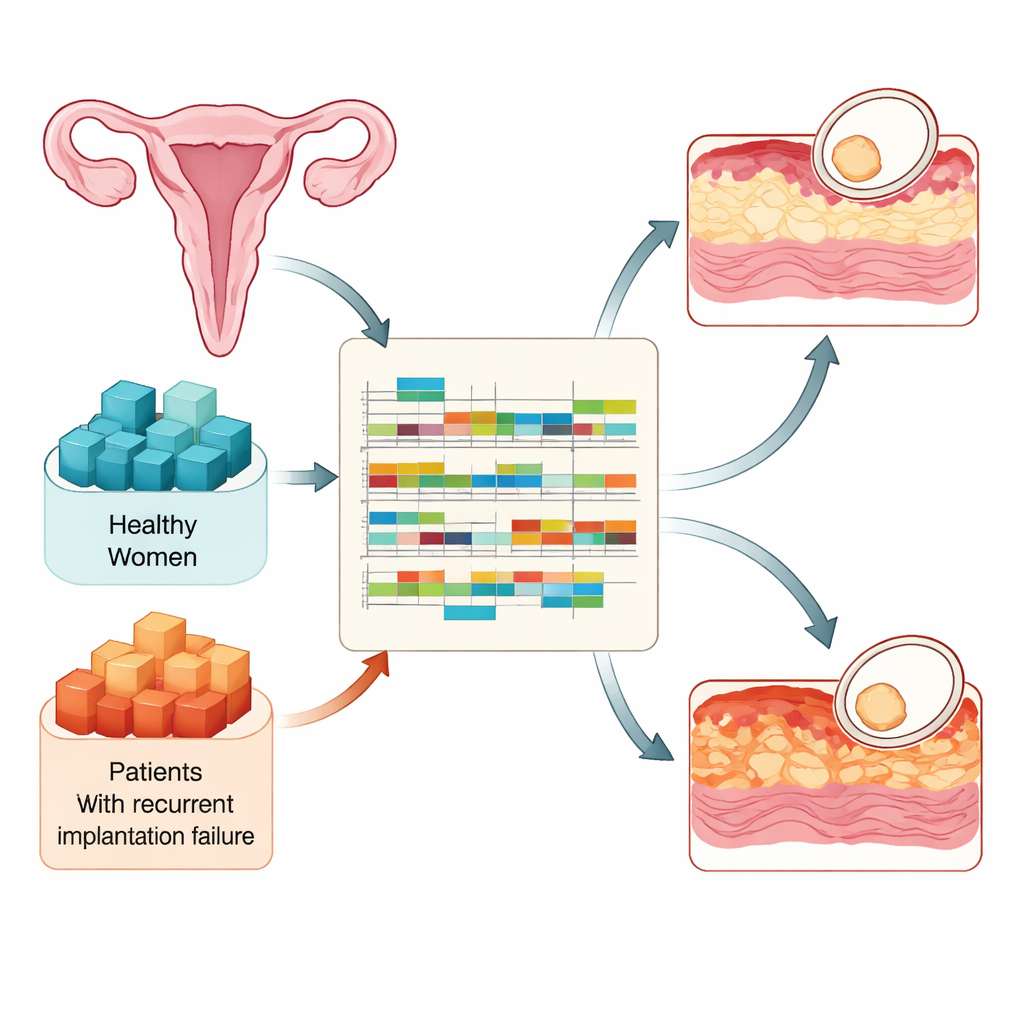
Genbudskap klippta och omordnade
Utöver att bara räkna hur mycket av varje gen som är aktiv fokuserade teamet på alternativ splitsning — processen där en enda gen kan klippas till olika budskapsvarianter och leda till skilda proteinformer. De fann över en miljon splitsningsevent i jämförelserna, med två typer — att hoppa över hela segment och att välja mellan ömsesidigt uteslutande segment — som särskilt vanliga. När de tittade enbart på förändringar som var både frekventa och statistiskt robusta såg de hundratals till tusentals förändringar i splitsningen när slemhinnan gick från icke‑mottaglig till mottaglig fas, särskilt från det tidiga (pre‑mottagliga) stadiet in i implantationsfönstret. Många av dessa förändringar skedde även när den totala mängden av genen förblev densamma, vilket betyder att proteinet ändrade form utan att total genaktivitet förändrades.
Celler som fäster, omformas och kommunicerar med immunsystemet
Gener som påverkades av förändrad splitsning och av ändringar i aktivitet var starkt involverade i hur celler fäster vid varandra, hur deras interna skelett omstruktureras och hur de skickar och tar emot immunsignaler. Dessa funktioner är avgörande när endometriet omvandlas från en enkel barriär till en yta som kan välkomna och förankra ett embryo samtidigt som blodkärl omformas. Hos både fertila kvinnor och dem med implantationsmisslyckanden kännetecknades den mottagliga fasen av kraftig ombyggnad i dessa banor, men kvinnor med upprepade misslyckanden tenderade att visa mer frekventa eller annorlunda mönstrade splitsningsförändringar. Några av de involverade generna har redan föreslagits som markörer för det ideala implantationsfönstret, vilket förstärker idén att inte bara genaktivitet utan även exakt form av deras produkter hjälper till att definiera när slemhinnan verkligen är redo.
Immunceller och en nyckelregulator för splitsning
Teamet uppskattade också vilka typer av immunceller som fanns i vävnaden utifrån samma RNA‑data. Hos kvinnor med implantationsmisslyckanden visade den mottagliga fasen färre cytotoxiska T‑celler och vilande natural killer‑celler, men fler monocyter och vissa makrofager jämfört med tidigare faser. Senare, efter att fönstret stängt, skiftade mönstren igen med förändringar i aktiverade natural killer‑celler och makrofagundergrupper. Flera av dessa förändringar i immuncellssammansättning följde tätt specifika splitsningsevent, vilket antyder att omformningen av genbudskap och immunsbalansen är kopplade. Bland proteiner som kontrollerar splitsning framträdde en kallad KHDRBS3 som en central nod kopplad till många av de ändrade eventen och som konsekvent minskade i nivå när slemhinnan blev mottaglig, både hos fertila och drabbade kvinnor. Detta tyder på att den kan bidra till att driva bytet i splitsningsmönster som följer öppningen av implantationsfönstret. 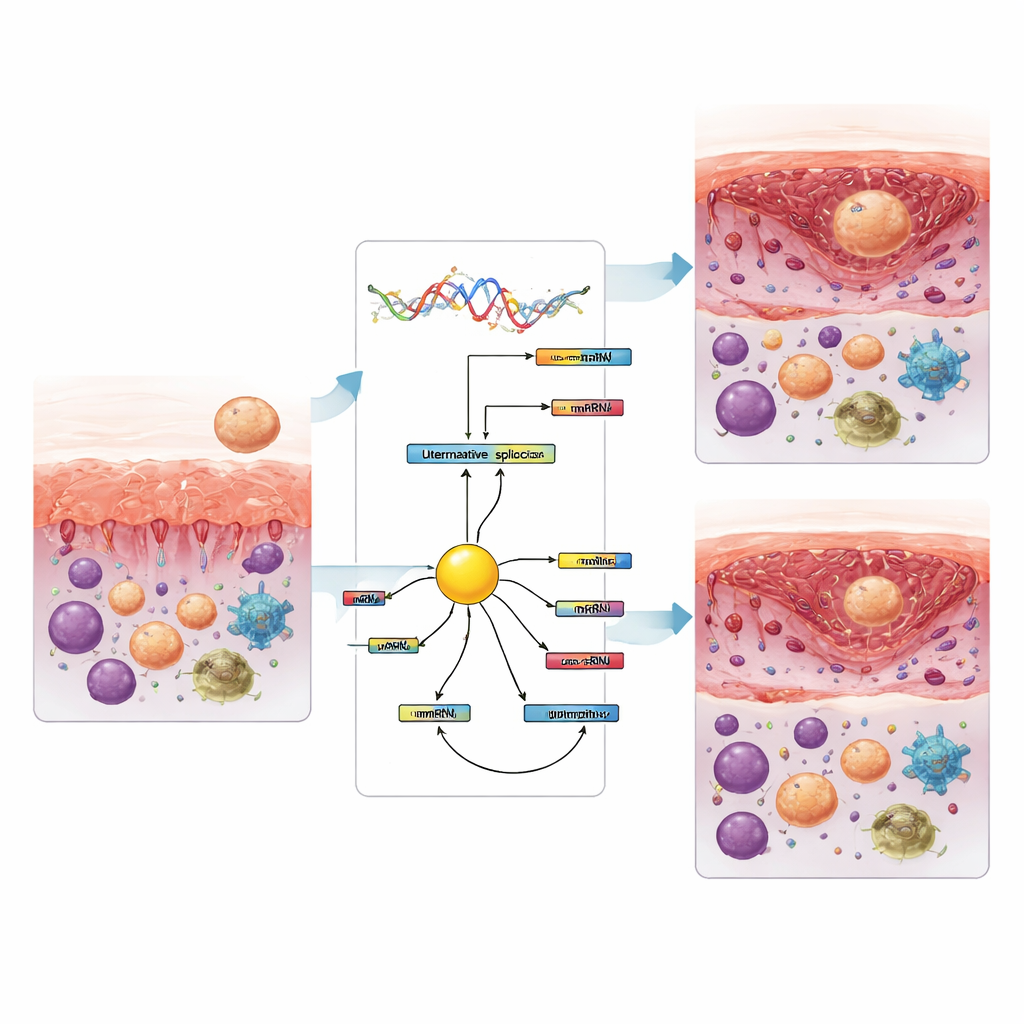
Visar vägen mot framtida tester och behandlingar
För att översätta dessa molekylära mönster till möjliga terapier undersökte forskarna om befintliga småmolekylära läkemedel skulle kunna motverka de onormala splitsningssignaturer de observerade. Genom att matcha sina genlistor mot stora läkemedelsresponsdatabaser identifierade de flera godkända eller experimentella föreningar som riktar sig mot gener kopplade till implantation, inklusive medel som påverkar immunreaktioner eller hormonrelaterade vägar. Även om dessa ligger långt ifrån redo för klinisk användning i detta sammanhang erbjuder de en startpunkt för laboratorietester.
Vad detta betyder för patienter
Sammanfattningsvis visar studien att implantationsmisslyckande inte enbart handlar om att ha ”fel” gener, utan om hur dessa gener redigeras till olika budskap och hur livmoderns immiljö finjusteras över tid. Arbetet framhäver KHDRBS3 och närstående faktorer som lovande reglatorer av denna process och avslöjar samordnade skift i immunceller som antingen kan stödja eller hindra ett embryos försök att slå sig ner. På sikt kan sådana insikter leda till mer förfinade tester som fastställer tidpunkten och kvaliteten på en kvinnas mottaglighetsfönster, samt riktade behandlingar som försiktigt justerar genbudskap eller immunsbalans för att ge embryon bättre chans att implantera.
Citering: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Nyckelord: endometriell mottaglighet, upprepade implantationsmisslyckanden, alternativ splitsning, uterina immunceller, assisterad reproduktion