Clear Sky Science · sv
Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy
Varför denna forskning är viktig
Personer med avancerade mjukdelssarkom – sällsynta cancerformer som växer i muskler, fett eller andra stödjevävnader – får ofta slut på effektiva behandlingsalternativ. Denna studie undersöker en ny tvåstegs läkemedelsstrategi som syftar till att fånga en befintlig cytostatika inne i tumören och avstänga tumörens blodförsörjning, i hopp om att förbättra sjukdomskontrollen samtidigt som biverkningarna hålls hanterbara.
En sällsynt cancer som behöver bättre alternativ
Mjukdelssarkom utgör bara omkring 1 % av vuxencancerfallen, men de är ofta aggressiva när de sprider sig eller inte kan avlägsnas kirurgiskt. Standardkemoterapi kan bromsa dem, men överlevnaden för personer med avancerad sjukdom är fortfarande låg. Trabectedin är ett av huvudläkemedlen som används när förstahandsbehandlingar misslyckas. Det verkar genom att skada cancercellernas DNA och genom att påverka cellerna i tumörens omgivning. Trots detta växer många tumörer tillbaka, vilket motiverar forskare att söka sätt att öka dess effekt utan att avsevärt öka skadan för patienterna.
En tvåstegs "fälla" för tumören
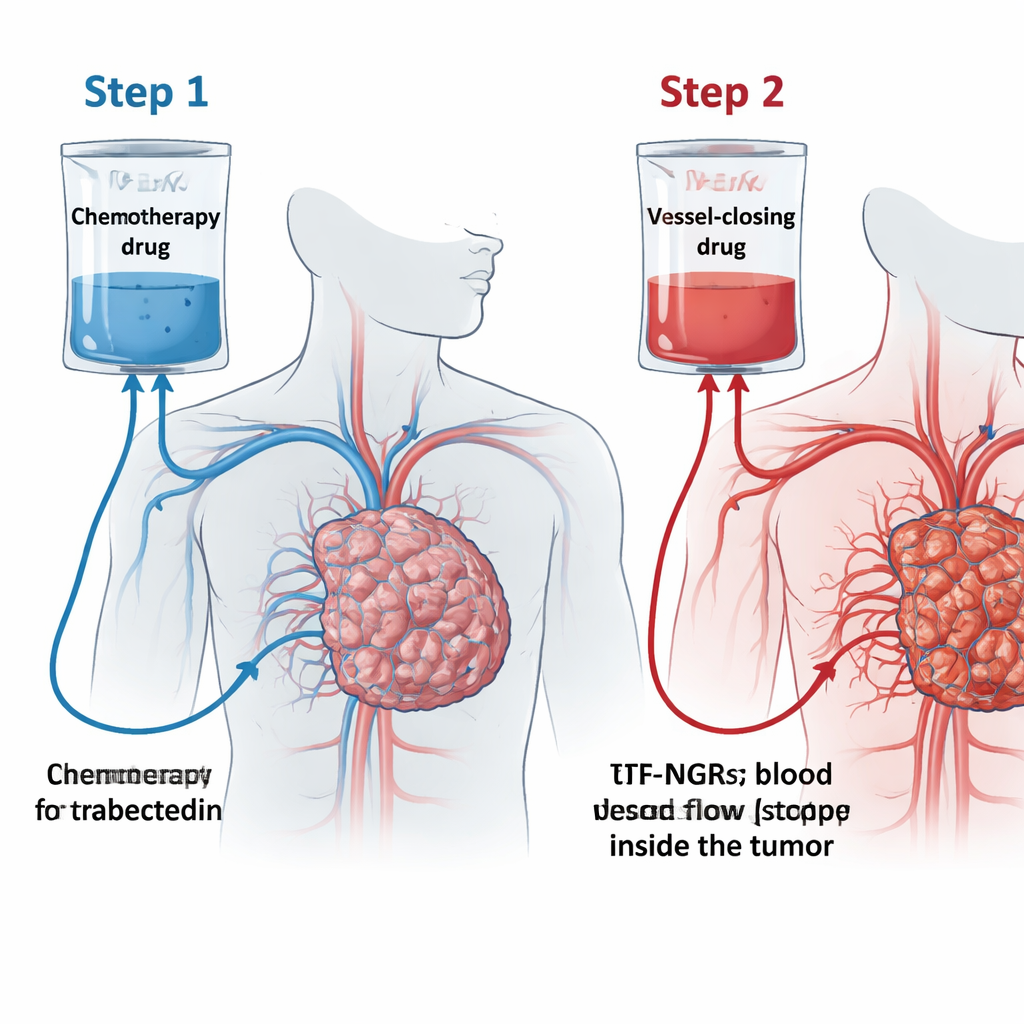
Forskargruppen testade ett koncept de kallar "trabectedinfällan" (TRABTRAP). Först får patienterna trabectedin via en 24-timmars infusion. Under de följande två eller tre dagarna får de ett andra läkemedel, tTF-NGR. Detta konstruerade protein söker upp en markör kallad CD13 som främst finns på de blodkärl som matar tumörer. När tTF-NGR binder till dessa kärl utlöser det lokal koagulation och blockerar blodflödet, vilket får delar av tumören att dö. Idén är att ge trabectedin först så att det tränger in i tumören, och sedan låsa inne det genom att tTF-NGR stänger tumörens små kärl, vilket fångar läkemedlet där det behövs mest och förstärker effekten av båda behandlingarna.
Från laboratoriet till tidig patientprövning
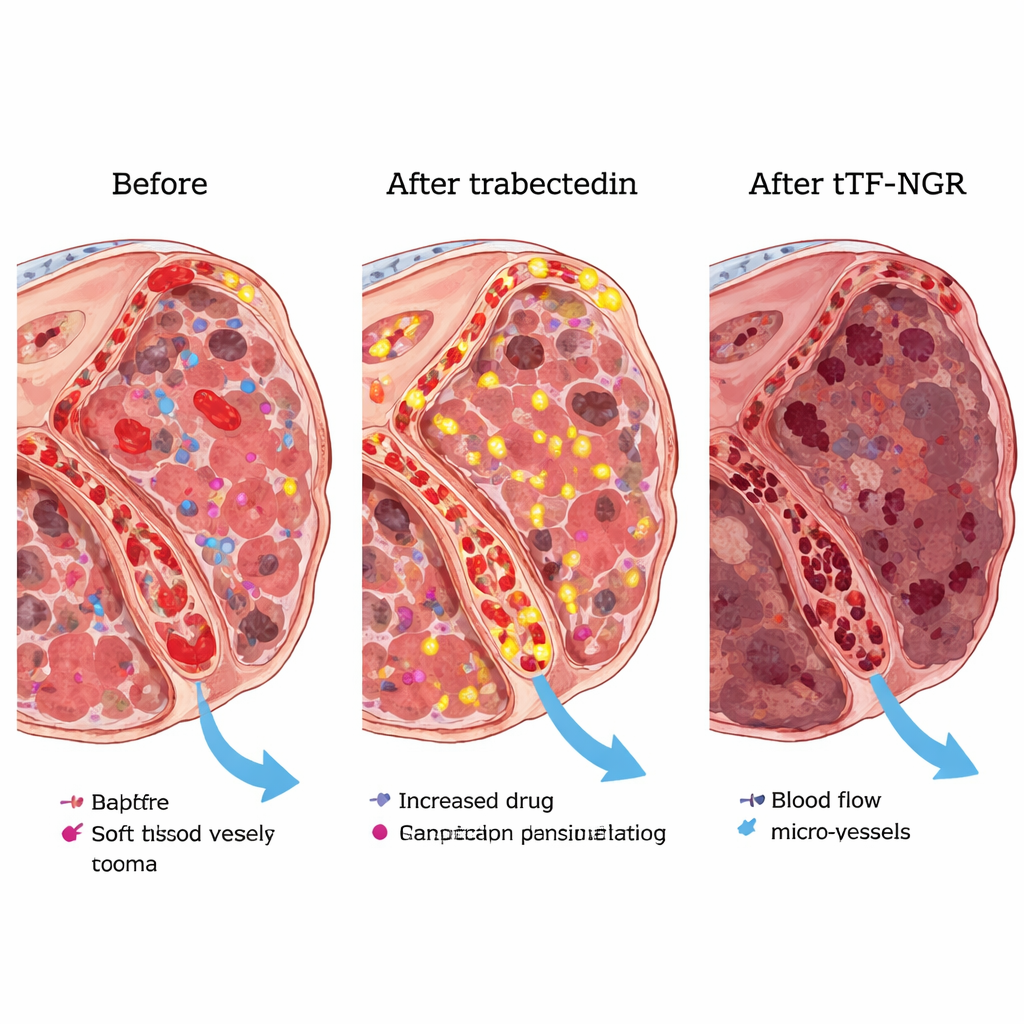
I laboratorieexperiment visade forskarna att trabectedin får blodkärlsceller och sarkomceller att uttrycka mer av en viss fettsamansättning på ytan som stödjer koagulation. Denna förändring gjorde tTF-NGR mer effektivt på att utlösa lokal blodproppsbildning på dessa celler, vilket är precis vad som behövs för att stänga ner tumörkärl. I möss med mänskliga sarkomtumörer krympte tumörerna mer när man gav trabectedin följt av tTF-NGR än vid behandlingen med något av läkemedlen ensamt. Eftersom djurtumörerna bröts ner så fullständigt under kombinationen kunde teamet inte pålitligt mäta hur mycket extra trabectedin som fångades, men den starkare tumörkontrollen stödde grundidén om "fällan".
Att hitta en säker dos hos verkliga patienter
Kärnan i denna artikel är säkerhetsfasen ("run-in") av TRABTRAP-prövningen hos 19 personer med avancerade, kraftigt förbehandlade mjukdelssarkom. Alla patienter fick standarddosen trabectedin. Det andra läkemedlet, tTF-NGR, startades på den högsta dos som tidigare tolererats när det användes ensamt, och sänktes sedan noggrant när allvarliga biverkningar uppträdde. Vid högre doser utvecklade vissa patienter betydande hjärt- eller koagulationsrelaterade problem, såsom tyst hjärtmuskelskada upptäckt via blodprover, små lungemboli eller djup ventrombos. Dessa händelser var reversibla med behandling och genom att avbryta eller reducera tTF-NGR, men de tydde på behovet av lägre doser. Vid 0,5 mg/m² tTF-NGR givet under två dagar efter trabectedin fullföljde sex patienter minst två cykler utan dosbegränsande toxiciteter, och några fortsatte upp till 14 cykler.
Tidiga tecken på nytta och hur läkemedlen samverkar
Även om denna del av studien var för liten för att bevisa effekt var resultaten uppmuntrande. Av de 19 patienterna hade de flesta åtminstone tillfällig sjukdomskontroll, och två uppvisade tydlig partiell tumörminskning. Hos personer med liposarkom eller leiomyosarkom – två vanliga sarkomsubtyper för vilka trabectedin används – hade nästan två tredjedelar stabil sjukdom eller partiella svar vid den första stora uppföljningen. Detaljerade MR-undersökningar hos en patient bekräftade att tTF-NGR vid vald dos selektivt kunde minska blodflödet inne i tumöransamlingarna. Blodprover visade att när tTF-NGR gavs efter trabectedin stannade det kvar längre i cirkulationen och verkade mer aktivt än när det användes ensamt, vilket hjälper förklara varför den säkra dosen i kombination är lägre än för monoterapi.
Vad detta betyder för patienter
För personer med avancerat mjukdelssarkom representerar TRABTRAP ett omsorgsfullt utformat försök att få mer effekt av en befintlig kemoterapi genom att kombinera den med en kärlavstängande agent som riktar sig mot tumörens egen blodförsörjning. Säkerhetsfasen visar att denna kombination, vid anpassade doser, kan ges upprepade gånger med biverkningar som är betydande men i allmänhet hanterbara och reversibla vid noggrann övervakning. Fastän det är för tidigt att säga om det kommer att förlänga livet eller konsekvent krympa tumörer, motiverar den lovande tidiga sjukdomskontrollen och de tydliga effekterna på tumörblodflödet att gå vidare till en större, randomiserad prövning. Om framtida resultat är positiva kan denna tvåstegsmetod öppna en ny väg för behandling av sarkom och kan inspirera liknande strategier för andra svårbehandlade cancerformer.
Citering: Hessling, K., Brand, C., Schwöppe, C. et al. Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy. Sci Rep 16, 7389 (2026). https://doi.org/10.1038/s41598-026-40362-4
Nyckelord: soft tissue sarcoma, trabectedin, tumor blood vessels, targeted coagulation therapy, combination chemotherapy