Clear Sky Science · sv
Adaptiv urvalsselektion för prototypbaserad förklarbar mitosdetektion i digital patologi
Varför detta är viktigt för cancervården
När patologer granskar cancersnitt i mikroskopet hjälper räkningen av hur många tumörceller som aktivt delar sig att avgöra hur aggressiv en cancer är och vilka behandlingar som bör väljas. Artificiell intelligens kan numera snabbt upptäcka dessa delande celler i digitala snitt, men dess bedömningar är ofta ett mysterium även för experter. Denna artikel introducerar en metod kallad Adaptiv Urvalsselektion (AES) som låter ett AI-system ”visa sitt arbete” genom att peka på verkliga tidigare fall som stöder eller motsäger varje beslut, vilket gör automatisk mitosdetektion mer transparent och kliniskt pålitlig.
Utmaningen att upptäcka delande celler
Delande tumörceller, så kallade mitotiska figurer, är små, sällsynta och visuellt mångformiga. Under den vanliga rosa- och lila-färgningen kan de likna ofarliga strukturer som döende celler eller vissa immunceller. Människor måste skanna enorma digitala snitt för att hitta dem, en process som är långsam, tröttande och benägen för oenighet. Moderna djupinlärningssystem kan matcha eller överträffa experters prestanda i denna uppgift, men de beter sig som svarta lådor: de ger ett poängvärde för varje misstänkt cell utan att tydligt förklara varför. Inom medicinen, där behandlingsbeslut kan förändra livet, är denna brist på tydlighet ett allvarligt hinder för att använda AI i vardaglig praxis.
Bygga en stark men ogenomskinlig detektor
Författarna tränar först ett state-of-the-art objektdetekteringsnätverk, baserat på Faster R-CNN-arkitekturen, för att hitta mitotiska figurer i en stor, divers dataset kallad MIDOG++. Dessa bilder kommer från både mänskliga och canina tumörer, över flera cancertyper och laboratorier, och inkluderar mer än elvatusen noggrant märkta delande celler. För att bevara fin detalj delas snitten i små patchar och kraftigt augmenteras för att efterlikna verkliga variationer i färgning och avbildning. Den resulterande detektorn uppnår stabil prestanda över tumörtyper, med F1-poäng upp till 0,84, vilket bekräftar att den är exakt men komplex—exakt den typ av system som behöver bättre förklarbarhet innan kliniker kan lita på det i praktiken.
Att lära AI att förklara sig med exempel
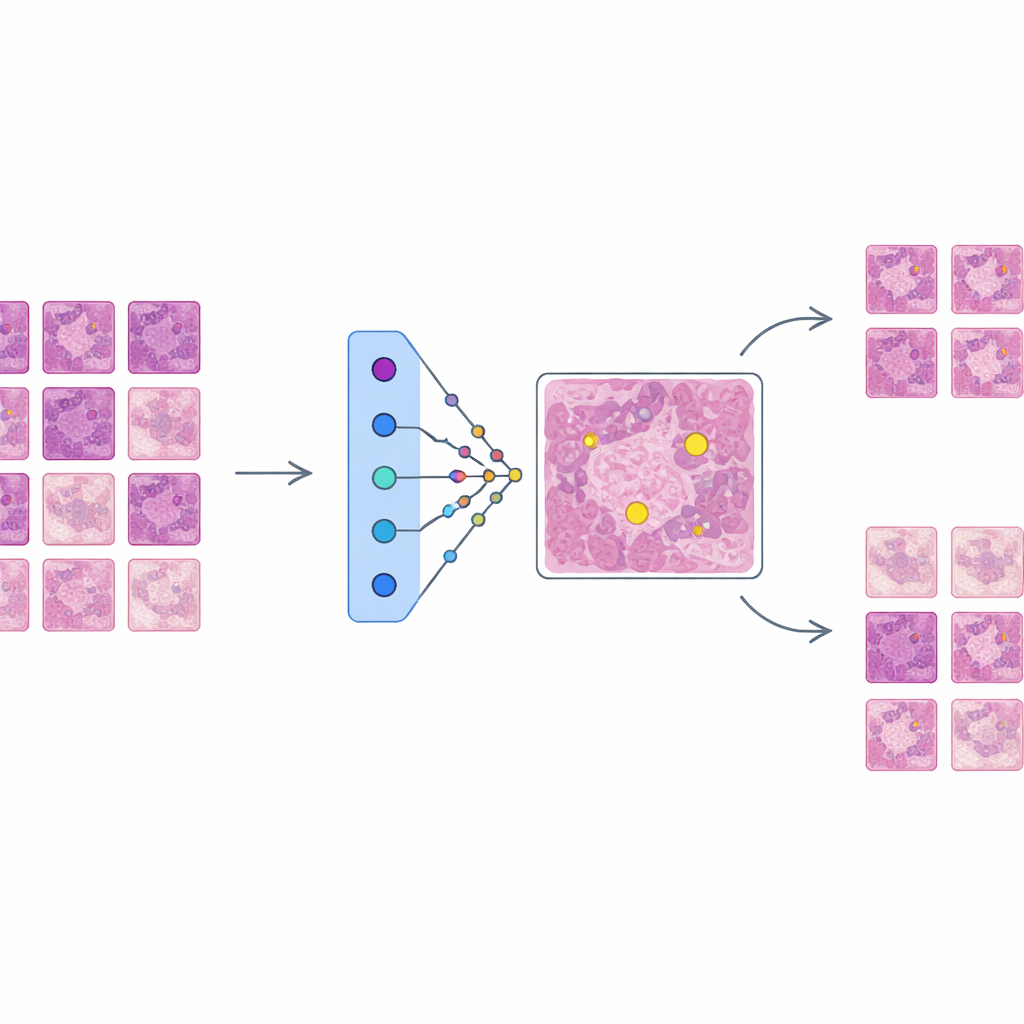
AES ligger ovanpå denna tränade detektor som ett tolkningslager snarare än att ändra hur detektorn fungerar. För varje kandidatregion som detektorn markerar som potentiellt mitotisk söker AES i ett bibliotek av verkliga vävnadspatchar tagna från träningsdata. Från detta bibliotek väljer den en liten uppsättning "stödjande" exempel som liknar verkliga mitoser och en uppsättning "motsägande" exempel som mer ser ut som icke-mitotiska celler. I bakgrunden behandlar AES detektorns förtroendesiffror som ett jämnt landskap och använder ett matematiskt verktyg kallat radiala basisfunktioner för att approximera hur det förtroendet förändras i närheten av varje fall. Endast prototyper som meningsfullt påverkar den lokala förtroendenivån behålls, så förklaringen till ett enda beslut involverar typiskt runt tio noggrant utvalda exempel snarare än hundratals knappt relevanta.
Vad exemplen avslöjar om AI-besluten
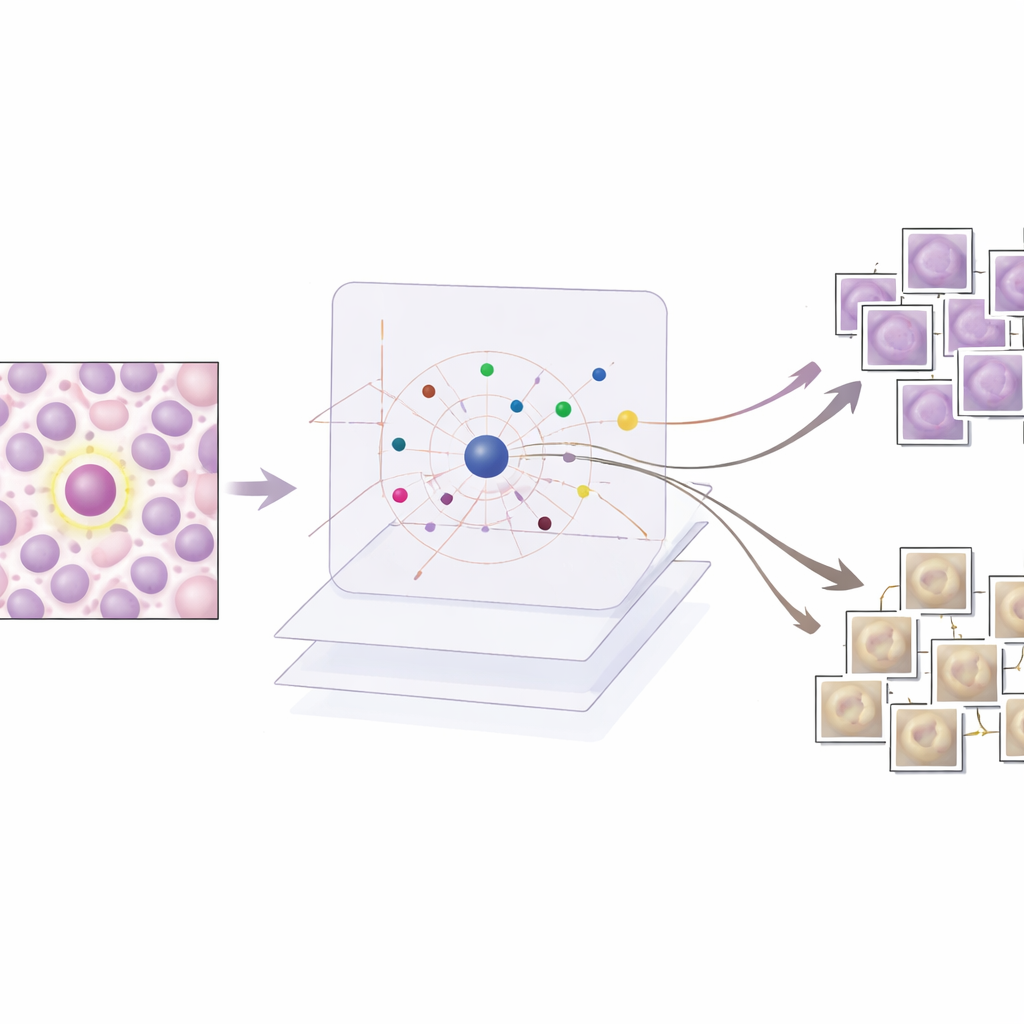
Forskarlaget utvärderar AES både kvantitativt och kvalitativt. Kvantitativt visar de att ett kompakt lexikon om cirka 190 prototypbilder kan efterlikna detektorns förtroendesiffror med mycket hög noggrannhet, samtidigt som antalet exempel som visas per fall hålls lågt nog för att en människa ska kunna granska. Kvalitativt granskar de tre vanliga scenarier. När detektorn tydligt har rätt återger AES endast mitotiska prototyper som starkt stödjer beslutet, vilket är lugnande för kliniker. Vid falsklarm lyfter metoden fram liknande mitotiska exempel som visar varför detektorn vilseleddes av liknande textur- eller kromatinmönster, ofta tillsammans med svagare icke-mitotiska prototyper som antyder osäkerhet. Vid missade mitoser tenderar AES att huvudsakligen returnera icke-mitotiska prototyper eller tvetydiga exempel, vilket pekar på blinda fläckar i träningsdata och visar var nya eller bättre märkta exempel behövs.
Från svart låda till ett samarbetande verktyg
Genom att förankra varje prediktion i en handfull verkliga, märkta vävnadspatchar får AES en komplex AI-detektor att bete sig mer som en mänsklig kollega som motiverar sina beslut genom att erinra sig tidigare fall. Systemet rapporterar inte bara om en cell sannolikt delar sig utan visar också varför och hur säkert det är, genom blandningen och påverkan av stödjande och motsägande prototyper. Denna utformning gör det möjligt för patologer att snabbt bekräfta starka prediktioner, rikta fokus mot gränsfall eller förvirrande regioner och identifiera systematiska felmönster som kan vägleda fortsatt träning. Även om metoden utvecklats för mitosdetektion kan samma angreppssätt tillämpas på andra uppgifter inom digital patologi, och hjälpa att föra AI från ogenomskinlig automatisering mot en tolkbar, fallbaserad assistent som kliniker kan ifrågasätta, lita på och förbättra.
Citering: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Nyckelord: förklarbar AI, digital patologi, mitosdetektion, prototypbaserade modeller, cancerdiagnostik