Clear Sky Science · sv
Molekylär evolution och mångfald hos norovirus RNA-beroende RNA-polymeras
Varför magbaciller ständigt överraskar oss
Norovirus är det ökända ”maginfluensa”-viruset som kan stänga ner kryssningsfartyg, skolor och sjukhus på bara några dagar. Det sprids lätt, gör hundratals miljoner människor sjuka varje år och ger ständigt upphov till nya varianter. Denna studie undersöker mekanismerna bakom den evolutionen med fokus på ett enda viralt enzym—en intern ”kopieringsmaskin” kallad RNA-polymeras—för att förstå hur det förändras över tid och hur stabilt det egentligen är. Att förstå denna dolda motor för förändring kan hjälpa förklara varför vissa norovirusstammar dominerar globalt och vägleda designen av framtida antivirala läkemedel.
Virusets inre kopieringsmaskin
Norovirus bär sitt genetiska material som RNA och är beroende av ett enzym kallat RNA-beroende RNA-polymeras för att kopiera det RNA:t inne i infekterade celler. Detta enzym, ungefär 510 byggstenar långt, liknar en hopkrupen hand med fingrar, handflata och tumme som bildar en kanal där RNA och nya byggstenar passerar. Inuti denna struktur finns sju små ”hotspots” som är nästan identiska mellan stammar; dessa regioner utför den grundläggande kemin vid kopiering av genomet. Eftersom polymeraset är avgörande för att viruset ska kunna föröka sig kan även små störningar i dessa hotspots vara katastrofala för viruset, och evolutionen tenderar därför att bevara dem mycket noggrant.
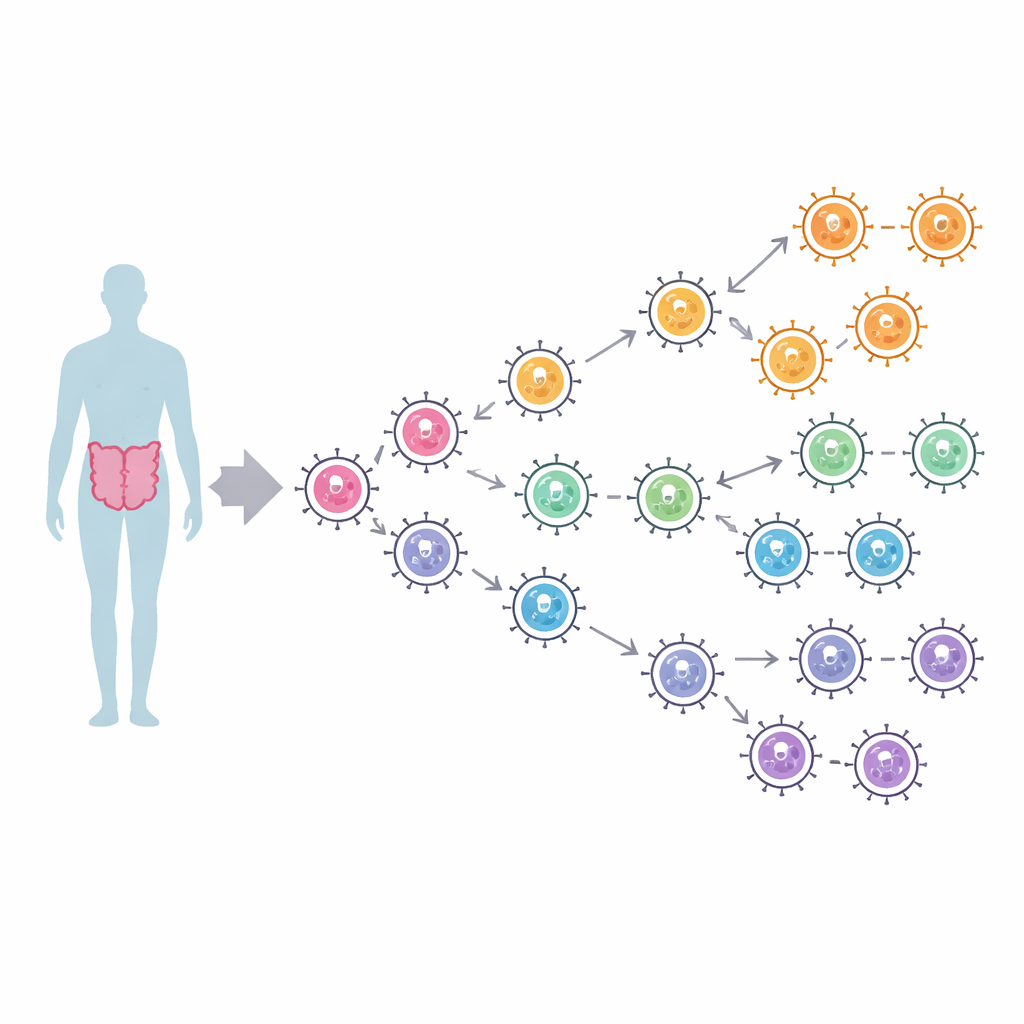
Hundratals stammar, några nyckelfamiljer
Forskarlaget samlade 1 094 kompletta polymerassekvenser från två stora mänskliga norovirusgrupper, kallade GI och GII, insamlade världen över mellan 1972 och 2024. Med hjälp av beräkningsbaserade släktträd som inkorporerar både provtagningsdatum och platser följde de hur dessa enzymer förgrenade sig över nästan fyra sekler. GI-polymeraser delade upp sig i tre huvudlinjer som sannolikt skiljdes åt redan från omkring 1600-talet, medan GII-polymeraser bildade fyra linjer, inklusive en distinkt gren för en typ känd som P16. Moderna infektioner domineras av två GII-polymerastyper, P16 och P31, båda historiskt kopplade till den långvariga pandemiska kapsidgenotypen GII.4. Trots global spridning visade träden dock liten geografisk klustring—stammar från olika kontinenter blandas—vilket tyder på att norovirus rör sig snabbt över världen utan att förbli bundet till särskilda regioner.
Långsam, stadig förändring med väl skyddade kärnor
Genom att jämföra aminosyrornas byggstenar vid varje position i polymeraset katalogiserade teamet tusentals förändringar över typerna. De fann betydligt färre förändringar i GI än i GII, vilket delvis reflekterar färre tillgängliga sekvenser, men ett tydligt mönster framträdde: de sju bevarade hotspotsen och den närliggande RNA-bindande ytan var nästan orörda. När substitutioner inträffade där var det vanligen milda byten mellan kemiskt liknande byggstenar, vilket antyder att enzymet endast tolererar mycket försiktiga justeringar i dessa avgörande zoner. De flesta frekventa förändringarna samlades i ”fingrarna” och andra yttre regioner av enzymet, bort från den centrala kemin. Vissa positioner visade till och med reversibla fram-och-tillbaka-förändringar mellan olika polymerastyper, ett tecken på konvergent evolution där orelaterade stammar oavsiktligt hittar liknande lösningar.
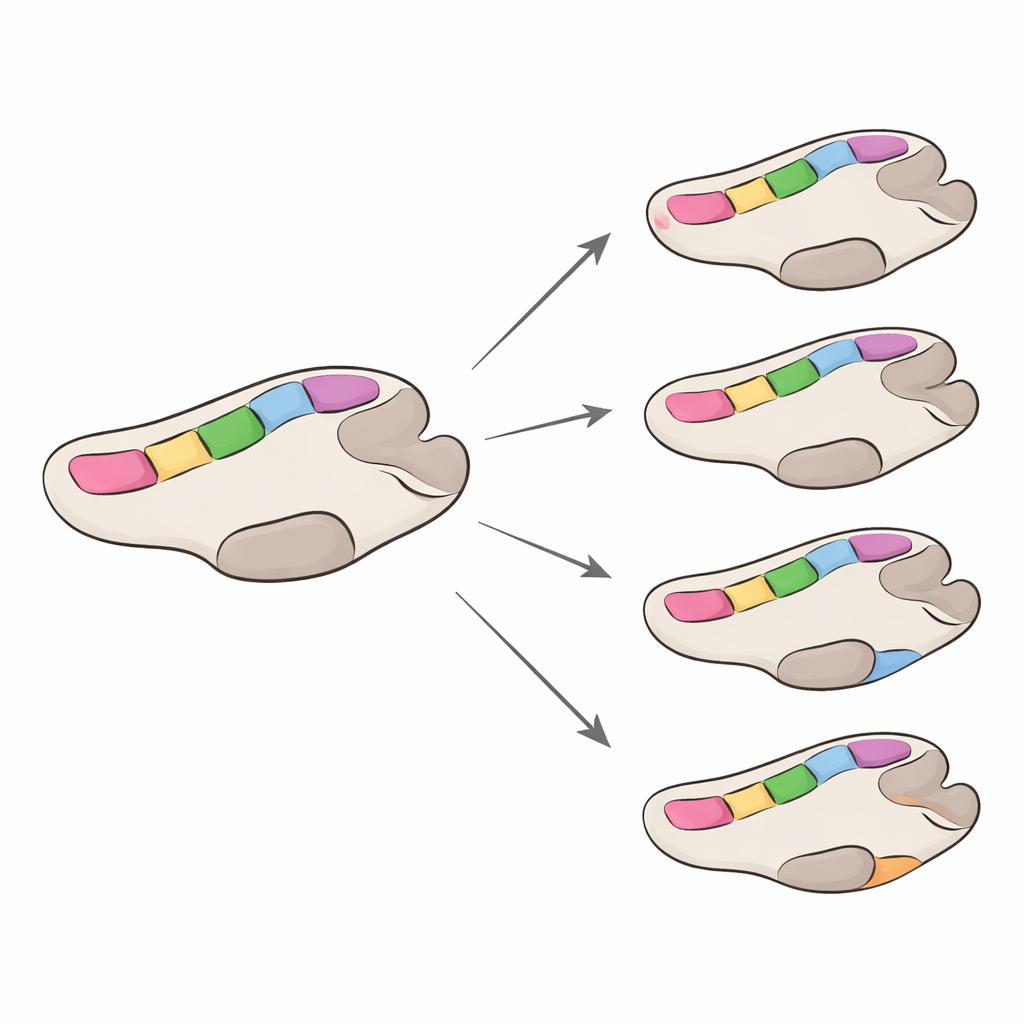
Olika hastigheter för olika virusfamiljer
Laget uppskattade sedan hur snabbt polymeraset utvecklas, med fokus på förändringar som ändrar aminosyror, eftersom dessa är mer benägna att påverka funktionen. Sammantaget förändrades GII-polymeraser cirka fyra gånger snabbare än GI-polymeraser, även om båda var långsammare än norovirus yttre skalprotein, känt för att snabbt förändras för att undkomma immunitet. Inom varje grupp utvecklades vissa polymerastyper något snabbare än andra, men skillnaderna var måttliga. Viktigt är att de flesta positioner i enzymet var under starkt "rengörande" (purifying) selektionstryck—mutationer som stör funktionen gallrades bort—medan endast ett fåtal platser visade tecken på att gynnas av positiv selektion. När dessa positivt selekterade platser kartlades på tredimensionella modeller av enzymet satt de nästan alltid utanför de mest bevarade hotspotsen, även om några låg tillräckligt nära för att potentiellt finjustera hur polymeraset binder RNA eller rör sig under kopieringen.
Vad detta betyder för framtida utbrott och behandlingar
Tillsammans målar dessa fynd upp noroviruspolymeraset som en förvånansvärt stabil kärna inramad av mer flexibla regioner som tillåter gradvis anpassning. GII-polymeraser, särskilt de som är associerade med historiskt pandemiska stammar, utvecklas något snabbare, vilket kan hjälpa dessa virus att hålla jämna steg med föränderliga värdar och konkurrerande varianter. Ändå tyder den djupa konserveringen av nyckelfunktionella regioner över århundraden på att detta enzym är en lovande stabil måltavla för antivirala läkemedel: störa den centrala kopieringsmaskineriet, och viruset har liten möjlighet att undkomma utan att försvagas själv. För icke-specialister är slutsatsen att medan norovirus yttre ytor sannolikt kommer fortsätta att skifta och göra nya utbrott oundvikliga, är den inre motorn som driver dessa förändringar både hårt begränsad och vetenskapligt hanterbar—vilket erbjuder ett stabilt sikte för framtida terapier.
Citering: Flint, A., Jawad, M. & Nasheri, N. Molecular evolution and diversity of the norovirus RNA-dependent RNA polymerase. Sci Rep 16, 9042 (2026). https://doi.org/10.1038/s41598-026-40248-5
Nyckelord: norovirus, virusets evolution, RNA-polymeras, antivirala måltavlor, molekylär epidemiologi