Clear Sky Science · sv
Bi-funktionell Caulis polygoni multiflori hämmar Staphylococcus aureus och förstärker erytromycins aktivitet in vitro
Varför en klängande ört spelar roll för seglivade infektioner
Läkemedelsresistenta ”superbakterier”, särskilt de som orsakas av Staphylococcus aureus i huden och i sår, blir allt svårare att behandla. Många patienter behöver kraftfulla sista-reserv-antibiotika som kan vara både dyra och toxiska. Denna studie undersöker om en traditionell kinesisk läkemedelsranka, Caulis Polygoni Multiflori (CPM), kan hjälpa på två sätt samtidigt: genom att direkt skada dessa bakterier och genom att göra ett vanligt antibiotikum, erytromycin, mer effektivt — även mot svåra meticillinresistenta stammar (MRSA). 
Det växande problemet med svårslagna mikrob
Staphylococcus aureus är en viktig orsak till infektioner som varierar från vardagliga bölder till livshotande lunginflammation och blodförgiftning. Dess meticillinresistenta form, MRSA, står emot många standardantibiotika och gömmer sig ofta i skyddande samhällen kallade biofilmer. I en biofilm fäster bakterier vid ytor som sårvävnad eller medicinska implantat och omsluts av en slemmig matris som blockerar läkemedel och immunceller. Det tvingar läkare att förlita sig på sista-reserv-antibiotika som vankomycin och linezolid, vilka kan ha allvarliga biverkningar och inte alltid är effektiva. Eftersom vissa MRSA-stammar till och med börjar motstå dessa läkemedel söker forskare nya strategier som antingen attackerar bakterierna på nya sätt eller försvagar deras försvar.
Att vända sig till ett traditionellt medel
CPM, känt som Shouwuteng, är den vedartade stammen av en klättrande växt som länge använts i kinesisk medicin för olika hälsobehov. Till skillnad från ett rent molekylärt antibiotikum är CPM en blandning av många naturliga föreningar som kan angripa bakterier på flera fronter. I den här studien beredde forskarna ett enkelt vattenextrakt — liknande ett starkt örtavkok — och testade det mot åtta stammar av Staphylococcus aureus, inklusive fyra MRSA-isolat från sjukhuspatienter. De mätte hur mycket CPM som krävdes för att stoppa bakteriens tillväxt och hur mycket som krävdes för att döda bakterierna helt. Över alla stammar bromsade CPM konsekvent och eliminerade först planktoniska (fritt simmande) bakterier, och dess effektivitet berodde inte på om stammen var resistent mot vanliga antibiotika.
Att blockera första fästpunkten och tidiga samhällen
Infektioner börjar ofta när bakterier fäster vid sårkomponenter som fibrin, nätverket som hjälper blodproppar att bildas. Teamet fann att CPM starkt minskade Staphylococcus aureus förmåga att binda till fibrin i en dosberoende grad: ju mer CPM, desto färre bakterier kunde fästa. CPM förändrade också hur bakterierna klumpade ihop sig. Vid lägre nivåer motverkade det lätt aggregation, men vid högre nivåer drev det bakterierna till stora, oordnade klumpar som sjönk ur vätskan. Mikroskopi visade att behandlade celler blev mindre och att deras ytor blev grövre. När forskarna undersökte biofilmbildning — steget då fästa bakterier bygger ett strukturerat, skyddande lager — visade CPM återigen stark, dosberoende hämning. Det störde tidig fästning och, vid högre koncentrationer, begränsade tillväxten av den klibbiga matrisen och mognaden av biofilmens ”mikrokolonier”. Däremot, när en mogen biofilm redan var etablerad, kunde CPM inte bryta ner den, troligen eftersom dess skrymmande naturliga föreningar hade svårt att tränga djupt in i biofilmfortet. 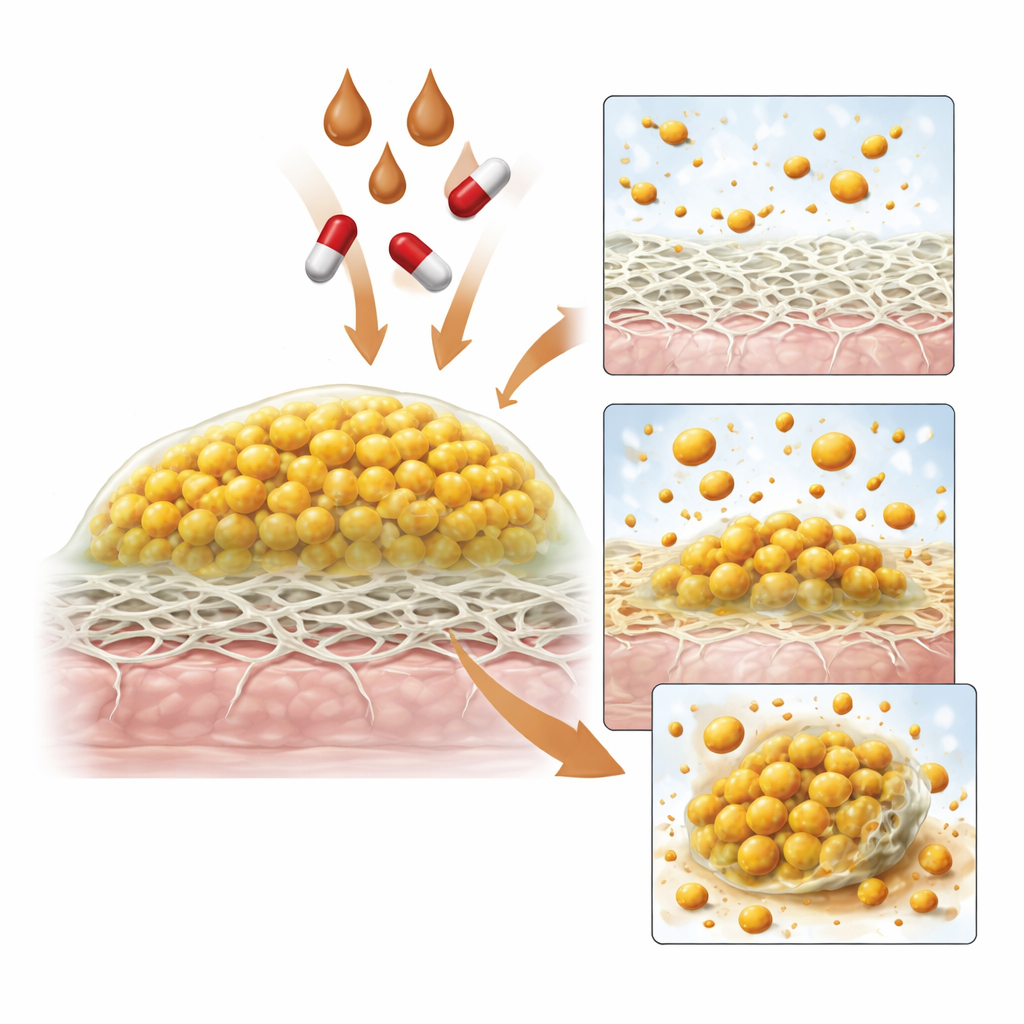
Att hjälpa ett gammalt antibiotikum att slå hårdare
Då läkare ofta kombinerar läkemedel för att överlista resistenta bakterier, undersökte forskarna om CPM kunde fungera tillsammans med standardantibiotika. I enkla platt-tester förstärkte CPM ibland zonerna där vissa antibiotika, särskilt erytromycin och penicillin, hämmade bakterietillväxt — ett tecken på synergi i vissa stammar. För att undersöka detta mer noggrant använde de en buljong-baserad ”checkerboard”-metod och blandade många olika koncentrationspar av CPM och erytromycin. I flytande kultur ökade CPM konsekvent erytromycins effektivitet mot samtliga åtta stammar. Tillsammans uppnådde de två medlen hämning och död av bakterier vid mycket lägre doser än var och en för sig, ett mönster som klassificerades som synergistiskt eller åtminstone additivt. Det tyder på att CPM kan försvaga bakteriernas försvar eller virulensfaktorer på sätt som öppnar dörren för att erytromycin återigen ska bli effektivt, även mot MRSA.
Vad detta kan innebära för patienter
För en lekman är huvudbudskapet att ett traditionellt växtextrakt, CPM, visade två värdefulla egenskaper i laboratoriet: det dödade direkt Staphylococcus aureus och det avväpnade bakterierna genom att förhindra att de fäste ordentligt och byggde skyddande biofilmer. Samtidigt gjorde det ett befintligt antibiotikum, erytromycin, mycket starkare i flytande kultur, inklusive mot resistenta MRSA-stammar. Extraktet löste inte upp etablerade biofilmer, och arbetet utfördes endast in vitro på ett begränsat antal stammar, så det är inte redo att användas som en fristående bot. Ändå framstår CPM som en lovande kandidat för framtida topiska behandlingar — såsom krämer eller förband för hud- och sårinfektioner — att användas tillsammans med konventionella antibiotika för att både angripa bakterierna och undergräva deras försvar.
Citering: Li, Z., Wang, W., Xu, W. et al. Bi-functional Caulis polygoni multiflori inhibits Staphylococcus aureus and potentiates the activity of erythromycin in vitro. Sci Rep 16, 9168 (2026). https://doi.org/10.1038/s41598-026-40228-9
Nyckelord: MRSA, biofilmer, erytromycinsynergi, traditionell kinesisk medicin, Caulis Polygoni Multiflori