Clear Sky Science · sv
Multimodal karaktärisering av flödesinducerad trombinitiering och tillväxt i extracorporeal membranoxygenation
Varför blodproppar i livsuppehållande maskiner spelar roll
Extracorporeal membranoxygenation, eller ECMO, är en form av hjärt–lungbypass som kan hålla svårt sjuka patienter vid liv medan deras organ återhämtar sig. Men att låta blodet passera genom pumpar och plaströr utsätter det för hårda mekaniska krafter som våra kroppar inte är avsedda att hantera. Dessa krafter kan utlösa farliga blodproppar inne i kretsen, vilket i sin tur ökar risken för stroke, organskada eller maskinfel. Denna studie syftade till att ta reda på hur blodflödet genom en ECMO-pump exakt formar uppkomsten och tillväxten av dessa proppar, med det långsiktiga målet att göra ECMO både säkrare och mer effektivt.
Hur ECMO håller patienter vid liv
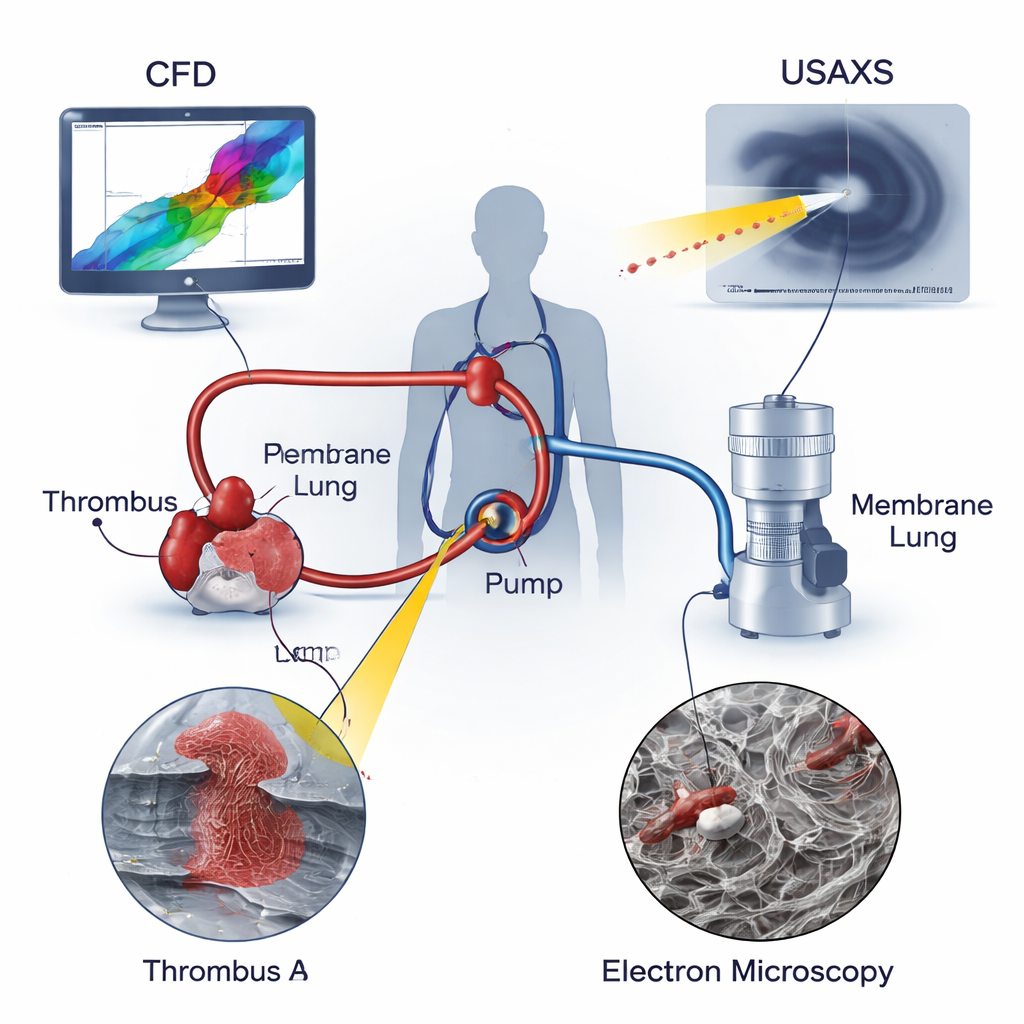
I ECMO dras blod från en större ven eller artär, drivs av en centrifugpump genom ett ”membranlung” som tillför syre och tar bort koldioxid, och återförs sedan till patienten. Till skillnad från blod som flyter jämnt genom naturliga kärl innefattar flödet i en ECMO-krets extrema förhållanden: mycket snabba strömmar, skarpa riktningsförändringar och nästan stillastående fickor där blodet dröjer kvar. Dessa miljöer är kända för att skada blodceller och stimulera koagulation. Klassiska medicinska modeller fokuserar på långsamt eller blockerat flöde i blodkärl, men de tar inte fullt ut hänsyn till den intensiva skjuvning och utdragning som blodet utsätts för inne i en snurrande pump. Författarna menar att för att verkligen förstå trombosrisk i ECMO måste man studera både de mekaniska krafterna i apparaten och den mikroskopiska strukturen hos de proppar som uppstår.
Att betrakta proppar från tre vinklar
Forskarna kombinerade tre kraftfulla verktyg för att analysera två verkliga proppar tagna från ECMO-kretsar använda hos barn: en propp vid pumpinloppet (Trombos A) och en annan i slangar strax nedströms pumpen (Trombos B). Computational fluid dynamics (CFD) simuleringar visade hur blodet rörde sig genom pumpen, kartlade områden med återcirkulerande och virvlande flöde och pekade ut var skjuv- och utdragningskrafter nådde sin topp. Ultra-small-angle X-ray scattering (USAXS) undersökte djupt inne i varje propp och mätte hur tätt packat och hur riktat fibrin-skelettet — proteinnätet som håller ihop proppar — var i hela provet. Scanning electron microscopy (SEM) gav mycket förstoringar av proppens ytor och visade formerna hos röda blodkroppar, vita blodkroppar, trombocyter och de omgivande fibrinfilamenten. Genom att överlagra dessa tre perspektiv kunde teamet koppla lokala flödesförhållanden till varje propps interna arkitektur.
En återcirkulationszon bygger en styv, riktad propp
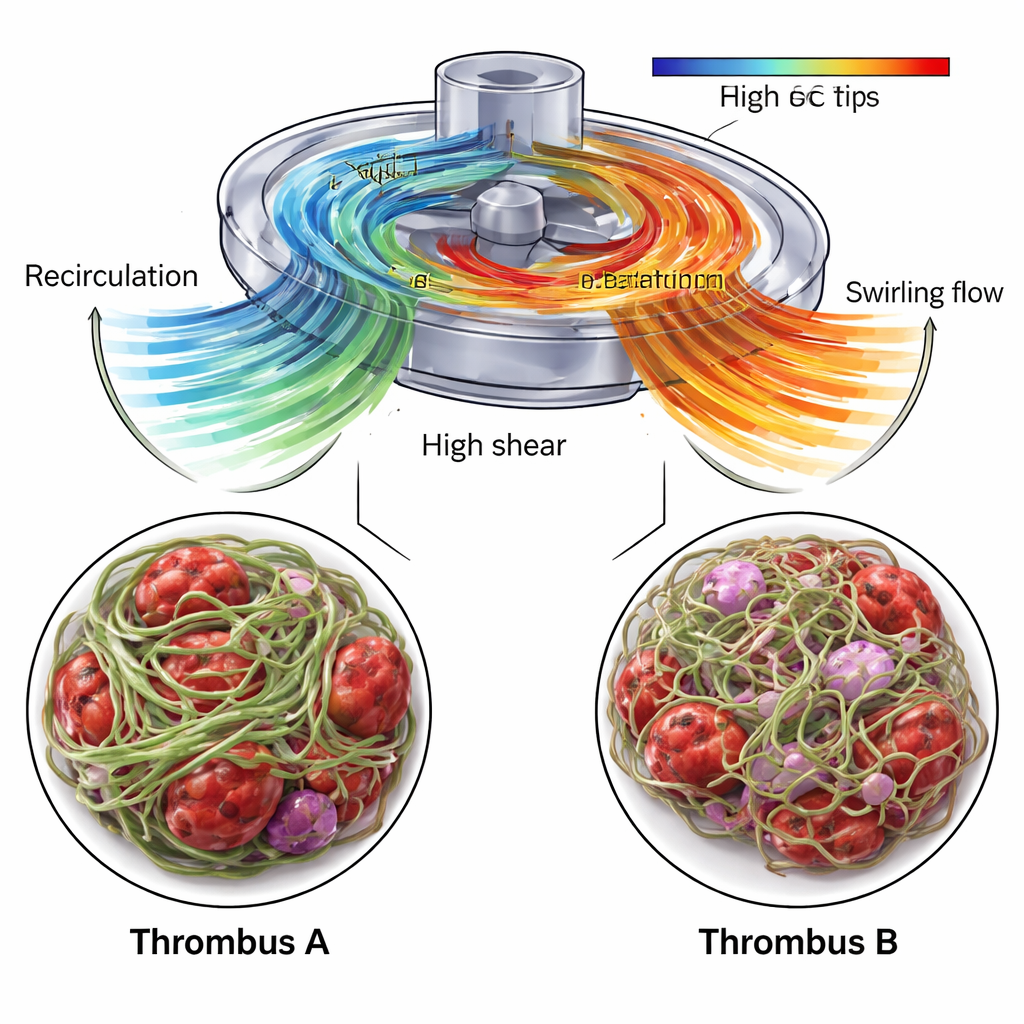
CFD visade att området nära pumpinloppet, där Trombos A bildades, innehöll en återcirkulationszon: blod pressades bakåt och upp längs höljet innan det återgick till huvudströmmen. Denna region tillät blodets beståndsdelar att dröja kvar samtidigt som de upplevde skarpa hastighetsskillnader vid gränsen mellan återcirkulerande och inkommande flöde. Inuti Trombos A indikerade USAXS en hög fibrinhalt — minst 70 procent — och en stark övergripande inriktning av fibrerna i en föredragen riktning, vilket tyder på ett tätt, styvt skelett. SEM-bilder bekräftade ett tätt vävt nät av fibrin, insprängt med abnormt formade röda blodkroppar och fragment av trombocyter. Författarna föreslår att kombinationen av långa uppehållstider och stark lokal skjuvning gynnade tillväxten av en kompakt, höggradigt ordnad propp som kunde motstå pumpens mekaniska påfrestningar.
Virvlande utflöde formar en lösare, vriden propp
Tvärtom växte Trombos B, tagen från slangar efter pumpen, i ett område dominerat av virvlande utflöde. CFD avslöjade roterande, spiral-liknande flödesstrukturer som lämnade pumpens utlopp, och USAXS-data visade ett fibrinnät som fortfarande var dominerande men mindre tätt och mindre starkt riktat i stort. Huvudriktningen för fibrinorienteringen skiftade gradvis över proppen, från en tilt vinkel till en annan, vilket speglade det vridna flödesmönstret. SEM-bilder visade fibrintrådar av varierande tjocklek och många instängda röda och vita blodkroppar, inklusive tecken på celldamaged och inflammation. Viktigt var att simuleringarna också identifierade små men betydande delar av pumpvolymen där utdragningskrafterna var tillräckligt höga för att veckla ut von Willebrand-faktor, ett nyckelblodprotein som blir klibbigt under påfrestning och snabbt kan rekrytera trombocyter. Dessa zoner koncentrerades nära impellerbladen och utloppet, vilket gör dem troliga platser för de initiala aktiveringshändelser som ledde till Trombos B.
Mot säkrare livsuppehållande maskiner
Genom att sammanfoga detaljerade simuleringar av blodflöde med röntgen- och elektronmikroskopmätningar av verkliga ECMO-proppar visar detta arbete att en propps interna ”korn” och densitet speglar den mekaniska miljö där den bildades. Återcirkulerande flöde nära pumpinloppet kopplades till ett tätt, starkt riktat fibrinskelett, medan virvlande utflöde associerades med ett mer vridet, öppet nätverk som ändå fångade många blod- och immunceller. Dessa insikter belyser specifika regioner i ECMO-pumpar och slangar där konstruktionsändringar eller målinriktade justeringar av antikoagulation troligen kan minska trombosrisken mest effektivt. På längre sikt kan sådan multiskalig kartläggning — från pumpgeometri och flödesmönster ner till proteinarrangemang — vägleda säkrare enhetsdesigner och hjälpa kliniker att bättre balansera de dubbla farorna blödning och trombos under livräddande ECMO-stöd.
Citering: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Nyckelord: ECMO, blodkoagulering, skjuvspänning, centrifugalt blodpump, fibrinstruktur