Clear Sky Science · sv
Maskininlärningsstyrd transkriptomisk integration identifierar GFM1 som en laktatyleringsrelaterad kandidatbiomarkör vid aortadissektion
Varför detta dolda hot i aortan spelar roll
Aortadissektion är ett medicinskt nödläge där ett sprickbildat skikt i kroppens största artär kan orsaka livshotande inre blödningar inom timmar. Läkare kan ofta rädda patienter med brådskande kirurgi, men det finns fortfarande inga tillförlitliga blodtester som varnar i ett tidigt skede eller läkemedel som bromsar sjukdomen i sig. Denna studie undersöker om subtila förändringar i hur artärcellernas energi- och kemiska signalering sköts kan avslöja nya varningssignaler, med fokus på en relativt okänd gen kallad GFM1 som kan koppla cellmetabolism till försvagning av aortaväggen.
Avkoda mekanismerna bakom en farlig spricka
Vid aortadissektion tränger blod in i aortaväggen och delar dess lager åt. Varför vissa människors aortor brister på detta sätt är fortfarande inte helt klarlagt. Författarna studerade mönster av genaktivitet i prover från personer med aortadissektion och från individer med friska aortor. De ägnade särskild uppmärksamhet åt gener kopplade till ”laktatylering”, en nyligen upptäckt mekanism där celler använder laktat — bättre känt som ämnet som ansamlas i muskler vid hård träning — för att finjustera proteiner och genreglering. Eftersom laktatylering har kopplats till inflammation och vävnadsombyggnad misstänkte teamet att laktatrelaterade gener också kan vara inblandade i skador på aortaväggen.
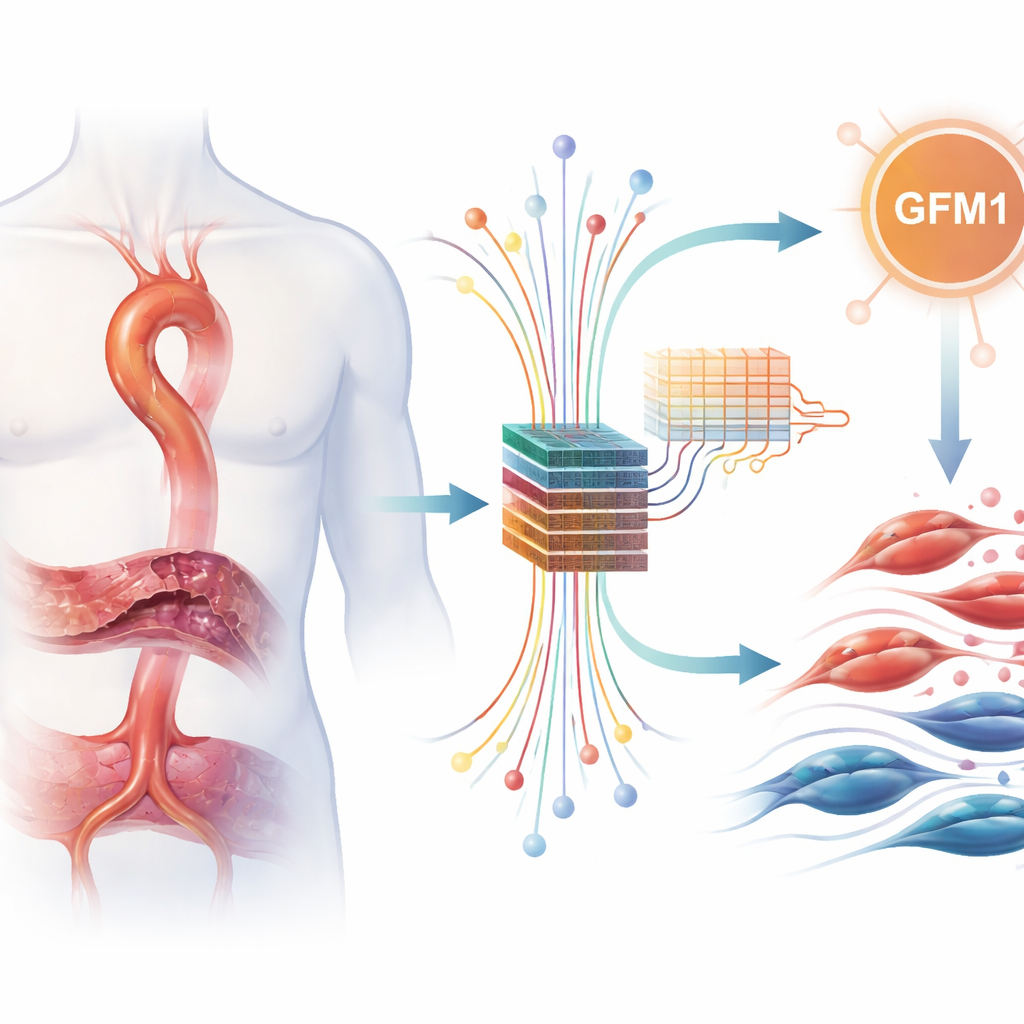
Bryta ner stora datamängder med smarta algoritmer
För att pröva idén sammanförde forskarna flera offentligt tillgängliga dataset som registrerar vilka gener som är upp- eller nedreglerade i aortavävnad. De korrigerade noggrant för tekniska skillnader mellan studierna och sökte sedan efter gener vars aktivitet konsekvent skilde sig mellan sjuka och friska prover. Av tusentals gener fann de 217 med tydliga förändringar, många av dem pekade mot immunreaktioner och ombyggnad av det vävnadsstödjande skelettet i aortan. Därefter fokuserade de på en kurerad lista med gener relaterade till laktathantering och laktatylering och identifierade 11 som både var förändrade vid aortadissektion och ingick i dessa laktatkopplade program.
Låta maskinerna rösta fram en huvudmisstänkt
Att hitta 11 intressanta gener var fortfarande för många för djupare laboratoriestudier, så teamet vände sig till maskininlärningsmetoder som ett objektivt ”röstningssystem”. De matade in data för dessa gener i tre olika modeller — LASSO, Random Forest och XGBoost — som ofta används för att plocka ut mönster som bäst skiljer patienter från kontroller. Varje metod framhöll sina favoriter, men endast en gen, GFM1, valdes starkt och konsekvent av alla tre. Denna korsvalideringsstrategi fick GFM1 att framträda som en särskilt robust kandidatmarkör, även om modellerna användes för rangordning snarare än för att bygga ett färdigt diagnostiskt test.
Zooma in på artärens muskelceller
GFM1 hjälper till att kontrollera hur mitokondrierna, cellernas energifabriker, bygger sina egna proteiner. Eftersom energibalans är avgörande för hur cellerna i artärväggen beter sig undersökte författarna GFM1 närmare. De bekräftade att GFM1-nivåerna var högre i vävnad från patienter med aortadissektion än i icke-sjuka aortor. Därefter gick de vidare till ett kontrollerat cellodlingssystem med musceller från vaskulära glatta muskelceller — de muskel-liknande celler som ger aortan dess styrka. När dessa celler stimulerades med angiotensin II, ett hormon kopplat till högt blodtryck och kärlstress, blev de mer benägna att dela sig och migrera, vilket efterliknar skadliga förändringar som ses i sjuka artärer. När forskarna använde små interfererande RNA för att sänka GFM1 i dessa celler minskade angiotensin‑driven tillväxt och migration märkbart, vilket tyder på att GFM1 bidrar till att främja dessa riskfyllda beteenden.
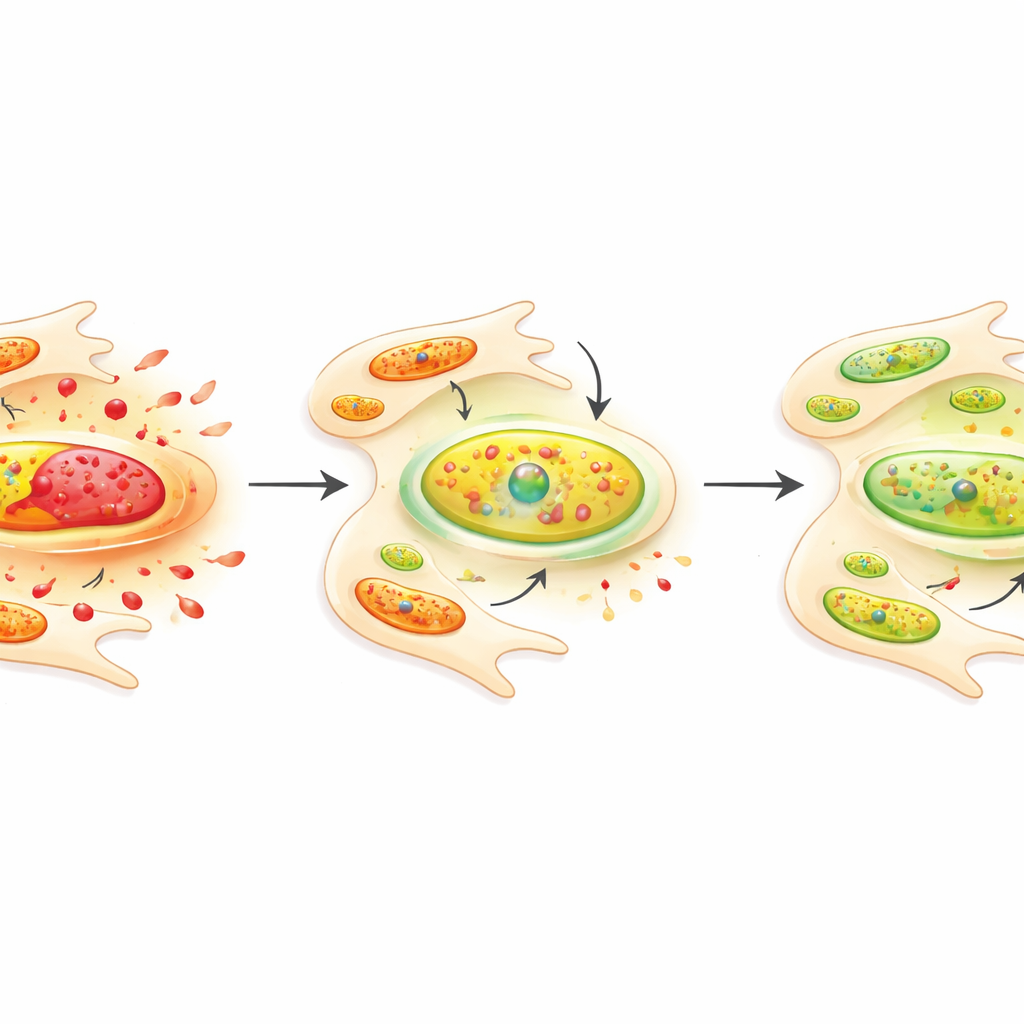
Vad detta innebär — och vad det ännu inte bevisar
Tillsammans tyder fynden på att GFM1 kan fungera som en brygga mellan förändrad cellmetabolism och det aggressiva beteendet hos artärväggens celler vid aortadissektion. Enkelt uttryckt verkar högre GFM1-aktivitet gå hand i hand med en mer instabil, skadekänslig aorta, och att dämpa den i labbodlade celler gör dem mindre benägna att överväxa och migrera. Författarna betonar emellertid att arbetet fortfarande befinner sig i ett tidigt, hypotesbyggande stadium. De mätte inte laktatylering direkt i vävnaderna och bevisade inte att GFM1 själv är kemiskt modifierad på det sättet, och modellernas prediktiva förmåga har inte testats i oberoende patientgrupper. Framtida studier måste bekräfta dessa resultat i större kohorter och utforska exakt hur GFM1 och relaterade metaboliska förändringar försvagar aortaväggen. Om dessa ansträngningar lyckas skulle GFM1 eller dess signalkedjor i framtiden kunna bli mål för nya blodtester eller behandlingar som syftar till att förebygga denna ofta dödliga spricka innan den inträffar.
Citering: Chen, J., Jiang, N., Guo, Z. et al. Machine-learning–guided transcriptomic integration identifies GFM1 as a lactylation-related candidate biomarker in aortic dissection. Sci Rep 16, 9033 (2026). https://doi.org/10.1038/s41598-026-40139-9
Nyckelord: aortadissektion, vaskulära glatta muskelceller, laktatmetabolism, mitokondriell funktion, biomarkörupptäckt