Clear Sky Science · sv
Ciprofol dämpar cerebral ischemia–reperfusion‑skada hos råttor genom att hämma ferroptos via uppreglering av AMPK
Varför det är viktigt att skydda hjärnan efter stroke
När en person drabbas av ischemisk stroke tävlar läkare mot klockan för att öppna det blockerade blodkärlet och återställa blodflödet till hjärnan. Paradoxalt nog kan detta livräddande ingrepp i sig orsaka ytterligare skada, ett fenomen som kallas reperfusionsskada. Hjärnan, plötsligt överspolad av syre och näring efter en period av brist, sätter igång en kaskad av kemiska reaktioner som kan döda sårbara nervceller. Den här studien undersöker om ciprofol, ett nytt anestetikum som redan används för sedering, också kan fungera som ett skydd för hjärnan under detta kritiska fönster genom att dämpa några av de mest skadliga processerna som utlöses när blodet återvänder.
Från blockerat blodflöde till hjärnskada
För att efterlikna vad som händer vid en mänsklig stroke blockerade forskarna tillfälligt en större hjärnartär hos råttor och återställde sedan blodflödet, vilket skapade det som kallas cerebral ischemia–reperfusionsskada. Vissa råttor genomgick enbart ingreppet, medan andra fick ciprofol kort efter att blodflödet återupptagits. Forskarna bedömde därefter hur väl djuren kunde röra sig och reagera på beröring, och undersökte deras hjärnor för områden med död vävnad och strukturella skador i nervceller. Råttor som fick ciprofol hade mindre hjärnskadeområden, nervceller med friskare utseende och bättre rörelse‑ och sensoriska poäng än obehandlade djur, vilket tyder på att läkemedlet dämpade de värsta följderna av insulten.
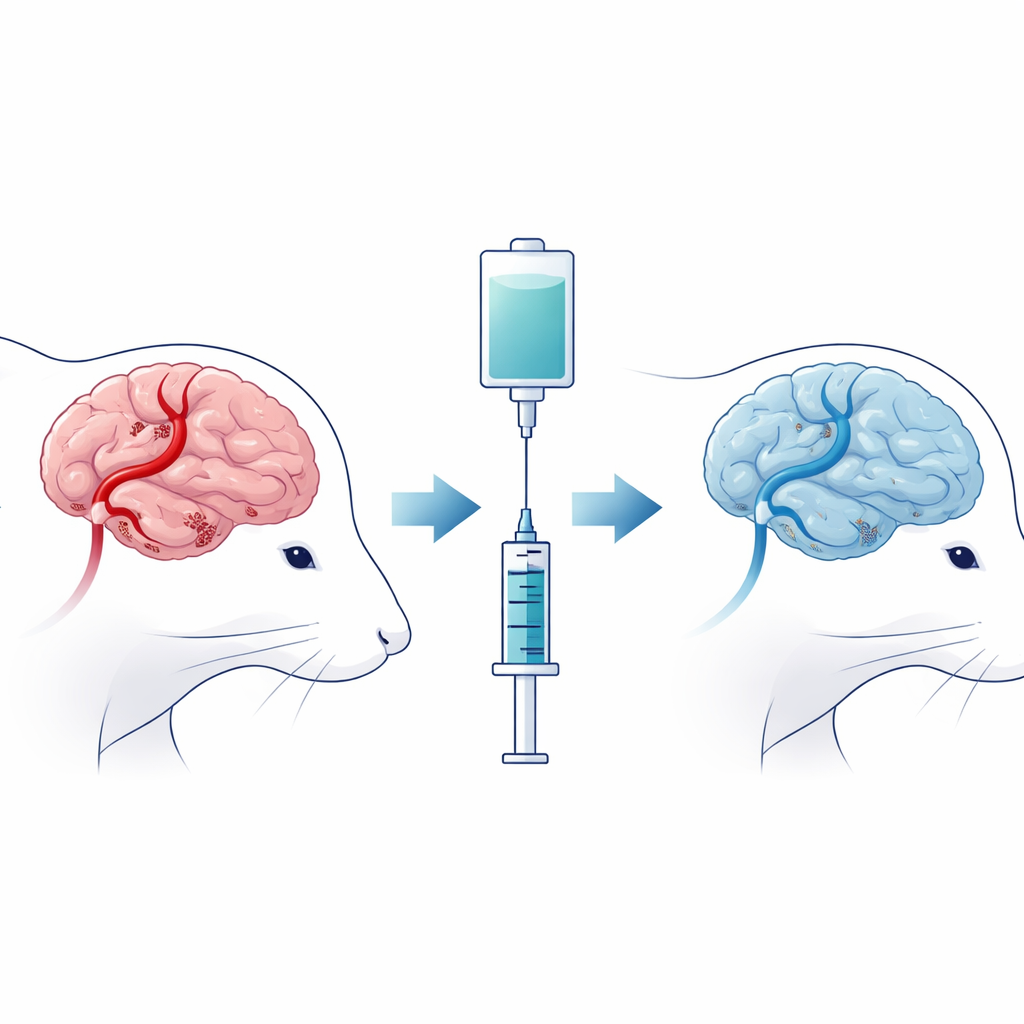
En dold form av celldöd driven av järn
Bortom synlig vävnadsskada fokuserade författarna på en nyligen erkänd typ av celldöd kallad ferroptos, som drivs av järn och okontrollerade kemiska reaktioner som angriper fettkomponenterna i cellmembran. I obehandlade stroke‑modellråttor innehöll vävnaden i den sårbara zonen kring skadans kärna mer järn, högre nivåer av en lipid‑skadeprodukt och nervcellernas mitokondrier såg svullna och strukturellt förstörda ut i elektronmikroskopet. Molekylära tester visade att skyddande proteiner som normalt detoxifierar skadliga lipidprodukter var minskade, medan proteiner som främjar denna destruktiva process var ökade. Ciprofol vände till stor del dessa förändringar: järn och lipid‑skador minskade, balansen mellan nyckelproteiner försköts mot skydd, och mitokondrierna behöll mer normala former och intern struktur.
En cellulär energisensor som kontrollväljare
Studien undersökte därefter hur ciprofol åstadkommer dessa skyddande effekter. Uppmärksamheten riktades mot AMPK, ett protein som fungerar som en cellulär energisensor och stressresponder. I de skadade hjärnorna hos obehandlade råttor var AMPK‑aktiviteten nedsatt. Ciprofol ökade den aktiverade formen av AMPK, parallellt med minskningarna i ferroptos‑relaterad skada. För att testa om denna energisensor verkligen ligger uppströms i den skyddande händelsekedjan använde forskarna ett annat läkemedel, Compound C, som blockerar AMPK. När djuren fick både ciprofol och denna AMPK‑hämmare gick ciprofols fördelar delvis förlorade: markörer för ferroptos gick tillbaka mot skadliga nivåer, järnackumulering återkom och AMPK‑signaleringen föll ännu lägre än hos obehandlade stroke‑djur. Detta mönster stödjer idén att aktivering av AMPK är ett nyckelsteg i hur ciprofol skyddar hjärnceller.
Dämpning av hjärnans inflammatoriska storm
Skador relaterade till stroke handlar inte bara om celldöd inne i neuroner; hjärnans immunologiska respons spelar också en stor roll. Forskarna mätte flera inflammatoriska budbärarmolekyler som typiskt stiger efter ischemia–reperfusion. Hos obehandlade djur var dessa signaler starkt förhöjda, vilket speglar en intensiv inflammatorisk reaktion. Ciprofol minskade samtliga tre huvudsakliga inflammationsmarkörer som mättes, vilket tyder på att det inte bara dämpar järndriven membranskada utan också lugnar den inflammatoriska storm som följer. När AMPK blockerades med Compound C försvagades dessa lugnande effekter på inflammationen, vilket återigen knyter ciprofols fördelar till denna centrala energisensorväg.
Vad detta kan innebära för framtida vård
Sammanfattningsvis tyder resultaten på att ciprofol kan vara mer än ett sedativum: i denna råttmodell verkar det begränsa stroke‑relaterad hjärnskada genom att aktivera AMPK, vilket i sin tur begränsar järndriven celldöd och dämpar inflammation. Eftersom ciprofol redan används kliniskt för anestesi och procedursedering är dess potentiella roll som hjärnskyddande medel särskilt intressant. Studien har dock viktiga begränsningar, bland annat beroendet av en enda djurmodell och möjligheten att AMPK‑hämmaren själv kan ha biverkningar. Fler studier, inklusive i andra arter och så småningom hos mänskliga patienter, behövs för att bekräfta om ciprofol säkert kan hjälpa till att skydda hjärnan under och efter strokebehandling.
Citering: Zeng, H., Yu, X., Zheng, Z. et al. Ciprofol attenuates cerebral Ischemia‒reperfusion injury in rats by inhibiting ferroptosis through upregulating AMPK. Sci Rep 16, 9282 (2026). https://doi.org/10.1038/s41598-026-40104-6
Nyckelord: ischemisk stroke, reperfusionsskada, ciprofol, ferroptos, neuroprotektion