Clear Sky Science · sv
MyoFuse är ett helt AI‑baserat arbetsflöde för automatiserad kvantifiering av fusion av skelettmuskulära celler in vitro
Varför räkning av muskelceller spelar roll
När vi tränar, återhämtar oss från skada eller utvecklar sjukdomar som diabetes, ombyggs våra skelettmuskler ständigt. I laboratoriet efterliknar forskare denna process genom att odla muskelceller i en skål och observera hur enskilda celler smälter samman till långa, flerkärniga fibrer. Ett enkelt tal, kallat fusionsindex, berättar hur väl denna fusion sker. I dag bestäms det talet ofta genom att personer manuellt räknar tusentals små cellkärnor på en skärm—ett långsamt arbete som kan bli inkonsekvent och feltolkat. Denna studie presenterar MyoFuse, ett helt AI‑baserat arbetsflöde som automatiserar denna räkningsuppgift i syfte att göra muskelforskning snabbare, mer tillförlitlig och mindre partisk.
Utmaningen att se vad som verkligen finns där
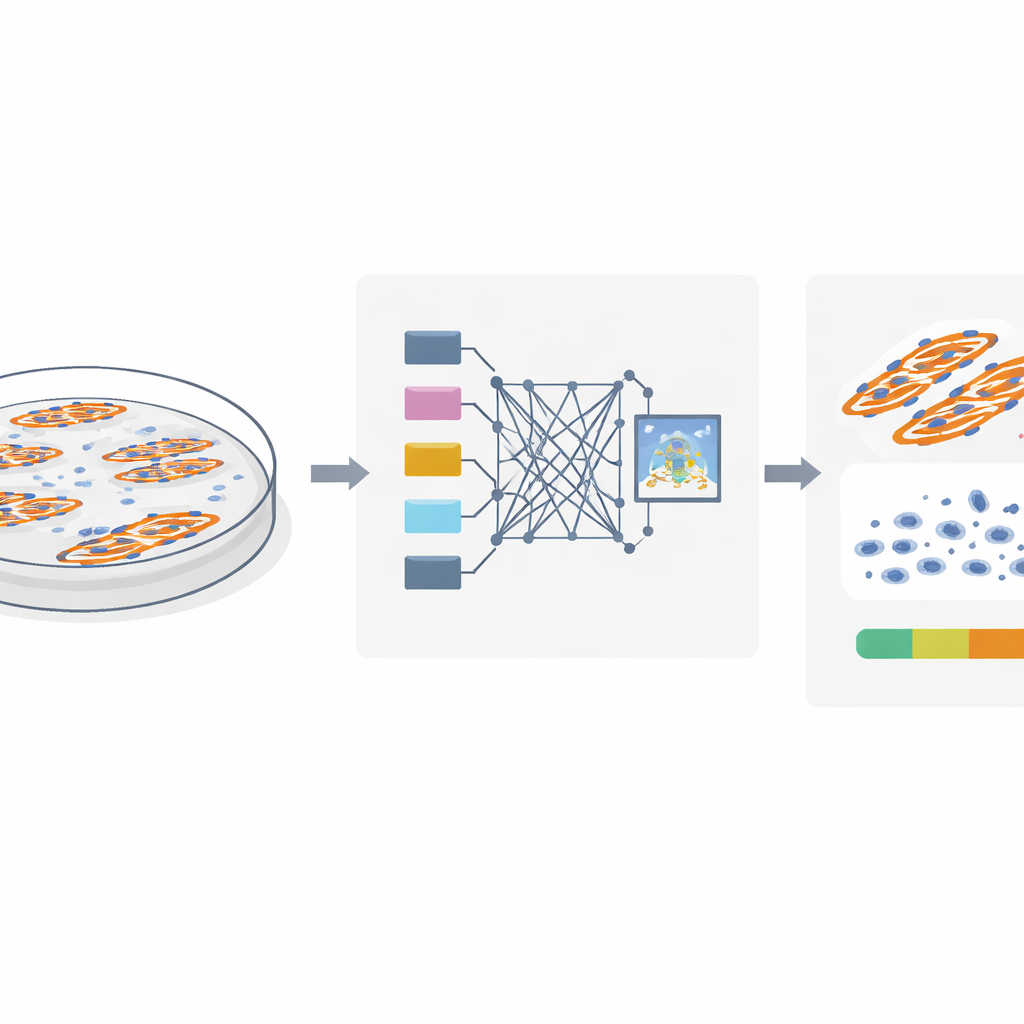
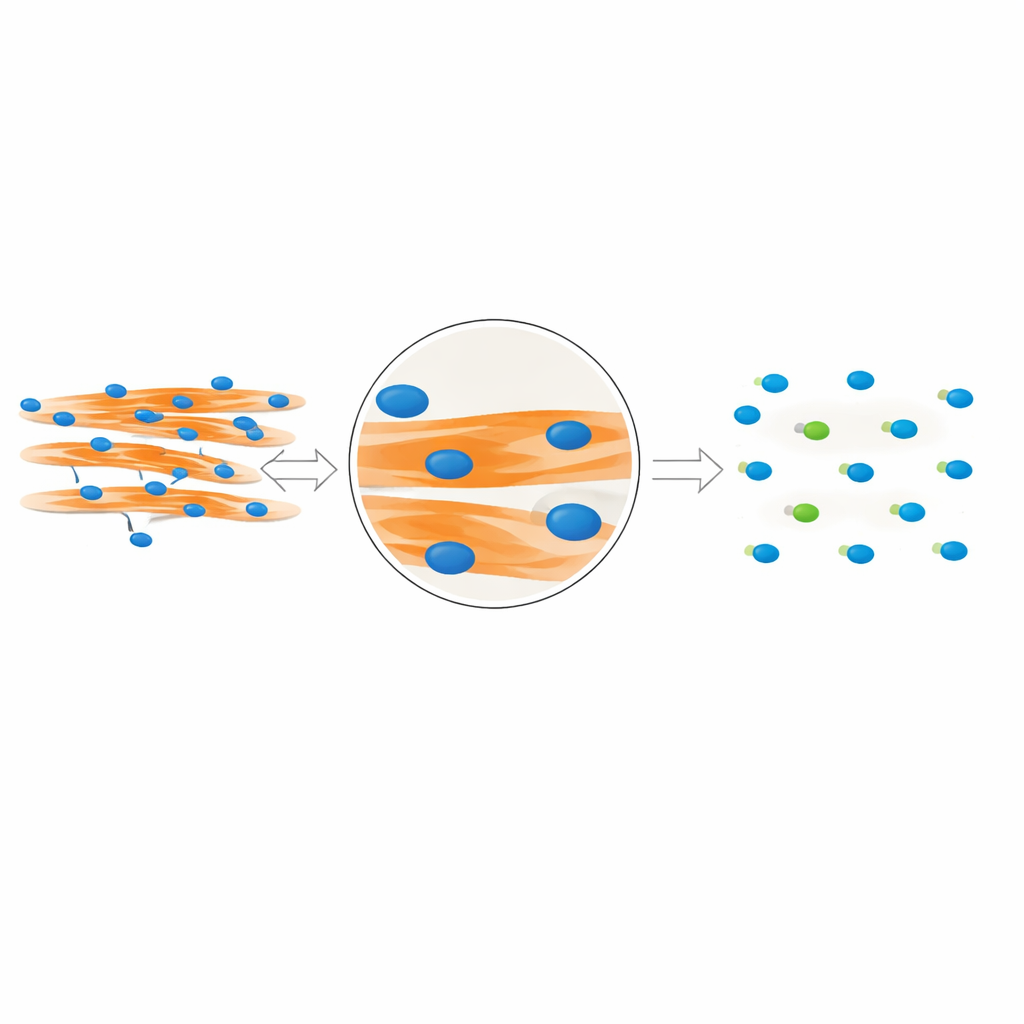
För att studera fusion av muskelceller färgar forskare cellkärnor och muskelfibrer med fluorescerande färgämnen och tar mikroskopbilder. Den centrala frågan är vilka kärnor som verkligen ligger inne i sammansmälta muskelfibrer och vilka som tillhör ofusade celler som ligger i närheten. Traditionella metoder antar att om en kärna överlappar en muskelfiber i en platt, tvådimensionell bild så måste den finnas inuti fibrerna. Men celler växer i tre dimensioner: en kärna kan ligga ovanför eller under en fiber och ändå se ut att överlappa i bilden. Författarna använder detaljerad konfokalbildtagning i både mus‑ och människomuskulatur för att visa att denna överlappningsregel kan vara missvisande, vilket gör att många närliggande kärnor felaktigt räknas som en del av sammansmälta fibrer och blåser upp fusionsindexet.
En smartare metod för att tolka fluorescensbilder
Teamet insåg att verkliga ”i‑fiber”‑kärnor lämnar ett distinkt visuellt fingeravtryck. Eftersom dessa kärnor fysiskt upptar utrymme inne i fibrerna skapar de små mörka luckor i den fluorescerande signalen som markerar muskelf Proteinet MyHC. Däremot stör inte kärnor som ligger ovanför eller under en fiber denna signal. Med detta som utgångspunkt utformade författarna MyoFuse, ett tvåstegs AI‑arbetsflöde. Först ritar en specialiserad segmenteringsmodell (anpassad från det öppna verktyget Cellpose) exakt ut individuella kärnor, även när de sitter tätt packade i kluster. Därefter undersöker ett lättviktigt neuralt nätverksklassificerare den omgivande MyHC‑signalen för varje kärna och avgör om den ligger inne i en muskelfiber eller utanför, baserat endast på detta lokala mönster snarare än på enkel överlappning.
Hur väl AI:n matchar mänskliga experter
Forskarlaget testade MyoFuse noggrant på bilder av mus‑C2C12‑celler och primära humana muskelceller från olika muskler. För båda arterna överensstämde AI:ns räkning av totala kärnor och det beräknade fusionsindexet mycket väl med noggranna manuella annotationer av experter, med nästintill perfekta korrelationer. På nivån för enskilda kärnor skilde klassificeraren korrekt mellan kärnor inne i och utanför fibrer i mer än 90 % av fallen över dataset, med prestandamått som når upp till mänsklig nivå. Viktigt är att MyoFuse också fungerade bra på en separat uppsättning mänskliga celler som aldrig använts för träning, vilket tyder på att metoden kan generalisera till nya prover i stället för att bara memorera träningsbilderna.
Avslöjar dold skevhet i vanliga metoder
Utöver sin noggrannhet exponerade MyoFuse systematiska problem i vitt använda mask‑baserade metoder som förlitar sig på enkel överlappning mellan kärn‑ och fibersignaler. När författarna jämförde fusionsindex från MyoFuse med ett förfinat mask‑förfarande på samma bilder överskattade maskmetoden konsekvent fusionen, särskilt i områden där muskelfibrerna täckte en större andel av ytan. Att justera detektionsgränser förändrade siffrorna men tog inte bort denna underliggande bias; till synes förbättringar berodde ofta på att fel släckte varandra snarare än bättre biologisk tolkning. Teamet visade också att fusionsuppskattningar kan variera kraftigt mellan olika regioner i en enda brunn, vilket understryker att analys av bara några handplockade fält kan ge en förvrängd bild av hur väl cellerna fusionerar.
Vad detta betyder för framtida muskelforskning
MyoFuse ger muskelbiologer ett sätt att mäta cellfusion som både är snabbare och trognare mot vad som faktiskt händer i skålen. Genom att kombinera automatisk mikroskopi med en AI som kan segmentera och klassificera hundratusentals kärnor på några minuter minskar arbetsbelastningen för människor, minimerar subjektiva val om var man ska titta och hur man sätter trösklar i bilder, och undviker att närliggande celler räknas som fusade muskelfibrer. Författarna medger att extrema avbildningsförhållanden eller mycket olika färgningsprotokoll kan kräva omträning, men metoden är öppet tillgänglig och utformad för att vara anpassningsbar. För laboratorier som studerar muskelutveckling, åldrande, regeneration eller metabola sjukdomar lovar MyoFuse mer robusta fusionsmätningar—och därigenom mer tillförlitliga slutsatser om hur muskler växer och förändras.
Citering: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
Nyckelord: skelettmuskel, cellfusion, artificiell intelligens, bildanalys, myogenes