Clear Sky Science · sv
RBP4 påverkar utvecklingen av skivepitelcancer i tungan genom att hämma PI3K/AKT-signalvägen och främja makrofagpolarisation mot M1-typ
Varför tungcancer kräver nya idéer
Tungcancer kan beröva människor förmågan att tala, äta och smaka, och även med operation, cytostatika och strålbehandling är långtidsöverlevnaden ofta otillfredsställande. Denna studie undersöker en oväntad hjälpare i vårt blod, ett vitamin A–bärande protein kallat RBP4, och visar hur det både kan bromsa tillväxten av tungtumörer och samla kroppens egna immundefender. Genom att avslöja hur denna molekyl verkar inne i cancerceller och i de omgivande immuncellerna pekar forskningen mot nya strategier som en dag kan göra behandlingar mer effektiva och mindre skadliga.
Ett dolt protein i tungtumörer
Forskarna började med att sålla i stora cancer-genomdatabaser för att se vilka immuntillhörande gener som kunde förutsäga hur patienter med skivepitelcancer i tungan klarar sig över tid. Bland hundratals kandidater framträdde RBP4, ett protein mest känt för att transportera vitamin A i blodet, som särskilt intressant. När teamet jämförde tumörprover med närliggande frisk tungvävnad fann de att RBP4-nivåerna konsekvent var mycket lägre i cancern. Detta mönster bekräftades i flera oberoende dataset och i vävnadsprover från 20 patienter, vilket tyder på att förlust av RBP4 är ett vanligt drag i denna sjukdom.
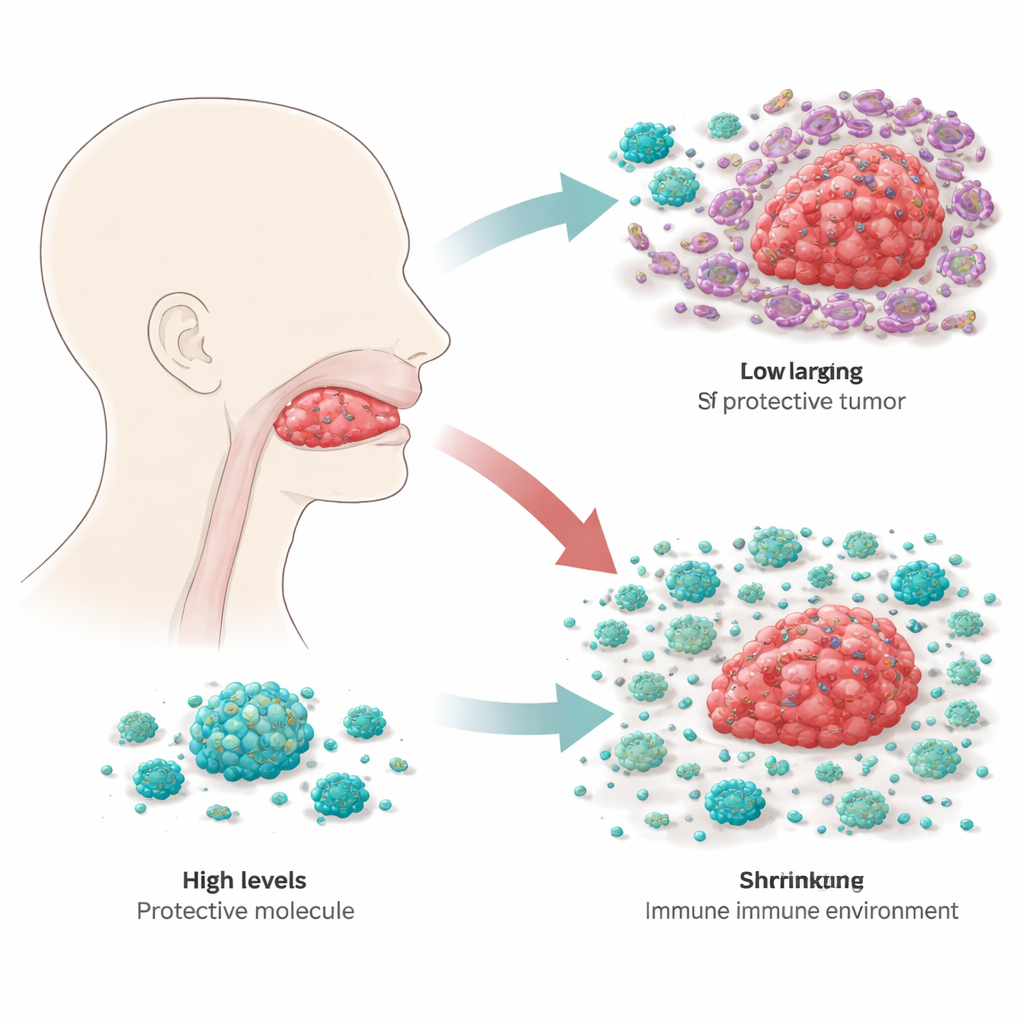
Bromsning av tumörtillväxt inifrån
För att ta reda på vad RBP4 faktiskt gör i tungcancerceller konstruerade forskarna tumörcellinjer som antingen producerade extra RBP4 eller mycket mindre av det. I odlingar växte celler med högre RBP4 långsammare, medan de med reducerat RBP4 delade sig snabbare och var bättre på att röra sig och invadera genom artificiella membran — beteenden kopplade till spridning och återfall. När dessa modifierade celler injicerades i möss förblev tumörer med extra RBP4 mindre, medan tumörer med minskad RBP4 växte mer aggressivt. Genom att följa nyckelregulatorer för tillväxt inne i cellerna visade teamet att RBP4 dämpar en huvudväg för tillväxt känd som PI3K–AKT–mTOR, vilken många cancerformer förlitar sig på som en intern gaspedal. Med höga nivåer av RBP4 är denna väg tystare och tumörcellerna har svårare att anta det flexibla, rörliga tillstånd som underlättar migration.
Förvandla immunceller till tumörbekämpare
Cancer växer inte isolerat; den lever inom ett grannskap av immunceller, blodkärl och stödjeceller kallat tumörmikromiljön. Här spelar makrofager — stora immunceller som antingen kan attackera eller hjälpa tumörer — en central roll. Forskarna märkte att tumörer med mer RBP4 också tenderade att innehålla fler av makrofagtypen “M1”, som förknippas med inflammation och tumördödande aktivitet, snarare än “M2”-typen, som ofta stöder tumörtillväxt. I cellkultur, när makrofager exponerades för antingen renat RBP4 eller tungcancerceller som designats att utsöndra mer RBP4, skiftade de mot detta M1-, tumörbekämpande tillstånd. När RBP4 minskades i cancercellerna tenderade makrofagerna istället att glida mot en mer tumörvänlig profil.
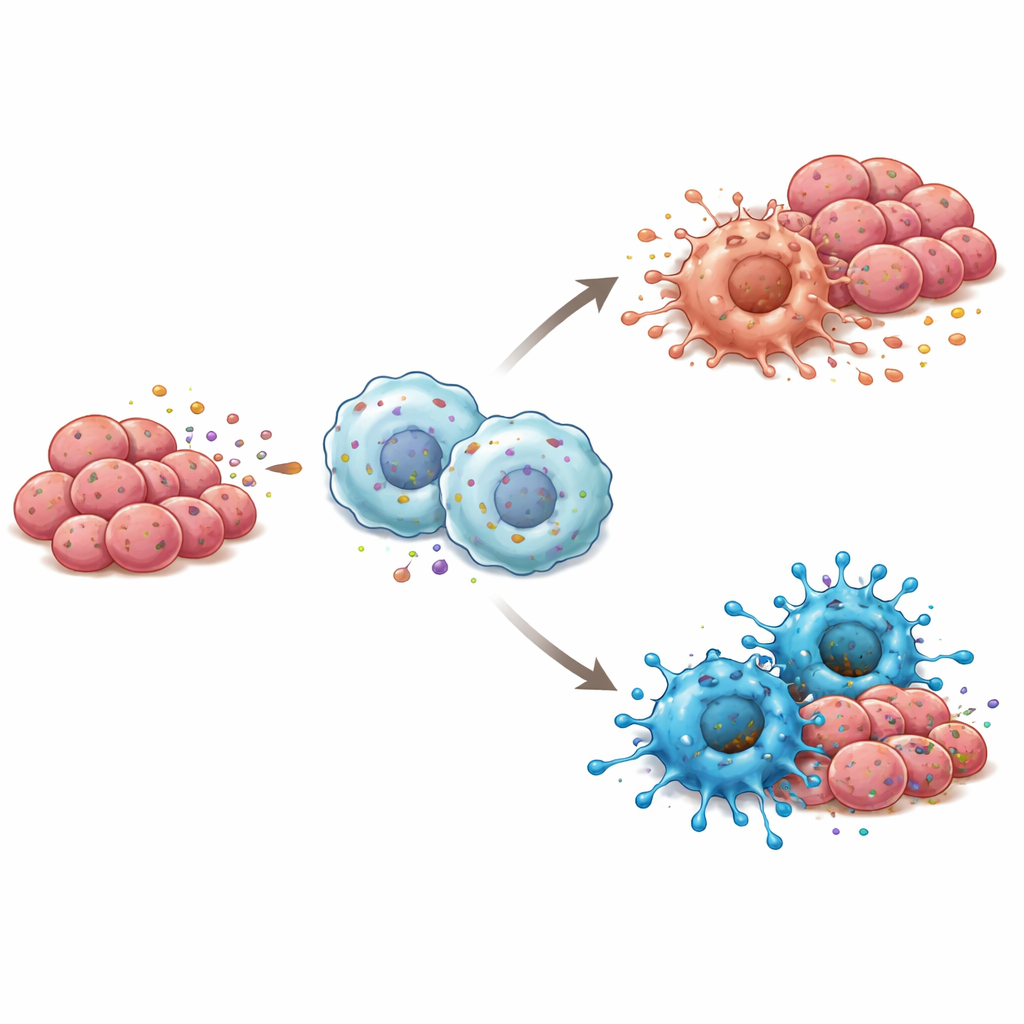
Signalvägar bakom immunskiftet
För att förstå hur RBP4 puffar makrofager mot en mer fientlig hållning gentemot tumörer undersökte forskarna vilka interna alarmsystem som aktiverades i dessa immunceller. De fann att RBP4 stimulerade en sensor kallad TLR4 på makrofagernas yta och i förlängningen aktiverade NF-κB, en huvudomkopplare som driver inflammatoriska responser. Att blockera TLR4 med en kemisk hämmare satte stopp för denna kedjereaktion och förhindrade att makrofager antog M1-tillståndet, även i närvaro av RBP4. I möss växte tumörer bildade av tungcancerceller rika på RBP4 och blandade med makrofager långsammare och innehöll fler M1-typceller, tillsammans med starkare TLR4- och NF-κB-aktivitet, vilket stärker idén att denna väg är nyckeln till RBP4:s immuneffekter.
Vad detta kan betyda för framtida vård
Sammantaget framställer arbetet RBP4 som en dubbelriktad broms mot tungcancer: inne i tumörcellerna dämpar det en överaktiv tillväxtkrets, och i tumörens omgivning hjälper det till att omvandla makrofager till mer vaksamma försvarare. Även om många frågor kvarstår — såsom exakt hur RBP4 interagerar med sina mål och hur man bäst kan höja det säkert — tyder studien på att återställande eller efterliknande av RBP4:s effekter både kan sakta tumörspridning och stärka kroppens eget immunsvar mot cancern. För patienter väcker det utsikten om framtida terapier som inte bara skär bort tumörer, utan också omformar deras interna kopplingar och lokala “ekosystem” för att förhindra återfall.
Citering: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Nyckelord: tungcancer, RBP4, tumörmikromiljö, makrofager, PI3K AKT-väg