Clear Sky Science · sv
Påverkan av oxidation av G-kvadrupel-RNA på dess konformationsdynamik och interaktion med ALS-associerade TDP-43
Varför detta är viktigt för nervhälsa
Amyotrofisk lateralskleros (ALS) är en dödlig sjukdom där nervcellerna som kontrollerar rörelse gradvis dör, men de grundläggande orsakerna till denna selektiva skada är fortfarande gåtfulla. Denna studie ställer en enkel men viktig fråga: när vi åldras och våra celler utsätts för mer ”rostlik” kemisk skada, stör denna nötning på RNA — arbetskopian av våra gener — viktiga signaler som håller motorneuron vid liv? Genom att zooma in på en speciell veckad RNA-form och ett nyckelprotein kopplat till ALS som kallas TDP-43, visar arbetet hur små kemiska ärr kan bidra till att bana väg för sjukdom.
En skör RNA-knut i motorneuronens hjärta
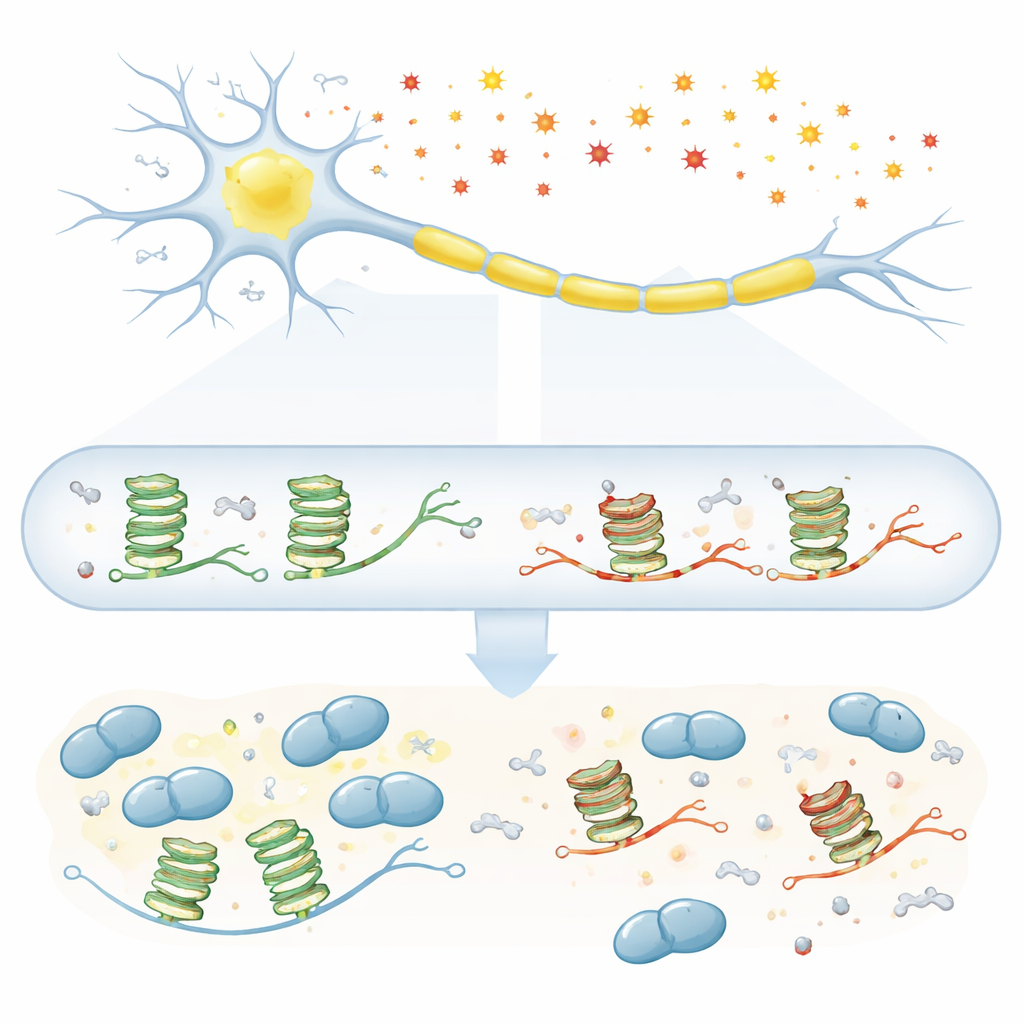
Motorneuron är beroende av långt avstånds‑transport av RNA‑budskap längs sina axoner så att proteiner kan tillverkas på plats, nära kopplingarna till musklerna. Många av dessa budskap bär en speciell strukturell ”knut” kallad en G‑kvadrupel, uppbyggd av sekvenser rika på basen guanin. Proteiner som TDP-43 känner igen denna knut och hakar på RNA:t till transportgranuler som rör sig längs axonen. Problemet är att guanin också är den bas som lättast oxideras när celler utsätts för reaktiva syrearter, vilka ackumuleras med åldern. Tidigare ledtrådar föreslog att G‑kvadrupeler och TDP‑43 är centrala i ALS, men det var oklart exakt hur oxidation av dessa RNA‑knutar skulle kunna störa deras samverkan.
Att iaktta hur oxidativ stress förvränger RNA‑former
Forskaren exponerade först humana neuroblastomceller för väteperoxid, ett vanligt oxiderande medel, och undersökte därefter tillståndet hos G‑kvadrupelstrukturerna. Signaler från en G‑kvadrupel‑känslig prob sjönk i takt med att den oxiderande stressen ökade, vilket indikerar att dessa kompakt veckade RNA‑knutar förlorade sin normala form. För att fastställa kemin byggde teamet syntetiska RNA‑sekvenser som bildar G‑kvadrupeler och blandade in varierande mängder 8‑oxoguanin, en välkänd oxiderad form av guanin som finns i åldrande neuroner och i ALS‑vävnad. Med en uppsättning biofysiska metoder visade de att redan måttliga nivåer av denna modifiering lossar den ordnade staplingen i G‑kvadrupelen, även om det exakta utfallet beror på den omgivande RNA‑sekvensen.
Nya fel: felparade baser och felkopplade strängar
Närmare analys avslöjade två distinkta typer av strukturella problem. I en G‑kvadrupel härstammande från PSD‑95‑budskapet tenderade oxiderade guaniner att para sig olämpligt med närliggande adenin, och bildade ”mismatchar” som subtilt förvrängde veckningen. Dessa mismatchar såg ut att uppstå lättast vid medelnivåer av oxidation, när RNA:t fortfarande tillfälligt kunde montera en G‑kvadrupel som förde fel partners i kontakt. I en annan G‑kvadrupel från CaMKIIα‑budskapet destabiliserade kraftig oxidation den vanliga intramolekylära knuten så starkt att de kvarvarande intakta guaninerna sökte partners på andra RNA‑strängar och främjade onormala intermolekylära G‑kvadrupeler. Sådana felkopplade strukturer kan trassla samman olika RNA och störa normal RNA‑trafik inne i neuronerna.
När skadat RNA förlorar sin proteinpartner
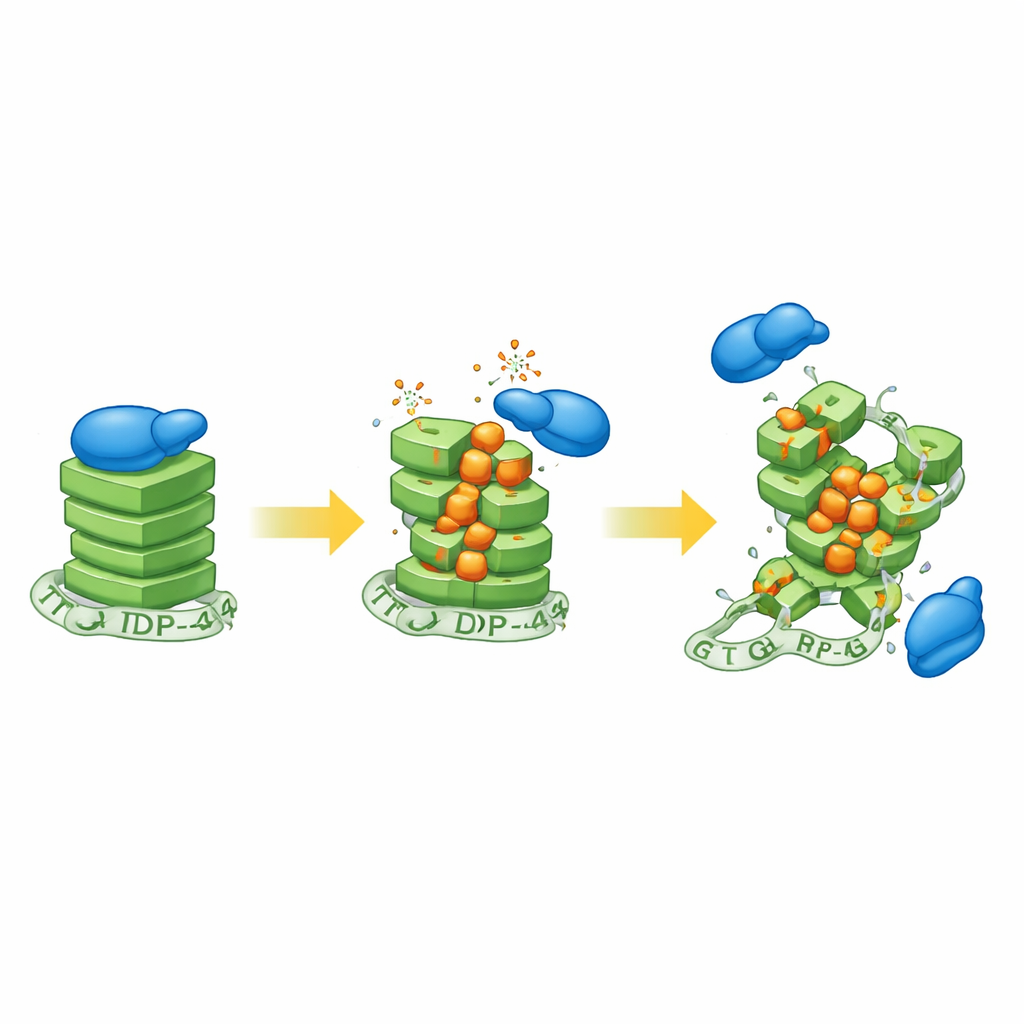
Studien undersökte därefter hur dessa förvrängda knutar interagerar med TDP‑43. Med gelbaserade bindningsanalyser visade forskaren att TDP‑43 starkt föredrar intakta, parallella G‑kvadrupeler och i allt högre grad misslyckas med att binda när fler oxiderade baser introduceras. CaMKIIα‑strukturen, redan tätt packad, visade sig vara särskilt känslig: även låg oxidation nästan eliminerade TDP‑43‑bindning. Ett annat protein, FUS — också kopplat till ALS — uppvisade en liknande men något mindre allvarlig förlust i affinitet, vilket tyder på att oxidation generellt försvagar greppet hos G‑kvadrupel‑bindande proteiner. Intressant nog pekade bevisen på att när TDP‑43 blandades med lätt oxiderat RNA, engagerade proteinet en instabil intermediär form av G‑kvadrupelen snarare än en fullständigt veckad knut, vilket antyder en dynamisk kamp mellan stabilisering och sönderfall.
Ökad sårbarhet i ALS‑kopplade mutantproteiner
Arbetet granskade vidare tio TDP‑43‑varianter som hittats hos ALS‑patienter, de flesta med förändringar i en flexibel, glycinrik svans som finjusterar RNA‑igenkänningen. Alla dessa mutanter band redan normala G‑kvadrupeler svagare än vildtypproteinet. När oxiderade G‑kvadrupel‑RNA introducerades som konkurrenter var mutanterna ännu mindre kapabla än det normala proteinet att känna igen och binda de skadade strukturerna. Vissa varianter belägna i särskilt oordningsbenägna regioner påverkades mest. Detta antyder ett dubbelträff i åldrande individer som bär sådana mutationer: inte bara är deras TDP‑43 i grunden mindre effektivt, utan åldersrelaterad RNA‑oxidation urholkar ytterligare dess förmåga att föra viktiga budskap längs motorneuronens axoner.
Vad detta betyder för förståelsen av ALS
Enkelt uttryckt visar denna studie att åldersdriven kemisk skada omformar känsliga RNA‑knutar som vägleder budskapstransport i motorneuron, och dessa missformade knutar samarbetar inte längre väl med TDP‑43 eller relaterade proteiner. Resultatet är en ökad sannolikhet för felriktade eller fastnade RNA‑laster, särskilt i de långa, sårbara axoner som håller muskler under kontroll. För personer som dessutom ärver TDP‑43‑mutationer kan denna oxidationsinducerade försvagning av RNA–protein‑interaktioner föra redan stressade neuroner närmare kollaps. Genom att belysa denna subtila men potenta kedja av händelser — från oxidativ stress till förändrad RNA‑arkitektur till störd transport — framhäver arbetet oxidation av G‑kvadrupel‑RNA som en lovande molekylär länk mellan åldrande och ALS och som ett potentiellt mål för framtida skyddande terapier.
Citering: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Nyckelord: amyotrofisk lateralskleros, RNA-oxidation, G-kvadrupel, TDP-43, motorneurondegeneration