Clear Sky Science · sv
Autism spektrumstörningsassocierad Sema5A p.Arg676Cys driver Arf6/FE65‑signalering och aberrant cellmorfogenes
Hur en liten förändring kan rubba hjärnans kopplingar
Autism spektrumstörning påverkar hur människor kommunicerar, samspelar och reagerar på omvärlden, men de biologiska stegen som leder från en DNA‑förändring till förändrad hjärnfunktion är ofta gåtfulla. I den här studien undersöks en sådan genetisk förändring i ett hjärnans ”väglednings”protein kallat Sema5A och visar, med ovanlig detaljrikedom, hur ett enda utbytt byggsten i proteinet kan få unga nervceller att växa onormalt långa, trassliga utskott. Att förstå detta mikroskopiska kopplingsfel kan så småningom hjälpa forskare att utforma behandlingar som styr nervceller tillbaka mot en hälsosammare form.
Nervceller som växer för långt
Under hjärnans utveckling skickar unga nervceller ut långa, tunna utskott som söker efter rätt partners och bildar de kretsar som ligger till grund för tanke och beteende. Denna tillväxt måste vara noggrant reglerad: för lite förgrening innebär att celler inte kopplar upp sig; för mycket kan göra att kretsarna blir brusiga eller felkopplade. Tidigare arbete visade att en autismkopplad variant av Sema5A, där en aminosyra vid position 676 ändrats från arginin till cystein, får nervceller i odling att bilda ovanligt långa utskott. Den nya studien ville ta reda på vilka interna brytare och hjälpproteiner denna mutanta Sema5A använder för att driva sådan okontrollerad tillväxt.
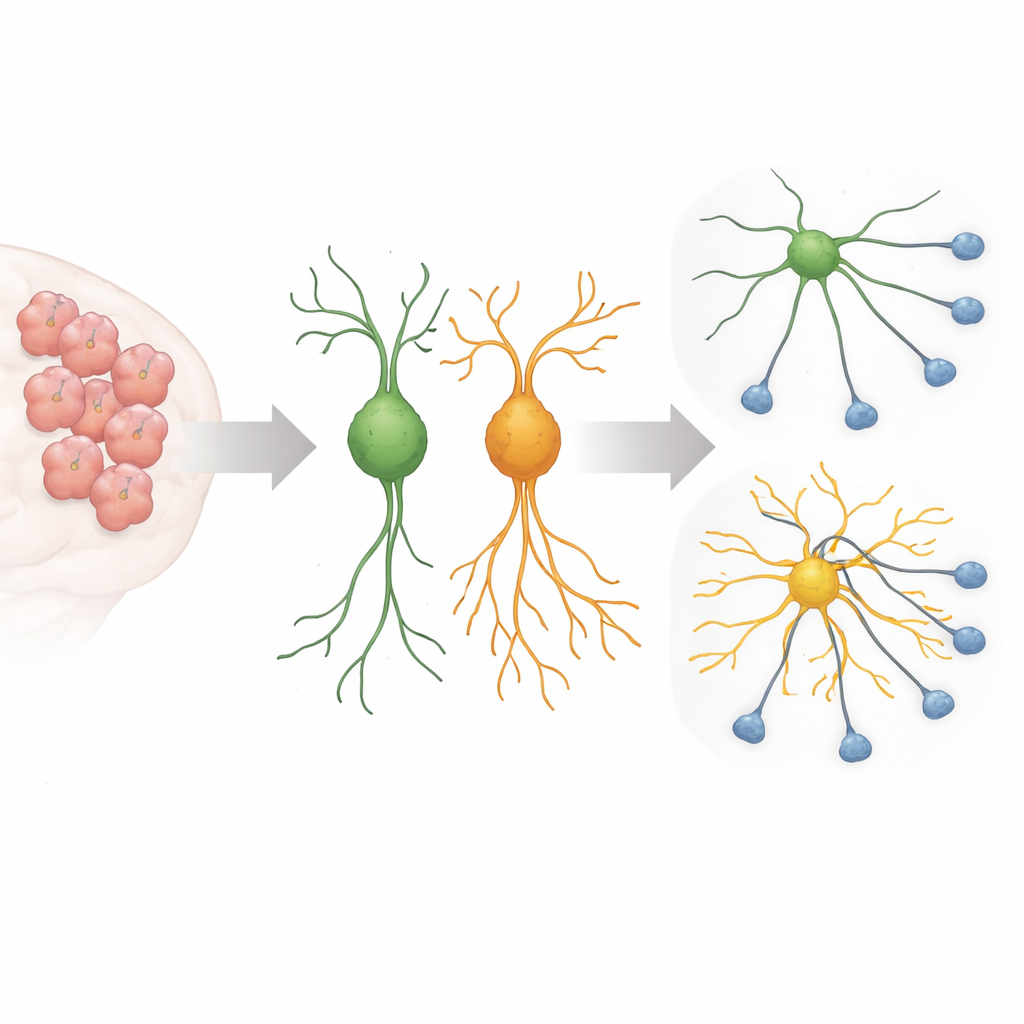
En vilseledande signal inuti cellen
Forskarna fokuserade på en liten molekylär brytare kallad Arf6 och ett ställningsprotein kallat FE65, båda kända för att påverka cellmembran och det inre skelett som stöder cellutskott. Genom att använda ett CRISPR–Cas13‑system för att selektivt minska dessa proteiners nivåer i musliknande nervceller och i primära mus-hjärnceller fann de att sänkning av Arf6 eller FE65 kraftigt minskade den överdrivna utväxten orsakad av mutanten Sema5A. De långa, spindellika utskotten krympte mot mer typiska längder och markörer för neuronal mognad minskade, vilket tyder på att mutationens effekt i hög grad beror på just denna signalväg.
Koppling till cellens formmotor
I nervceller fungerar en familj molekyler som en form‑”motor” genom att reglera aktin, det huvudsakliga strukturella filamentet i cellers utskott. En viktig medlem i denna familj, Rac1, blir normalt aktiv för att hjälpa neuriter att växa, men för hög aktivitet kan driva okontrollerad tillväxt. Teamet visade att i celler med normal Sema5A krävs Arf6 för vanlig Rac1‑aktivering under hälsosam utväxt, medan FE65 inte är avgörande. Med den mutanta Sema5A blev dock både Arf6 och FE65 kritiska: att sänka någon av dem, eller att översvämma cellen med just den FE65‑region som binder dess partner ELMO2, reducerade den abnormt höga Rac1‑aktiviteten mot det normala. Detta antyder att den skadliga versionen av Sema5A specifikt utnyttjar ett Arf6–FE65–ELMO2–DOCK5‑komplex för att överstimulera Rac1 och få neuriter att växa för långt.
En trång knutpunkt av signaleringspartners
För att se hur dessa delar hänger ihop studerade forskarna även ELMO2‑baserade ”signalosomer”—kluster av proteiner som sätts ihop för att vidarebefordra tillväxtsignaler. När Arf6 eller FE65 minskades bildade celler som uttryckte mutant Sema5A färre av dessa ELMO2‑komplex i sina cellekroppar och växande toppar, i linje med idén att Arf6 och FE65 hjälper till att bygga den apparat som omvandlar Sema5A‑mutationen till en fysisk förändring i cellform. Arbetet passar in i en bredare bild där små molekylära brytare som Arf6 och Rac1, hjälpta av ställningsproteiner som FE65, fungerar som centrala nav som kopplar många autism‑associerade gener till den slutliga arkitekturen hos hjärnans kretsar.
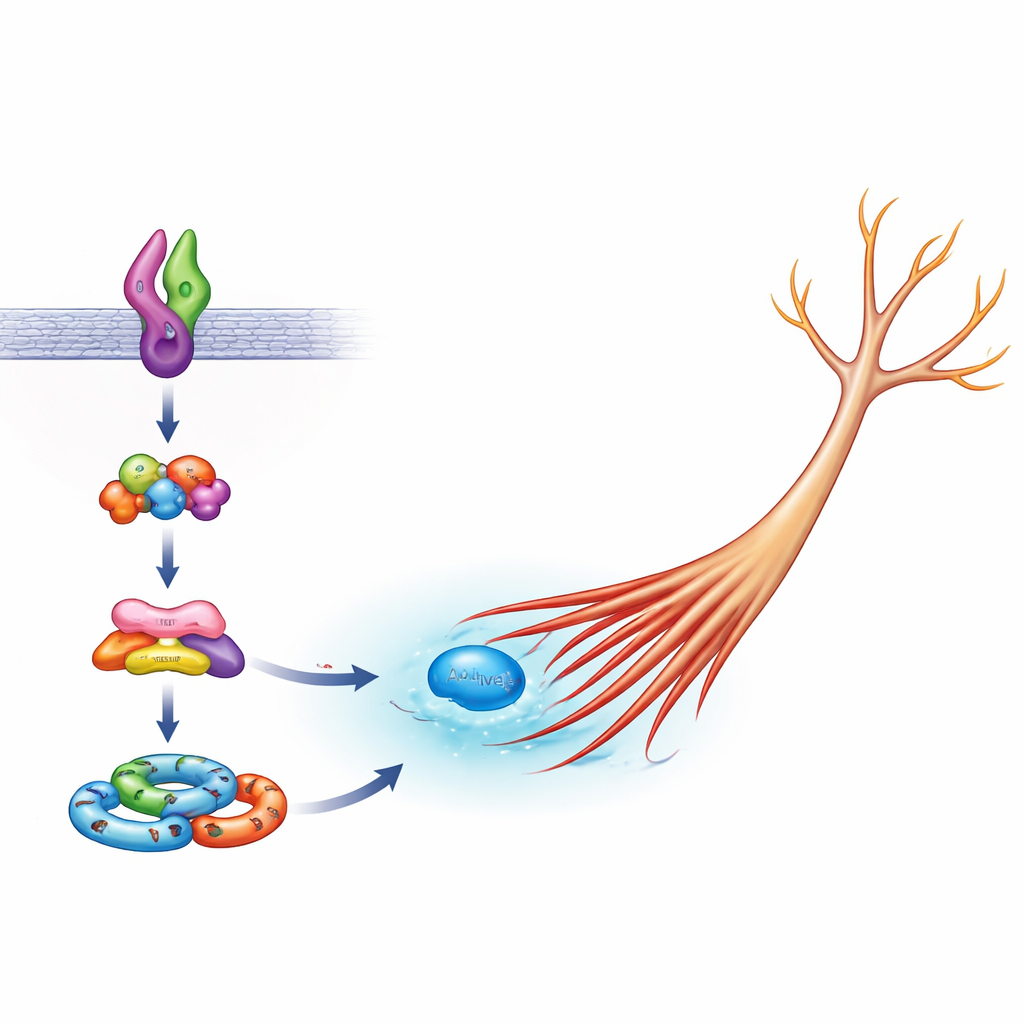
Varför denna mikroskopiska kedja spelar roll
För icke‑specialister kan alfabetssoppan av proteinnamn verka avlägsen från den levda erfarenheten av autism. Ändå erbjuder denna studie en konkret bro: den spårar hur en precis genetisk förändring i Sema5A kan överaktivere en specifik kedja av hjälpmolekyler, vilket får nervceller att förlänga sina utskott för mycket och potentiellt koppla hjärnan på atypiska sätt. Genom att peka ut Arf6, FE65 och ELMO2‑signalkomplexet som avgörande länkar i denna kedja framhäver arbetet potentiella framtida läkemedelsmål. I princip skulle läkemedel som varsamt dämpar denna överaktiva bana en dag kunna hjälpa till att korrigera de underliggande cellformsförändringarna som är förknippade med Sema5A‑relaterade former av autism, och därigenom lägga en viktig pusselbit i förståelsen av neurodevelopmentala störningar.
Citering: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Nyckelord: autism spektrumstörning, Sema5A‑mutation, neuronal morfogenes, Rac1‑signalering, Arf6 FE65‑väg