Clear Sky Science · sv
Målstyrning av specifika neuronala typer i icke-mänskliga primathjärnor med en rekombinant immunotoxin riktad mot murint CD25
Varför denna hjärnstudie är viktig
Att förstå hur specifika grupper av hjärnceller styr rörelse, känslor och beteende är avgörande för att behandla sjukdomar som Parkinsons sjukdom och autism. Men hjärnan är en tät skog av sammanflätade celler, och de flesta verktyg fäller många “träd” samtidigt. Denna studie visar ett sätt att ta bort endast en utvald celltyp i en apas hjärna med minimal kollateral skada, vilket öppnar dörren för mycket skarpare experiment om hur särskilda kretsar formar beteende och sjukdom.
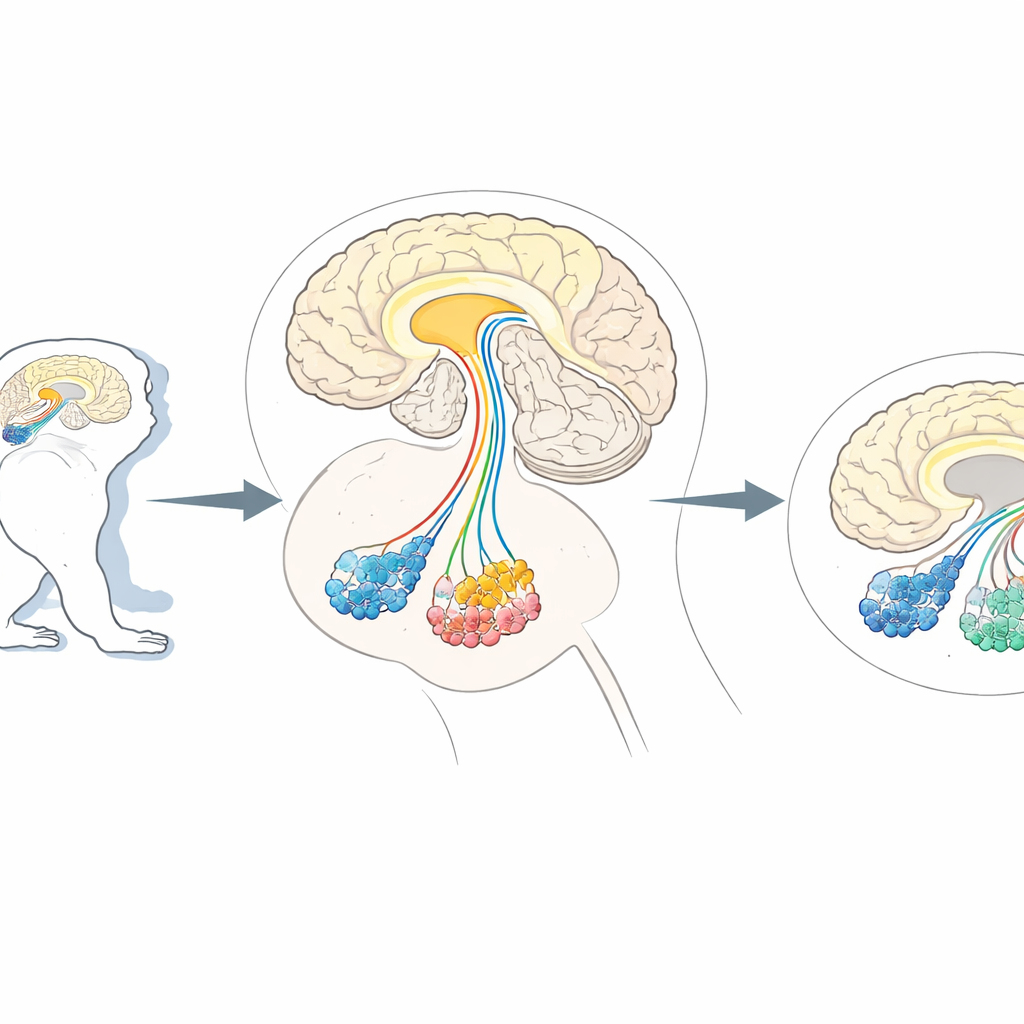
Behovet av precis “cellbeskärning” i hjärnan
Forskare vänder sig ofta till icke-mänskliga primater, som marmosetter och makaker, eftersom deras hjärnor är organiserade mycket på samma sätt som våra. Dessa djur är ovärderliga modeller för tillstånd som påverkar högre hjärnfunktioner, från parkinsoniska rörelsestörningar till autismliknande förändringar i socialt beteende. Befintliga metoder kan tysta eller stimulera specifika banor, men att faktiskt avlägsna bara en typ av neuron i dessa komplexa hjärnor utan att skada andra har varit svårt. Tidigare arbete i möss använde ett knep: utvalda neuroner konstruerades för att visa en cellmembranmarkör kallad CD25, som kan kännas igen av ett designat toxin som dödar endast de märkta cellerna. Men denna samma markör förekommer naturligt i primaters immunceller och möjligen även i vissa hjärnceller, vilket ökar risken att toxinet skulle angripa fel mål hos apor.
Utformning av ett säkrare molekylärt skalpell
Författarna gav sig i kast med att bygga en ny molekylär skalpell anpassad för användning i primater. Istället för att rikta in sig på den humana versionen av CD25 fokuserade de på den murina (mus-)versionen, som är mycket mindre lik den naturliga CD25 som finns hos apor. De immuniserade först en kanin med mus-CD25-proteinet och använde en chipbaserad metod för att fiska upp individuella kaninceller som producerade antikroppar som band starkt till mus-CD25 men inte till den humana formen. Från dessa identifierade de en framstående antikropp, kallad RMAb-52, med mycket hög bindningsstyrka. De sammanfogade sedan de nyckeldelarna av denna antikropp med en toxisk fragment från bakterien Pseudomonas för att skapa ett enskilt konstruerat ”immunotoxin”-protein, benämnt anti-mCD25-PE38.
Sätta verktyget på prov
I provrörsexperiment grep det nya immunotoxinet tag i mus-CD25 mycket starkare än i human CD25, vilket bekräftade dess selektivitet. När det applicerades på kultiverade celler som konstruerats att bära mus-CD25 minskade toxinets dos kraftigt cellöverlevnaden vid mycket låga koncentrationer, medan celler med human CD25 lämnades oskadda. Nästa steg togs i levande marmosetter. Med hjälp av en särskild viral vektor som färdas retrogradt längs nervfiberna levererade de mus-CD25-genen till dopaminproducerande neuroner som sänder signaler från ett djupt hjärnområde kallat substantia nigra till striatum, en bana som är avgörande för rörelsekontroll. Efter att ha gett viruset tid att slå på markören i dessa neuroner injicerade de anti-mCD25-PE38-proteinet direkt i det målinriktade mellanhjärnsområdet.
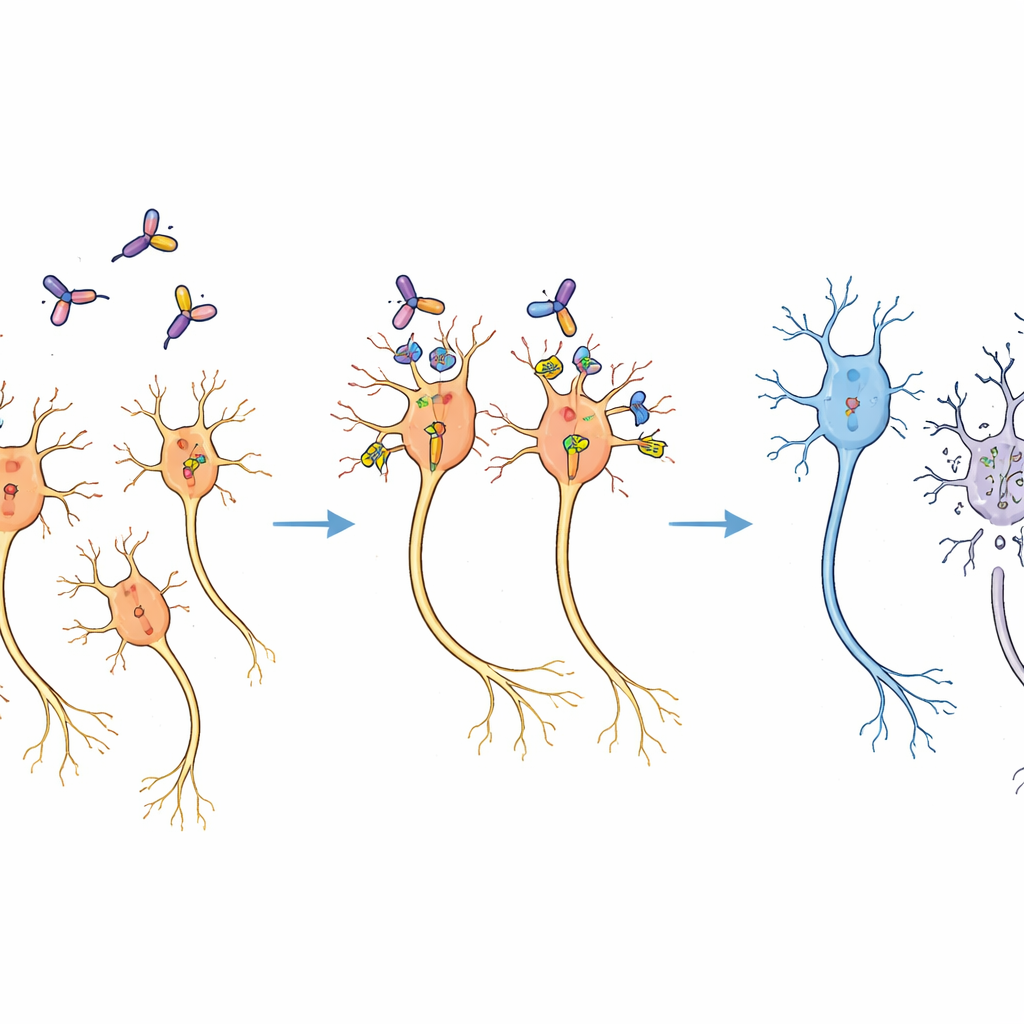
Selektiv förlust utan omfattande skada
Två veckor efter behandlingen berättade hjärnsektioner från marmosetterna en tydlig historia. På den sida som fick immunotoxinet var antalet dopaminneuroner reducerat till ungefär två tredjedelar jämfört med den obehandlade sidan, vilket visades med färgning för ett dopaminproducerande enzym. Likväl såg den omgivande hjärnvävnaden normal ut i mikroskopet, och andra hjärnregioner som också fått den virala vektorn uppvisade ingen tydlig cellförlust. Pilotexperiment hade redan fastställt en doseringsintervall som undvek icke-specifik vävnadsskada, och den valda dosen låg väl inom detta säkra fönster. Mönstret av förlust matchade den förväntade spridningen av virus och toxin, vilket indikerar att neuroner eliminerades specifikt eftersom de konstruerats att visa mus-CD25, inte för att toxinet skadade celler ospecifikt.
Vad detta betyder för framtida hjärnforskning
För en lekman är huvudbudskapet att forskarna har byggt en mycket selektiv raderingsknapp för valda neuronpopulationer i primathjärnor. Genom att kombinera ett retrogradt viralt leveranssystem med ett mus-specifikt immunotoxin kan de ta bort definierade banor—till exempel dopaminkretsar inblandade i Parkinsons sjukdom—samtidigt som närliggande celler sparas. Denna strategi undviker farliga korsreaktioner med djurets egen CD25 och bör vara särskilt användbar när den naturliga receptorn är närvarande eller förhöjd vid sjukdom. På lång sikt kommer detta tillvägagångssätt att hjälpa forskare kartlägga hur enskilda vägar i hjärnans ledningsnät bidrar till rörelse, beslutsfattande och psykiatriska symtom, vilket för oss närmare riktade behandlingar som justerar felaktiga kretsar istället för att i stort påverka hela hjärnan.
Citering: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Nyckelord: neurovetenskap hos icke-mänskliga primater, immunotoxinriktning, dopaminneuroner, marmosethjärnkretsar, modeller för Parkinsons sjukdom