Clear Sky Science · sv
Hypoxi‑inducerbart faktor 1α utövar dubbla roller i urinblåsans cancerprogression genom TIMP3‑medierad reglering av angiogenes och invasion
Varför syrebrist i tumörer är viktig
Cancerceller växer ofta så snabbt att de hinner före blodtillförseln, vilket lämnar delar av en tumör utan tillräckligt med syre. Denna lågsyremiljö, eller hypoxi, tvingar cellerna att slå på överlevnadsprogram som kan göra cancer svårare att behandla. I urinblåsecancer — en vanlig tumör i urinvägarna — har forskare länge misstänkt att ett sådant syresensorprogram, styrt av ett protein som kallas HIF-1α, främst hjälper tumörer att växa och spridas. Denna studie går närmare in och hittar en överraskande tvist: under vissa förhållanden kan nedreglering av HIF-1α faktiskt göra urinblåsecancerceller mer aggressiva, och ett annat protein, TIMP3, ligger i centrum för detta paradoxala samband.
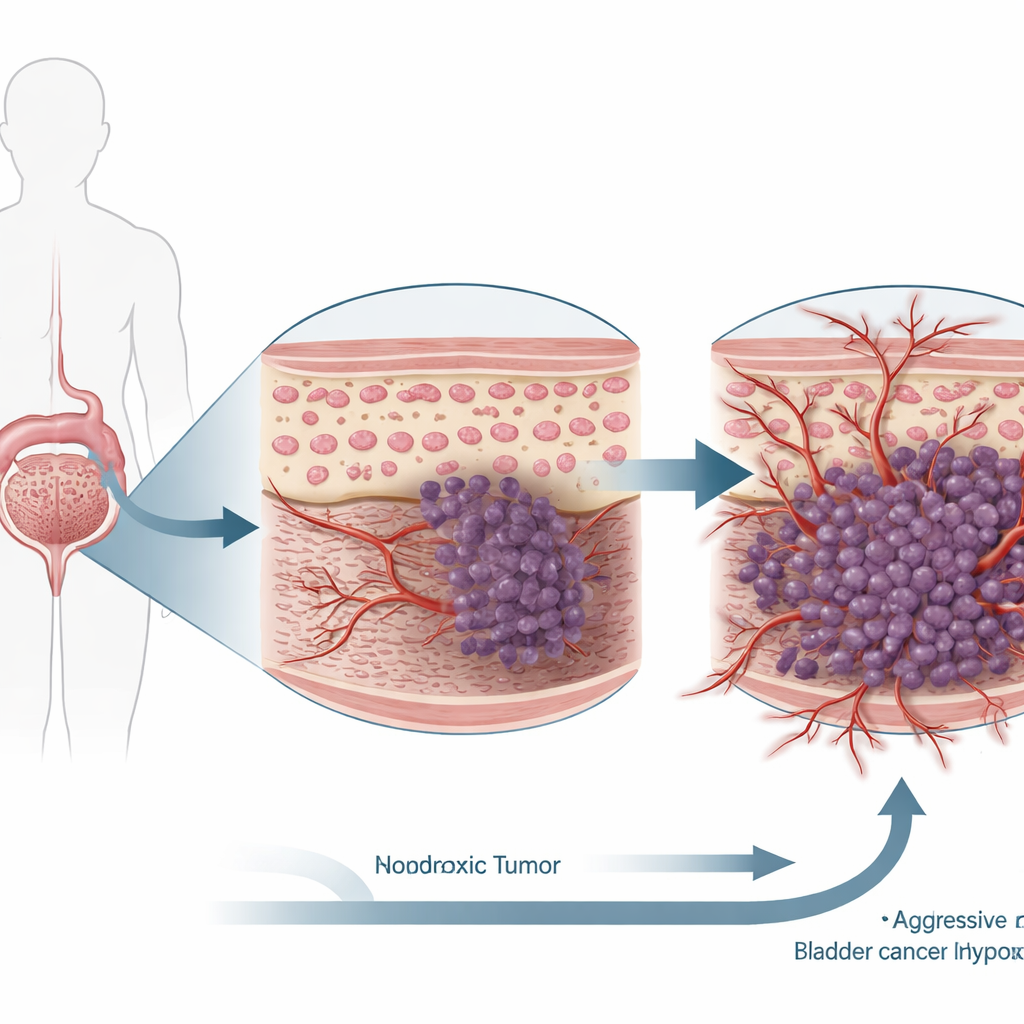
Närmare titt på urinblåsecancerceller
Forskarna arbetade med två väletablerade humana urinblåsecancercellinjer och exponerade dem antingen för normala syrenivåer eller för hypoxi, vilket efterliknar de syrefattiga fickorna i verkliga tumörer. De använde sedan genetiska verktyg för att dämpa HIF-1α i dessa celler och mätte hur denna förändring påverkade grundläggande canceregenskaper: hur snabbt cellerna delade sig, hur benägna de var att dö, och hur väl de kunde röra sig, invadera genom en barriär och stimulera nybildning av blodkärl. Parallellt undersökte de urinblåsetumörprover från patienter för att jämföra nivåer av HIF-1α och TIMP3 i cancerös vävnad versus närliggande normal blåsvävnad.
En överraskande rollomkastning vid låg syrehalt
Patientprover bekräftade att HIF-1α faktiskt är högre i urinblåsetumörer än i normal vävnad, i linje med dess rykte som en tumörfrämjande faktor. Ändå hade nedtagning av HIF-1α under hypoxi i cellexperimenten motsatt effekt mot vad många skulle förvänta sig. När HIF-1α slogs ner och syret var knappfött, växte cancercellerna snabbare över tid, var mindre benägna att genomgå programmerad celldöd och blev bättre på att migrera och invadera genom modellbarriärer. De utsöndrade också signaler som uppmuntrade kärlceller att bilda tätare, mer omfattande rörliknande nätverk — ett kännetecken för ökad tumörblodtillförsel. Kort sagt: med mindre HIF-1α i en lågsyremiljö uppvisade urinblåsecancercellerna mer malignt beteende.
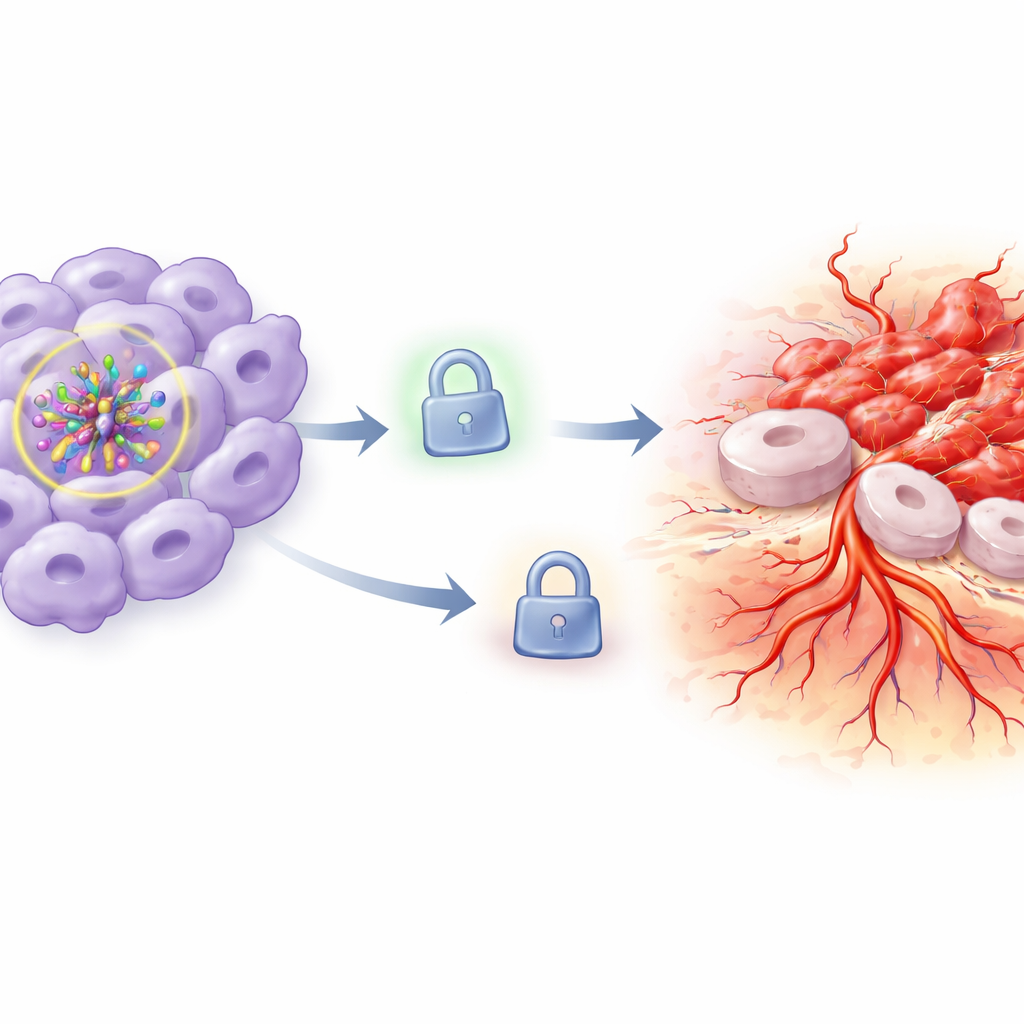
Bromsen som försvann vid tumörspridning
För att förstå varför detta hände fokuserade teamet på TIMP3, ett protein som normalt fungerar som en broms på vävnadsnedbrytning och ny kärltillväxt genom att blockera enzymer som bryter ner den omgivande matrixen. I HIF-1α‑reducerade celler under normala syreförhållanden förblev TIMP3‑nivåerna relativt höga. Men när syrenivåerna sjönk föll TIMP3‑proteinet kraftigt. Denna förlust av TIMP3 stämde väl överens med den observerade ökningen av invasion och kärlbildning: med bromsen försvagad kunde cancercellerna lättare omforma sin omgivning och expandera. Forskarna vände sedan utvecklingen genom att tvinga fram överuttryck av TIMP3 i celler där HIF-1α fortfarande var nedreglerat under hypoxi. Återställandet av TIMP3 vände till viss del — och i många fall nästan helt — det aggressiva beteendet: cellerna växte mindre, dog lättare, rörde sig och invaderade mindre och inducerade färre och kortare rörliknande kärlstrukturer.
Vad detta betyder för framtida behandlingar
Dessa fynd tyder på att HIF-1α har en dubbel natur i urinblåsecancer. Å ena sidan är dess totala nivåer högre i tumörer och det driver kända cancerfrämjande program. Å andra sidan verkar det under svår syrebrist bidra till att upprätthålla den skyddande närvaron av TIMP3. Att ta bort HIF-1α i det sammanhanget kan oavsiktligt sänka TIMP3 och släppa lös ett mer invasivt, kärlblodstimulerande beteende. För behandling innebär detta att en enkel blockad av HIF-1α kan få negativa konsekvenser om man inte samtidigt hittar sätt att bevara TIMP3 eller liknande bromsmekanismer. Arbetet betonar vikten av att förstå inte bara enstaka mål utan det bredare nätverket av motvikter som formar hur en tumör svarar på sin hårda, syrefattiga miljö.
Citering: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
Nyckelord: urinblåsecancer, tumörhypoxi, HIF-1α, TIMP3, angiogenes