Clear Sky Science · sv
Molekylär dockning och dynamik avslöjar nya CDK6‑hämmare för riktad glioblastomterapi
Varför denna hjärncancerstudie är viktig
Glioblastom är en av de mest aggressiva formerna av hjärncancer, och för många patienter fungerar dagens behandlingar fortfarande inte tillräckligt bra eller länge nog. Denna studie undersöker ett nytt sätt att angripa glioblastom genom att rikta in sig på en enda överaktiv kontrollpunkt i tumörcellerna, ett protein kallat CDK6. Med hjälp av avancerade computersimuleringar istället för djurförsök eller provrör sorterade forskarna igenom hundratals läkemedelslika molekyler och identifierade en särskilt lovande kandidat, kallad förening 21, som en dag skulle kunna hjälpa till att bromsa eller stoppa denna dödliga sjukdom.
En dödlig tumör som undviker nuvarande behandlingar
Glioblastom växer snabbt, invaderar närliggande hjärnvävnad och återkommer nästan alltid efter operation, strålning och kemoterapi. Standardläkemedel som temozolomid kan först krympa tumörer, men många cancerceller anpassar sig och blir resistenta, vilket leder till återfall. En anledning är att deras interna maskineri för celldelning är fast i ”gå”-läge. Proteiner som kallas CDK:er fungerar som tidshjul som talar om för cellerna när de ska kopiera sitt DNA och dela sig. I glioblastom är CDK4/6‑vägen ofta överaktiv, vilket driver cellerna att föröka sig även i mötet med strålning och läkemedel. Det gör CDK6 till ett tilltalande mål: om forskare kan stänga av det selektivt i tumörceller kan de kanske bromsa tillväxten och få befintliga behandlingar att fungera bättre.
På jakt efter en bättre CDK6‑hämmare på datorn
I stället för att börja i laboratoriet genomförde teamet en storskalig virtuell sökning. De började med en känd CDK6‑bindande molekyl och bad ett screeningsprogram att hitta hundratals liknande strukturer från en läkemedelsdatabas. Av 400 inledande kandidater valdes 109 ut för detaljerad dator‑dockning mot den tredimensionella strukturen av mänskligt CDK6. Dockning är som att prova många nycklar i ett lås: programvaran förutspår vilka molekyler som glider mest tätt in i proteinets aktiva ficka och hur starkt de kan binda. Fyrtioåtta kandidater såg ännu bättre ut än referensmolekylen, men en, förening 21, stack ut med den starkaste förutsagda bindningen och särskilt fördelaktiga kontakter vid specifika platser på CDK6 som är kända för att styra selektivitet.
Kontrollera om den ”virtuella medicinen” beter sig som ett verkligt läkemedel
Sterk bindning är bara en del av historien; ett användbart läkemedel måste också nå hjärnan, lösa sig väl och undvika att skada frisk vävnad. Forskarna använde ytterligare program för att uppskatta hur varje toppkandidat skulle absorberas, transporteras i kroppen och elimineras. Förening 21 klarade standardregler för ”läkemedelslikhet”, visade god förväntad löslighet och, viktigt för hjärntumörer, förutsågs korsa blod‑hjärnbarriären samtidigt som den förblev relativt säker. Ett separat toxicitetsverktyg föreslog att, bortsett från potentiella problem vid mycket höga perorala doser, var förening 21 mindre benägen än många andra att irritera hud eller ögon eller orsaka svåra akuta skador. Ett annat beräkningsset undersökte hur elektroner är fördelade inom molekylen, vilket gav ledtrådar om dess kemiska stabilitet och benägenhet att bilda oönskade sidoreaktioner; dessa tester gynnade återigen förening 21 framför referensläkemedlet.
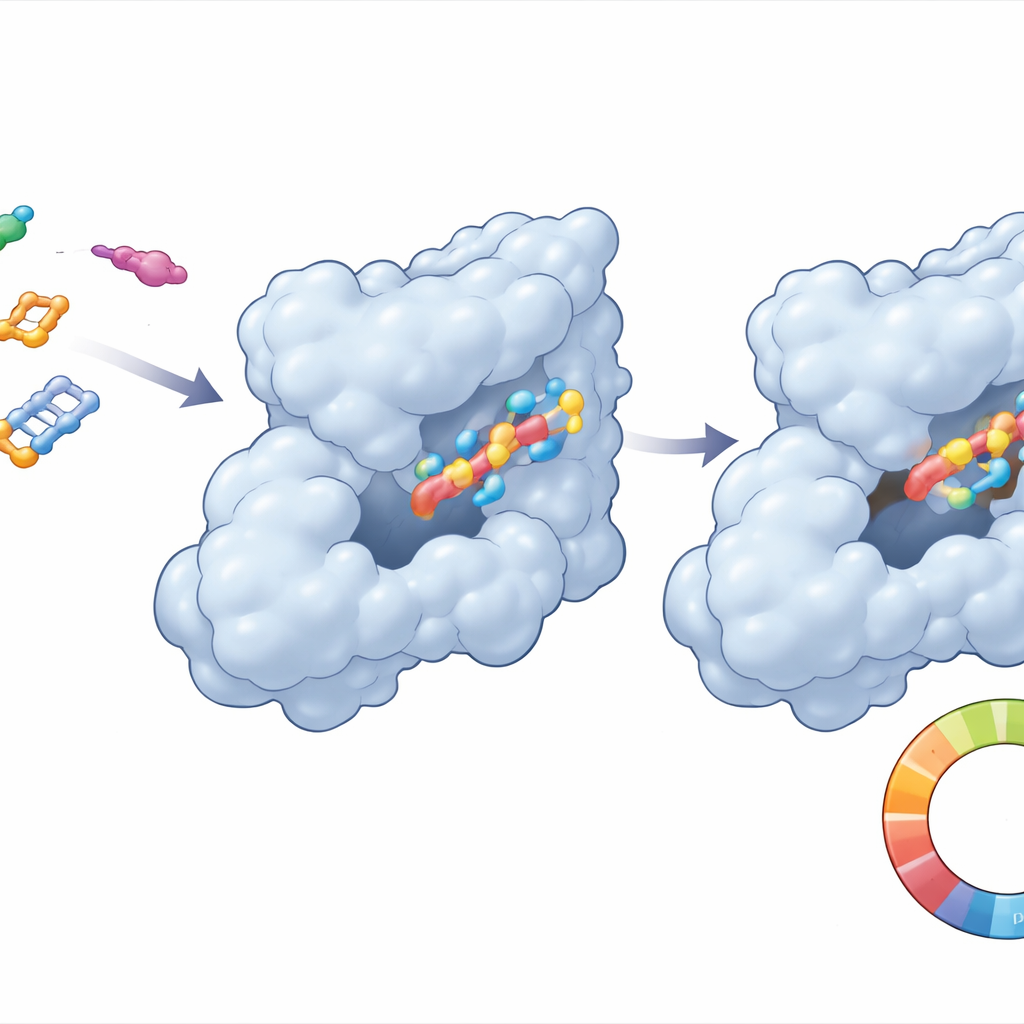
Se läkemedlet och dess mål röra sig tillsammans
Eftersom proteiner och läkemedelsmolekyler inte är stela körde teamet långa dator‑”filmer” på 250 miljarder sekunddelar för att se hur CDK6 och varje förening faktiskt beter sig i en vatten‑ och kroppslik miljö. För förening 21 satte sig komplexet snabbt i en stabil arrangemang och svajade bara måttligt, ett gott tecken på att molekylen skulle stanna kvar i CDK6‑fickan. Viktiga kontaktpunkter mellan läkemedlet och proteinet bibehölls, medan CDK6:s övergripande form förblev kompakt. I kontrast visade referensföreningen större fluktuationer och svagare, mindre konsekventa kontakter. Ytterligare energiberäkningar stödde idén att CDK6 föredrar att binda förening 21 mer tätt, huvudsakligen genom täta hydrofoba (oljliknande) interaktioner och välplacerade vätebindningar.
Vad detta kan innebära för framtida vård av hjärncancer
Sammantaget bygger dessa datorbaserade tester ett starkt case för att förening 21 är en högkvalitativ utgångspunkt för ett nytt glioblastomläkemedel riktat mot CDK6. Den verkar mer selektiv, mer stabil och bättre lämpad för att nå hjärnan än referensmolekylen, samtidigt som den undviker många vanliga toxicitetsfällor. Arbetet befinner sig dock fortfarande i en prediktiv fas: inga celler eller djur behandlades i denna studie. Nästa steg blir att syntetisera förening 21, testa om den verkligen bromsar glioblastomcellstillväxt i laboratoriet och se hur den beter sig i djurmodeller. Om dessa studier bekräftar simuleringarna kan denna molekyl — eller förbättrade versioner av den — så småningom bidra till mer precisa, riktade terapier som ger glioblastompatienter bättre odds och längre bestående kontroll över sin sjukdom.
Citering: Khan, M.U., Munir, M., Manzoor, H. et al. Molecular docking and dynamics reveal novel CDK6 inhibitors for targeted glioblastoma therapy. Sci Rep 16, 9000 (2026). https://doi.org/10.1038/s41598-026-39629-7
Nyckelord: glioblastom, CDK6‑hämmare, riktad terapi, virtuell läkemedelscreening, hjärncancer