Clear Sky Science · sv
En zebrafisk-multimodal verktygslåda för att studera blod-hjärnbarriären i hälsa och sjukdom
Varför läckande hjärnkärl spelar roll
När blodkärl i hjärnan eller ögat börjar läcka tränger vätska och proteiner in i den omgivande nervvävnaden och orsakar svullnad som kan sudda ut synen eller försämra tankeförmågan. Denna form av "vattenmättnad"—kallad vasogent ödem—spelar en roll vid diabetisk synförlust, stroke, hjärnskador och vissa former av demens. Ändå saknar forskare fortfarande enkla och prisvärda sätt att i realtid följa när denna skyddande barriär sviktar. Denna studie introducerar en mångsidig zebrafiskmodell som gör det möjligt för forskare att se, mäta och undersöka hur högt blodsocker försvagar hjärnans kärlbarriär, vilket potentiellt kan påskynda sökandet efter nya behandlingar.
En liten fisk med en tydlig fördel
Zebrafisklarver erbjuder ett unikt fönster in i den levande hjärnan. Till skillnad från däggdjur är deras kroppar genomskinliga i tidig ålder, och deras hjärnans blodkärl kan göras lysande under mikroskopet. Författarna utnyttjade detta genom att fokusera på blod–hjärnbarriären, den täta tätningen mellan blod och hjärnvävnad som liknar den inre blod–retinabarriären som skyddar våra ögon. Eftersom samma celltyper och många av samma skyddande proteiner delas mellan hjärna och näthinna, använde teamet hjärnbarriären i zebrafisk som en modell för att studera sjukdomar som diabetiskt makulaödem och andra neurovaskulära störningar—men i ett snabbare, mer etiskt och billigare system än traditionella gnagarmodeller.
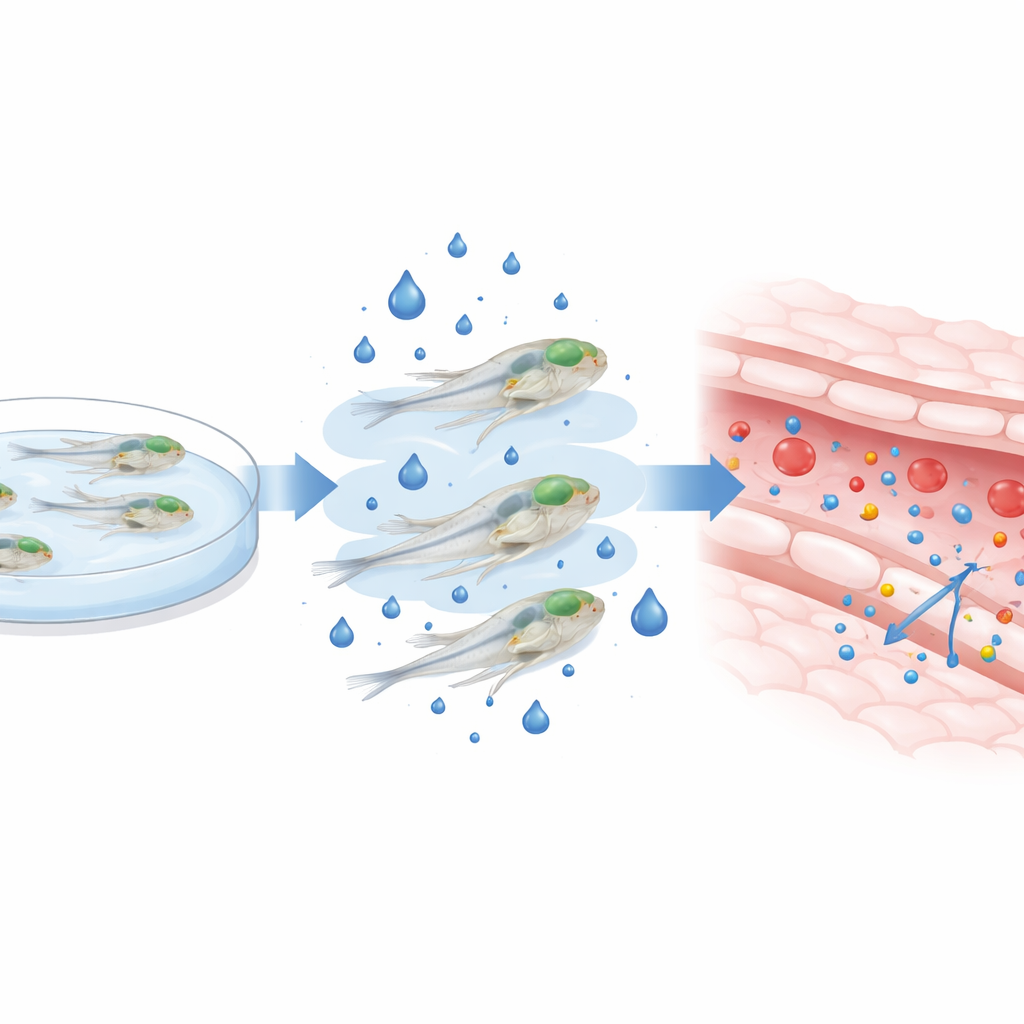
Att höja blodsockret hos babyzebrafisk
För att efterlikna det höga blodsocker som ses vid diabetes höjde forskarna zebrafisklarver i vatten innehållande extra glukos mellan tre och fem dagar efter befruktningen—ett kritiskt fönster då hjärnbarriären fortfarande mognar. De bekräftade att detta yttre sockbad drev upp interna glukosnivåer flera gånger om utan att döda larverna eller förändra deras allmänna form. Med fiskarna fortfarande vid liv och simmande injicerade de fluorescerande färgämnen av olika storlekar i cirkulationen och använde högupplösta konfokala mikroskop för att följa hur mycket färg som sipprade från hjärnans blodkärl ut i den omgivande vävnaden. Efter två dagars exponering för högt glukos läckte både små och stora färgmolekyler mer in i hjärnan, särskilt vid den högre socker-dosen, vilket indikerar att barriären blivit mer genomsläpplig.
Vad som händer med kärlväggen
Utöver att bara mäta läckaget byggde teamet en multimodal "verktygslåda" för att undersöka vad som gick fel i kärlväggen själv. De mätte bredden på en viktig hjärnartär och fann att högt glukos orsakade att kärlet vidgades—en tidig förändring som också ses hos människor med diabetisk ögonsjukdom. Genom att använda zebrafisk som är genetiskt konstruerade för att lysa upp specifika proteiner visade de att högt glukos minskade nivåerna av claudin-5, en huvudkomponent i de täta tätningarna mellan intilliggande kärlcellers, och ökade nivåerna av PLVAP, ett protein förknippat med omogna, läckagebenägna kärl som transporterar material över cellagret. Elektronmikroskopi, som kan avslöja strukturer på nanometerskala, bekräftade subtil utvidgning vid fogarna mellan celler, även om de små transportfickorna kallade caveolae var för få till antalet för att kvantifieras tillförlitligt i detta första genomförande.
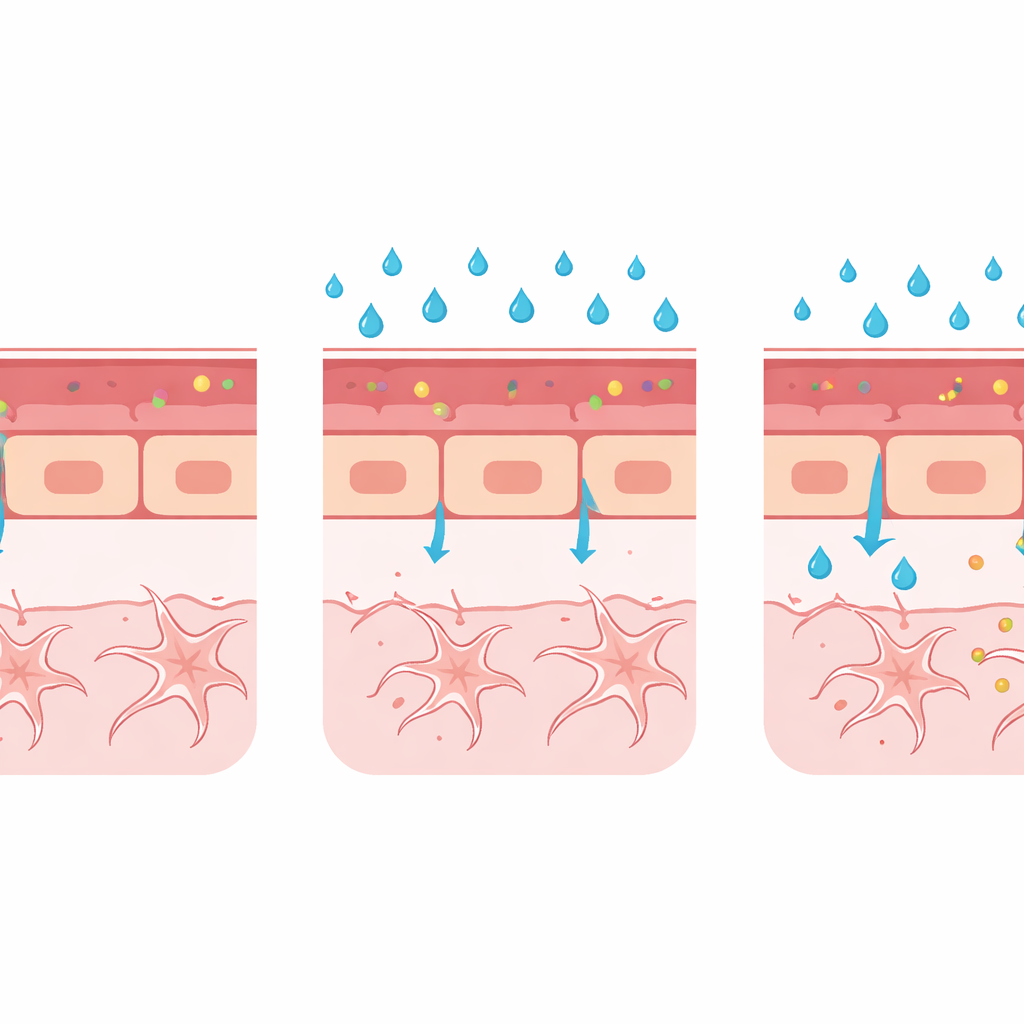
En flexibel plattform för framtida sjukdomsforskning
Tillsammans ger dessa förändringar—ökad färgläckage, vidare kärl, svagare cellförbindelser och ökad PLVAP—en konsekvent bild: högt blodsocker kan fördröja eller störa korrekt barriärbildning i den utvecklande hjärnan. Modellen fångar ännu inte upplösningen av en fullt mogen barriär, som sker vid kronisk mänsklig sjukdom, men den är utmärkt för att visa hur skadliga förhållanden under utveckling kan hindra barriären från att någonsin tätas ordentligt. Eftersom teknikerna är kompatibla med ett antal fluorescerande rapportörlinjer och avancerad avbildning kan samma plattform utvidgas för att studera andra utlösare av barriärsvikt, såsom inflammatoriska molekyler, förändrade stödjande celler som pericyter och gliaceller, eller störningar i nyckelsignalvägar.
Vad detta betyder för patienter
För icke-specialister är huvudbudskapet att detta arbete levererar en praktisk, levande testbädd för att iaktta hur hjärnans skyddsvägg sviktar under stress, med små genomskinliga fiskar istället för större däggdjur. Genom att följa hur högt blodsocker omformar kärlstruktur och funktion i realtid kan forskare snabbare peka ut vilka molekyler och celltyper som bör riktas för att hålla barriären intakt. I slutändan kan sådana insikter vägleda utvecklingen av nya läkemedel eller behandlingsstrategier för att förebygga eller minska vätskefläckage i ögon och hjärna—och därigenom bevara synen och skydda kognitiv funktion hos personer med diabetes och andra neurovaskulära sjukdomar.
Citering: Bakker-van Bugnum, N., Snijders, E.E., Hogendorp, E.F. et al. A zebrafish multimodal toolbox to study the blood-brain barrier in health and disease. Sci Rep 16, 9422 (2026). https://doi.org/10.1038/s41598-026-39616-y
Nyckelord: blod-hjärnbarriär, zebrafiskmodell, diabetiska komplikationer, kärl-läckage, neurovaskulär sjukdom