Clear Sky Science · sv
Genomisk och in vitro-karaktärisering av två lytiska bakteriofager som infekterar multiresistenta Erwinia sp. stam AnSW2-5
Varför bakterier som förstör grödor angår alla
Runt om i världen kämpar lantbrukare mot bakteriella sjukdomar som ruttnar frukter, får blad att vissna och förstör skördar. Många av dessa utbrott orsakas nu av stammar som inte längre svarar på vanliga antibiotika, vilket hotar såväl livsmedelsförsörjningen som de försörjningar som är beroende av den. Denna studie undersöker ett framväxande alternativ: att använda virus som angriper bakterier, så kallade bakteriofager, för att säkert oskadliggöra en särskilt seglivad växtpatogen som hittats i jord kopplad till hög antibiotikaanvändning.
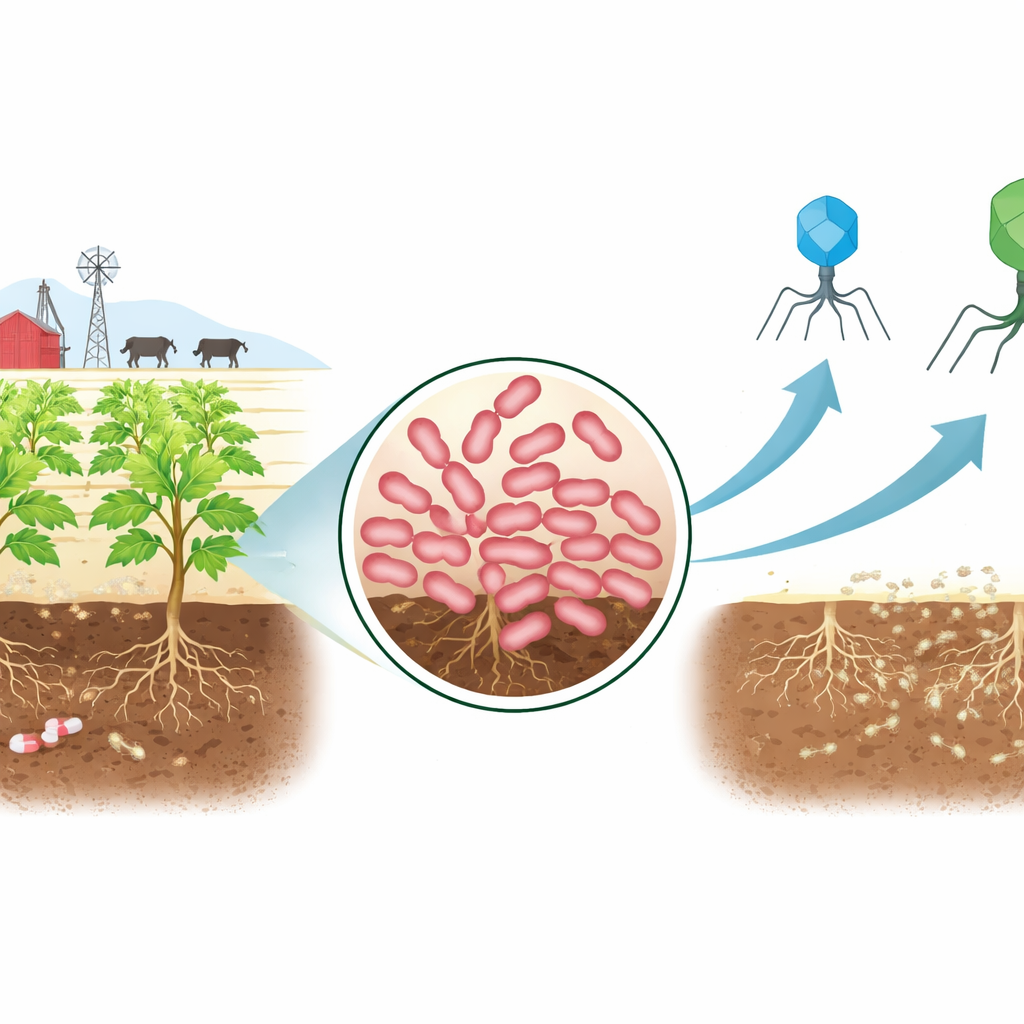
En hårdnackad ny inkräktare på gården
Forskarna började med att ta jordprov från en nöt- och kreatursinhägnad som var känd för att ta emot djurspillning och antibiotika. Från denna krävande miljö isolerade de en stam av Erwinia, en bakteriegrupp som inkluderar ökända orsaker till brandröta i äpplen och mjukröta i potatis. Tester visade att denna stam, kallad AnSW2-5, kunde stå emot flera stora antibiotikafamiljer, inklusive läkemedel som används mot ett brett spektrum av infektioner. Genetisk analys bekräftade varför: dess DNA bar på flera kända resistensgener och kraftfulla molekylära pumpar som aktivt pumpar ut antibiotika ur cellen. Samtidigt visade genomjämförelser att denna stam är skild från tidigare beskrivna Erwinia-arter, vilket gör den till en användbar modell för att studera hur man kan kontrollera nya, svårbehandlade växtpatogener.
Två små rovdjur med olika styrkor
För att hitta naturliga fiender till denna multiresistenta bakterie riktade teamet in sig på sötvatten från samma plats och berikade det för bakteriofager som kunde infektera AnSW2-5. De isolerade två lovande kandidater, betecknade P-A och P-K. I elektronmikroskopet framstod P-A som kompakt med en kort svans, en utformning som förknippas med snabb, direkt infektion. P-K, däremot, hade en längre, kontraktil svans med en komplex basstruktur, vilket tyder på ett mer kraftfullt sätt att borra sig in i värden. Sekvensering av deras genom visade att båda fagerna är strikt lytiska: de invaderar, replikerar och spränger cellen, i stället för att ligga tysta i bakteriens DNA. De gör detta med mycket olika genetiska verktyg—P-A:s strömlinjeformade genom stödjer snabb attack, medan P-K:s större genom kodar för mer invecklad struktur- och replikationsmaskineri.
Hur det virala laget angriper
När forskarna följde varje fags livscykel i laboratoriet fann de att P-A slår till snabbt: den behöver bara cirka 20 minuter innan nya viruspartiklar börjar dyka upp, och varje infekterad bakterie frigör omkring 70 avkommor. P-K tar längre tid—ungefär 35 minuter innan den börjar producera nya fager—men varje infekterad cell ger ungefär 110 nya partiklar. I kokulturtester där bakterier och fager växte tillsammans under tre dagar bromsade båda fagerna ensam bakterietillväxten men förhindrade den inte helt. Bakterierna återhämtade sig så småningom, vilket speglar framväxten av resistenta överlevare. När P-A och P-K däremot kombinerades i en cocktail reducerade de bakteriepopulationen med mer än 80 % och höll den undertryckt under hela den 72 timmar långa försöksperioden.
Hindra att resistens får fotfäste
Ett av de mest anmärkningsvärda fynden var hur fagparet påverkade uppkomsten av resistenta mutanter. När de utsattes för antingen P-A eller P-K var för sig lyckades en liten bråkdel av bakterierna—ungefär en på en miljon till en på tio miljoner—undkomma och växa trots fagattack. Men när båda fagerna användes tillsammans blev resistenta kolonier så sällsynta att de föll under försöksgränsen för upptäckt. Det tyder på att de två virusen sannolikt fäster vid olika mål på bakterieytan eller stör cellen på komplementära sätt. För att en enda bakterie ska överleva skulle den behöva övervinna båda samtidigt, en praktiskt taget osannolik händelse. I praktiska termer gör detta cocktailen mycket mer robust mot de evolutionära knep som ofta fäller antibiotika.
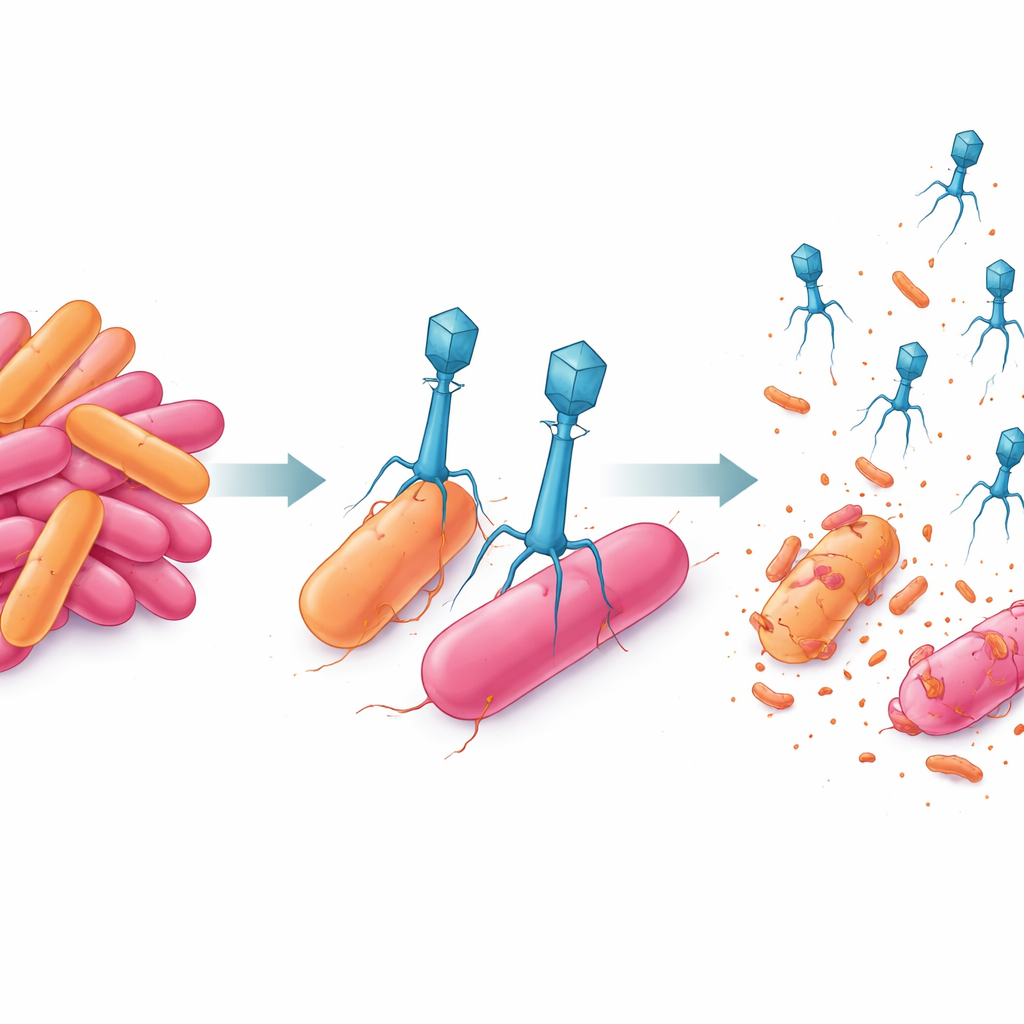
Vad detta kan betyda för framtida skördar
Tillsammans visar arbetet att noggrant utvalda par av bakteriofager kan göra mer än att bara sänka farliga växtbakterier—de kan också begränsa bakteriernas förmåga att utveckla resistens. Genom att kombinera en snabbverkande fag med en som producerar fler avkommor skapade forskarna ett viralt lag som höll en multiresistent Erwinia-stam i schack i flera dagar samtidigt som det förhindrade påvisbara undkommande varianter. Även om dessa försök utfördes i labb snarare än i fruktträdgårdar eller åkrar, pekar de mot en framtid där målinriktade fagblandningar blir en del av standardiserad integrerad bekämpning, vilket hjälper bönder att skydda grödor med avsevärt mindre beroende av traditionella antibiotika.
Citering: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Nyckelord: bakteriofag biokontroll, växtbakteriesjukdomar, antibiotikaresistens inom jordbruket, Erwinia-fagterapi, fagcocktails