Clear Sky Science · sv
Nya konjugat av benzimidazol-alkanosulfonat som kolinesterashämmare med in vitro- och in silico-validering
Varför denna forskning är viktig för minne och åldrande
Alzheimers sjukdom urholkar långsamt minnet, självständigheten och livskvaliteten för miljontals människor världen över, men dagens läkemedel lindrar mest symtom utan att bromsa den underliggande skadan. Denna studie undersöker en ny familj laboratorietillverkade molekyler utformade för att bättre skydda en nyckelhjärnkemikalie som är involverad i inlärning och minne, samtidigt som de bekämpar skadlig oxidativ stress. Genom att förena egenskaper från flera framgångsrika läkemedelstyper i en enda struktur syftar forskarna till att ta ett steg närmare mer effektiva behandlingar mot Alzheimers sjukdom.
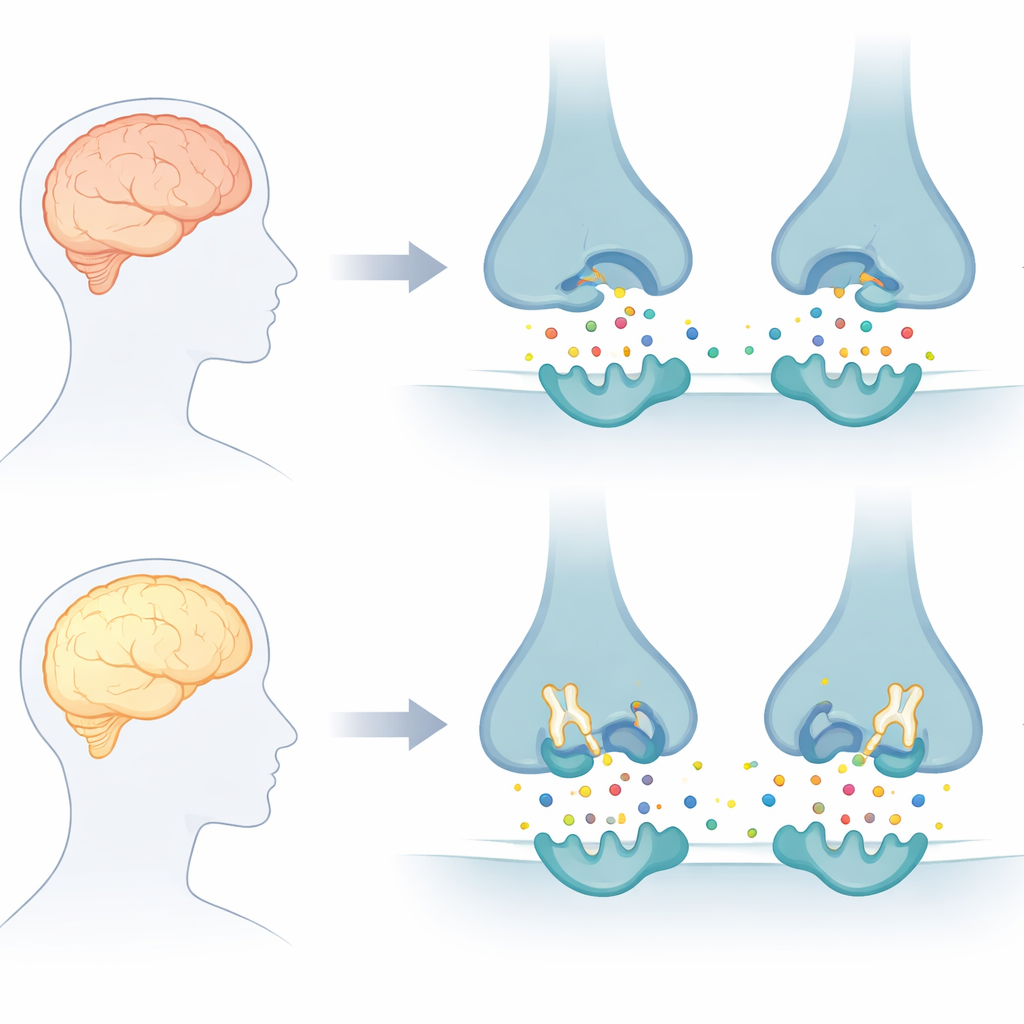
Hjärnsignalen som försvinner för fort
Friska hjärnceller kommunicerar med hjälp av kemiska budbärare, varav en av de viktigaste är acetylkolin. Vid Alzheimers sjukdom bryts acetylkolin ner för snabbt av två enzymer, acetylkolinesteras och butyrylkolinesteras, vilket bidrar till minnesförlust och förvirring. Nuvarande läkemedel blockerar huvudsakligen bara ett av dessa enzymer och endast under en begränsad tid, vilket är anledningen till att de ger kortsiktig symtomlindring snarare än långsiktigt skydd. Författarna till denna artikel fokuserade på att utforma ”dubbla” hämmare som skulle kunna rikta in sig på båda enzymerna samtidigt och potentiellt ge acetylkolin en bättre chans att utföra sitt arbete.
Bygga en smartare molekylär nyckel
För att skapa dessa dubbla hämmare använde teamet en strategi kallad molekylär hybridisering: de sammanfogade delar från tre typer av kemiska byggstenar som redan är kända för att interagera väl med kolinesterasenzym. Dessa delar inkluderade en benzimidazolring som ofta förekommer i läkemedel, en sulfonatgrupp som kan binda starkt i enzymfickor, och en hydrazonlänk som hjälper till att koppla ihop delarna på ett flexibelt sätt. Resultatet blev en serie besläktade föreningar, märkta 4a till 4r, vars strukturer noggrant bekräftades med standardkemiska tekniker såsom infraröd och kärnmagnetisk resonansspektroskopi.
Testning av enzymhämning och antioxidantkapacitet
De nya föreningarna screenades först i provrörsexperiment för att se hur väl de kunde bromsa de två kolinesterasenzymen. De flesta medlemmar i serien visade måttliga till starka hämmande effekter, men fem särskilt — kända som 4b, 4h, 4i, 4q och 4r — utmärkte sig för sin förmåga att hämma acetylkolinesteras. När forskarna mätte mer precisa potensvärden matchade flera av dessa molekyler eller överträffade till och med donepezil, ett av huvudläkemedlen som för närvarande ordineras för Alzheimer. Teamet undersökte också om de bästa enzymhämmarna kunde neutralisera fria radikaler, instabila molekyler som skadar hjärnceller. Föreningarna 4q och 4r visade särskilt stark antioxidantaktivitet i flera olika tester, och närmade sig eller överträffade referensantioxidanten vitamin C.
En titt in i enzymets lås
Eftersom dessa experiment utfördes utanför kroppen vände sig forskarna till datorbaserad modellering för att förutsäga hur molekylerna kan bete sig som läkemedel. Med hjälp av allmänt använda in silico-verktyg uppskattade de absorptions-, distributions- och metabolisegenskaper och simulerade sedan hur föreningarna skulle passa in i acetylkolinesteras tredimensionella struktur. Dockningsstudierna antydde att benzimidazolportionen av varje molekyl lägger sig nära enzymets yttre öppning, medan sulfonatbärande änden når djupt in i det katalytiska centrum där acetylkolin normalt bryts ner. Noterbart bildade 4q och 4r flera stabiliserande interaktioner inne i enzymfickan och visade högre beräknad bindingsstyrka än donepezil självt, vilket speglar deras starka prestation i provrörstesterna.
Vad detta betyder för framtida Alzheimerbehandlingar
Tillsammans visar fynden att denna nya klass av benzimidazol‑alkanosulfonatkonjugat kan kraftigt hämma acetylkolinesteras, uppvisa användbart antioxidativt beteende och binda till sitt enzymmål på ett sätt som är förenligt med nuvarande principer för läkemedelsdesign. Även om dessa molekyler är långt ifrån redo för användning hos patienter — de har ännu inte testats i djur eller människor — erbjuder de en lovande ritning för nästa generations Alzheimerbehandlingar som kombinerar enzymhämning med skydd mot oxidativ stress. Med vidare förfining och biologisk testning skulle några medlemmar av denna familj en dag kunna bidra till läkemedel som bättre bevarar minne och tänkande i den åldrande hjärnan.
Citering: Omar, M.A., Al-Ashmawy, A.A.K., Abd El Salam, H.A. et al. New benzimidazole-alkanesulfonate conjugates as cholinesterase inhibitors with in vitro and in silico validation. Sci Rep 16, 8946 (2026). https://doi.org/10.1038/s41598-026-39534-z
Nyckelord: Alzheimers sjukdom, acetylkolinesterashämmare, benzimidazolderivat, antioxidativa föreningar, läkemedelsdesign