Clear Sky Science · sv
Strukturell modellering och dockningsanalys av kanoniska och nya resistensassocierade missense-mutationer i sudanesiska Escherichia coli
Varför detta spelar roll för vardagshälsan
Antibiotikaresistenta infektioner är inte längre sällsynta medicinska kuriositeter; de hotar i ökande grad rutinbehandlingar för urinvägsinfektioner, kirurgi och intensivvård. Denna studie undersöker noggrant Escherichia coli‑bakterier från Sudan och ställer en mycket specifik fråga: hur förändrar små genetiska förändringar i bakteriella proteiner hur vanliga antibiotika verkar? Genom att använda datorbaserad strukturell modellering i stället för kostsamma laboratorieexperiment avslöjar författarna dolda resistensmönster som standardtester och globala databaser kan missa—särskilt i resursbegränsade miljöer där resistens ökar snabbast. 
En titt i bakteriernas verktygslåda
Forskarna fokuserade på så kallade ”missense”-mutationer—enstaka basbyten i DNA som byter ut en aminosyra i ett protein mot en annan. De analyserade helgenomsekvenser från 55 E. coli‑isolat insamlade i Sudan och zoomade in på bakteriella proteiner som är direkta måltavlor för stora antibiotikaklasser, inklusive fluorokinoloner, makrolider och rifampicin. Dessa mål inkluderar DNA‑vridande enzymer (gyras och topoisomeras IV), det proteintillverkande ribosomet och enzymet RNA‑polymeras. Av 71 mutationer som hittades i dessa proteiner flaggades 19 av flera prediktionsverktyg som sannolikt skadliga för proteinfunktionen, och anmärkningsvärt nog verkade de flesta av dessa vara nya variationer som ännu inte katalogiserats i globala resistensdatabaser.
Nya problemområden i välkända mål
Några av de viktigaste förändringarna samlades i ett ribosomalt protein kallat L22, som hjälper till att bilda den tunnel genom vilken nysyntetiserade proteiner lämnar ribosomet. Detta område fungerar också som en dockningsplats för makrolidantibiotika såsom erytromycin. Studien identifierade en tät samling tidigare ej rapporterade L22‑mutationer, många i samma stam, som ligger precis längs denna tunnel och vid kontaktpunkter med ribosomalt RNA. Beräkningsanalyser föreslog att flera av dessa förändringar destabiliserar den lokala strukturen eller gör den mer flexibel, vilket potentiellt omformar tunneln så att makrolidmolekyler passar mindre tätt. Samtidigt framträdde mer välkända ”kanoniska” resistensmutationer i DNA‑bearbetande proteiner ParC och ParE och i RNA‑polymeras, vilket bekräftar att sudanesiska stammar delar vissa globala resistensdragningskraftar samtidigt som de bär på sina egna lokala variationer.
Hur formförändringar försvagar antibiotikagreppet
Teamet gick bortom listor över sekvenser och undrade hur dessa mutationer skulle kunna ändra det tredimensionella samspelet mellan antibiotika och deras mål. Med molekylära dockningssimuleringar jämförde de hur olika läkemedel bundit till normala och muterade proteiner. För topoisomeras IV‑proteinet ParC försvagade nyckelmutationer nära läkemedelskontaktstället väsentligt den predikterade bindningen av fluorokinolonen trovafloxacin, vilket återspeglar ett lösare grepp vid enzym–DNA–läkemedels‑gränssnittet. I det närbesläktade proteinet ParE minskade mutationer måttligt bindningen av novobiocin. I kontrast verkade en ny mutation i gyrasproteinet GyrA destabiliserar enzymets struktur utan att märkbart ändra hur tätt fluorokinolonen moxifloxacin kunde binda, vilket antyder att resistens ibland kan uppstå genom subtila störningar av enzymets funktion snarare än genom att enkelt hålla bort läkemedlet. 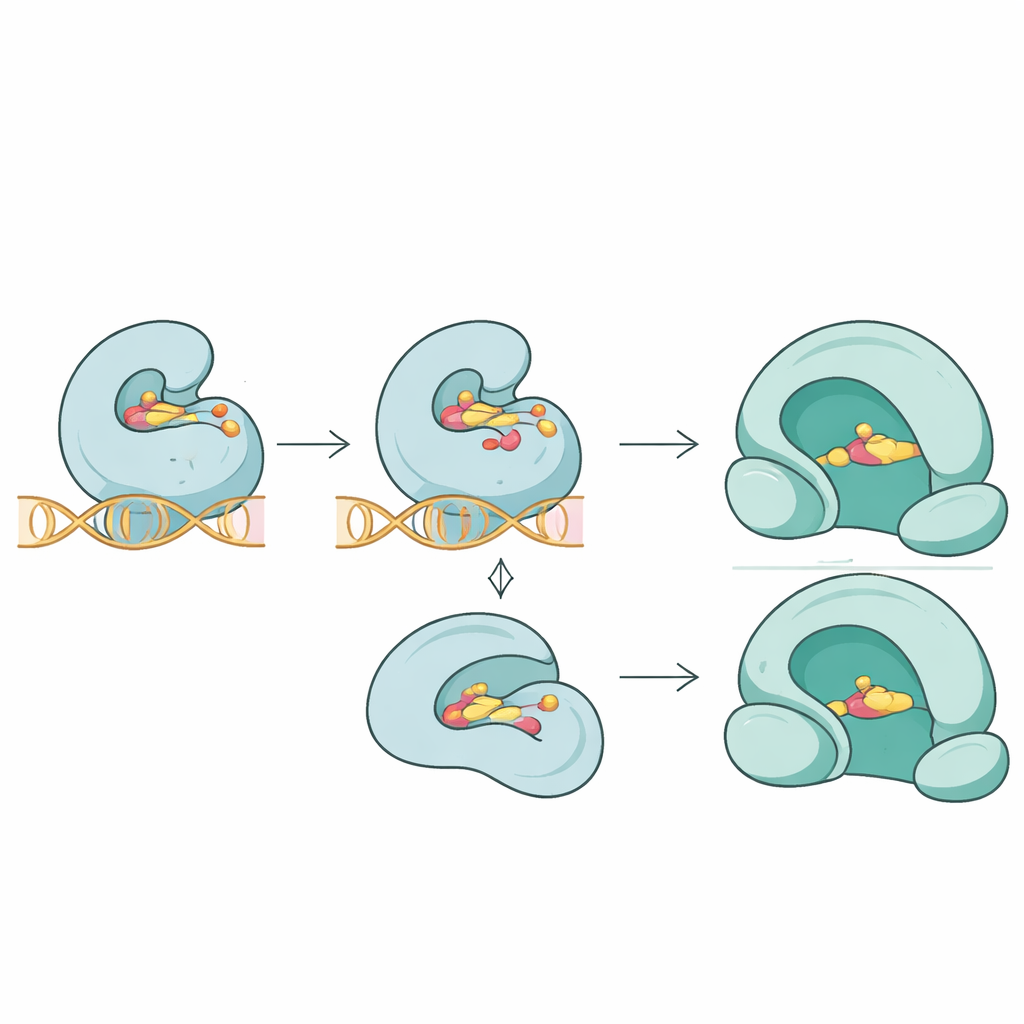
Blandade effekter på olika läkemedel
Alla mutationer påverkade inte läkemedelsbindningen på samma sätt. Klassiska rifampicin‑resistensförändringar i RNA‑polymerasproteinet RpoB störde i liten utsträckning bindningen av en nyare, strukturellt avvikande hämmare som riktar sig mot en närliggande plats, vilket tyder på att framtida läkemedel kan utformas för att kringgå befintliga resistensmönster. För ribosomproteinet L22 visade dockningsstudier med erytromycin ett lapptäcke av utfall: vissa mutationer försvagade bindningen, några hade liten effekt och en förbättrade till och med den predikterade passformen något. Dessa resultat understryker att resistens sällan är allt‑eller‑inget; istället skjutsar varje mutation proteinstabilitet, flexibilitet och läkemedelsbindning i olika riktningar, och den samlade effekten på behandling beror på hur dessa förändringar kombineras i en levande bakteriecell.
Vad detta betyder för patienter och övervakning
Ur ett lekmannaperspektiv är huvudbudskapet att bakterier i platser som Sudan utvecklar resistens både via välkända och mindre kända vägar. De välkända vägarna involverar klassiska mutationer som redan följs av internationella program, men denna studie visar att många ytterligare, lokalt förhöjda mutationer också kan försvaga antibiotika på mer subtila sätt. Genom att kartlägga dessa förändringar på detaljerade proteinstrukturer ger författarna en prioriterad lista över mutationer som bör testas i laboratoriet och beaktas i regionala diagnostiska paneler. I praktiska termer argumenterar deras arbete för att smart datorbaserad modellering kan hjälpa länder med begränsad laboratoriekapacitet att bättre hålla koll på framväxande resistens, vilket i slutändan stöder mer tillförlitliga behandlingsval och inspirerar till läkemedelsdesigner som ligger ett steg före bakterieevolutionen.
Citering: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Nyckelord: antimikrobiell resistens, Escherichia coli, missense-mutationer, strukturell bioinformatik, Sudan