Clear Sky Science · sv
Omfattande prestandautvärdering av BMIA-12, ett system för kvantifiering av benmärgsceller i normala och hematologiska malignitetsprover
Varför det är viktigt att räkna benmärgsceller
När läkare diagnostiserar blodcancer som leukemi eller multipelt myelom undersöker de noggrant benmärgsutstryk i mikroskop och räknar tusentals celler för hand. Detta långsamma, noggranna arbete påverkar livsavgörande beslut om diagnos, behandling och prognos. Artikeln presenterar och rigoröst testar ett nytt artificiellt intelligenssystem, BMIA-12A, utformat för att automatisera stora delar av denna räkning — vilket potentiellt kan ge snabbare, mer konsekventa resultat och göra dem mindre beroende av den enskilda experten som läser preparatet.
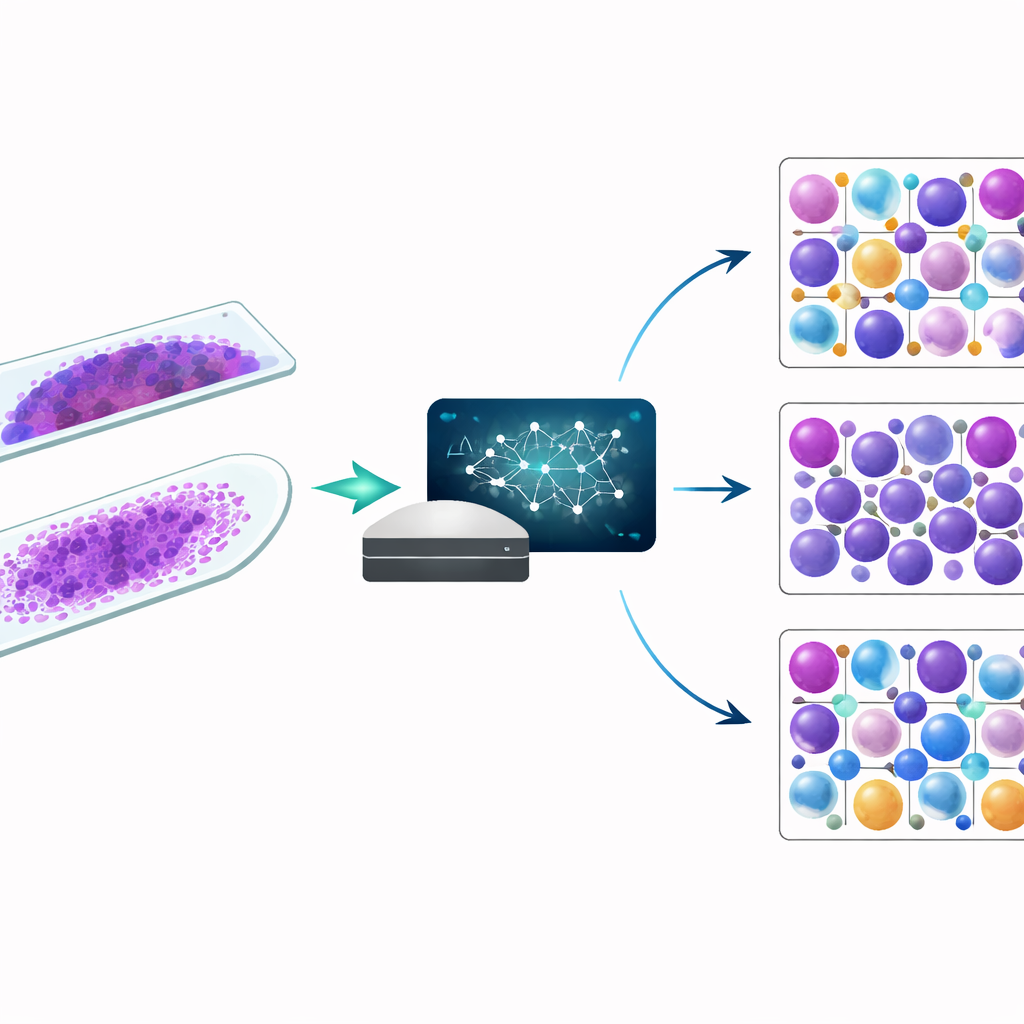
En ny digital hjälp för mikroskopet
BMIA-12A-systemet tar digitaliserade bilder av benmärgsutstryk och använder djupinlärningsalgoritmer för att känna igen och kategorisera celler i 16 huvudtyper, inklusive tidiga “blast”-celler som hjälper till att definiera leukemier och plasmaceller som är centrala vid multipelt myelom. I denna studie analyserade forskarna 298 benmärgsutstryk från 149 personer, som täcker normala prover, plasmacellsrubbningar och flera former av akut leukemi. För varje utstryk jämfördes tre tillvägagångssätt: helt automatiska AI-räkningar, AI-räkningar granskade och korrigerade av specialister, samt traditionell manuell räkning med ljusmikroskop. De undersökte också två vanliga prepareringstekniker, så kallade wedge- och squash-utstryk, för att se hur preparatkvalitet påverkar AI-prestanda.
Hur väl systemet känner igen normala celler
I benmärg från personer utan malignitet presterade AI-systemet imponerande väl. Det klassificerade korrekt cirka 95 % av nästan 38 000 celler i både wedge- och squash-preparat, med 14 av 16 celltyper som hade återkallning över 90 %. Wedge-preparat — där provet jämnt sprids över glaset — gav något bättre precision för nyckelceller av diagnostiskt intresse såsom plasmaceller, blastceller och sällsynta basofiler. De flesta av AI:ns fel uppstod mellan celltyper som ser mycket lika ut, såsom närliggande stadier av vita blodkroppars mognad eller reaktiva lymfocyter som liknar blastceller. När forskarna jämförde hur ofta varje celltyp förekom i hela prover matchade AI- och expertgranskade resultat varandra väl, medan traditionella manuella räkningar var märkbart mer varierande, vilket speglar subjektivitet och begränsad provtagning vid manuell räkning.
Vad som händer vid myelom och leukemi
Systemets prestation i sjukdomstillstånd var mer blandad. Vid plasmacellsrubbningar var AI mycket precis när det gällde att identifiera plasmaceller men missade ungefär en fjärdedel av dem, särskilt vid multipelt myelom där märgen är fylld av abnorma plasmaceller som skiljer sig i form från de läroboksexempel som användes för träning. Som ett resultat tenderade AI att underskatta plasmacellsandelarna jämfört med manuella och expertkorrigerade räkningar, särskilt när tumörbördan var hög. Ett liknande mönster syntes vid akuta leukemier: AI var övergripande bra på att upptäcka blastceller, särskilt på wedge-preparat, men den placerade ofta atypiska blastceller i liknande kategorier såsom monocyter eller tidiga myeloida celler. Manuella räkningar visade konsekvent högre blastprocent än både automatiska och expertgranskade digitala resultat, med de största skillnaderna i vissa genetiska undertyper som AML med NPM1-mutation och B-cells ALL med BCR::ABL1-fusionen, där blastmorfologin är särskilt ovanlig.
Varför preparering och genetik spelar roll
Studien visade att både hur utstryket görs och sjukdomens underliggande genetik påverkar AI-prestanda. Squash-utstryk, där märgfragment försiktigt komprimeras mellan glas, introducerade distorsioner som suddade ut fina nukleära detaljer och ökade förväxlingen mellan intilliggande mognadsstadier samt mellan blastceller och andra unga celler. Wedge-utstryk bevarade strukturen bättre och gav högre återkallning och precision, så författarna rekommenderar dem som standardformat för AI-assisterad analys. På biologins sida har blastceller från specifika genetiska undertyper ofta distinkta, ibland deformerade nukleära former eller andra atypiska egenskaper. Eftersom nuvarande AI-system vanligtvis tränas främst på normala celler kan dessa neoplastiska varianter tvingas in i den "närmsta" normala kategorin, vilket leder till systematisk underskattning av sjukdomsbördan just hos de patienter där korrekta gränsvärden är mest kritiska.
Hur detta förändrar laboratoriet i dag
Sammantaget tyder resultaten på att BMIA-12A redan är tillräckligt pålitligt för att fungera som ett kraftfullt screening- och triageverktyg, särskilt för normala benmärgsprover och rutinmässiga differentialräkningar. Det kan snabbt granska tiotusentals celler per preparat och levererar stabila, reproducerbara resultat som stämmer väl överens med expertgranskning. De tydliga och ibland stora avvikelserna gentemot manuella räkningar vid leukemier och plasmacellssjukdomar visar dock att mänskliga specialister förblir nödvändiga för slutlig tolkning, särskilt i närheten av diagnostiska gränsvärden och i genetiskt definierade högrisksubtyper. Författarna menar att laboratorier som inför sådana AI-verktyg måste validera dem noggrant för sina egna prepareringsmetoder och bygga arbetsflöden där AI tillhandahåller en objektiv bas som experter förfinar, snarare än en ersättning för expertbedömning.
Citering: Kim, H.N., Lee, J.H., Jung, Y. et al. Comprehensive performance assessment of the BMIA-12 a system for bone marrow cell quantification in normal and hematological malignancy samples. Sci Rep 16, 8798 (2026). https://doi.org/10.1038/s41598-026-39443-1
Nyckelord: artificiell intelligens inom hematologi, benmärgscytologi, leukemidiagnostik, multipelt myelom, digital mikroskopi