Clear Sky Science · sv
Upptäckt av potentiella antivirala föreningar och påskyndande av terapeutisk upptäckt mot apkoppsvirus
Varför denna forskning är viktig nu
Apkoppor, numera ofta kallat mpox, har gått från att vara en sällsynt tropisk infektion till en global angelägenhet, med utbrott rapporterade på flera kontinenter under de senaste åren. Till skillnad från COVID-19 finns det fortfarande inget läkemedel som specifikt har tagits fram för att stoppa detta virus. Den här studien använder avancerade datorverktyg för att söka efter nya små molekyler som kan stänga av viruset där det gör mest skada: dess förmåga att gömma sig för vårt immunsystem. Om dessa kandidatföreningar bekräftas i laboratoriet kan de bli startpunkten för en ny klass av antivirala läkemedel.
Hur viruset gömmer sig från våra försvar
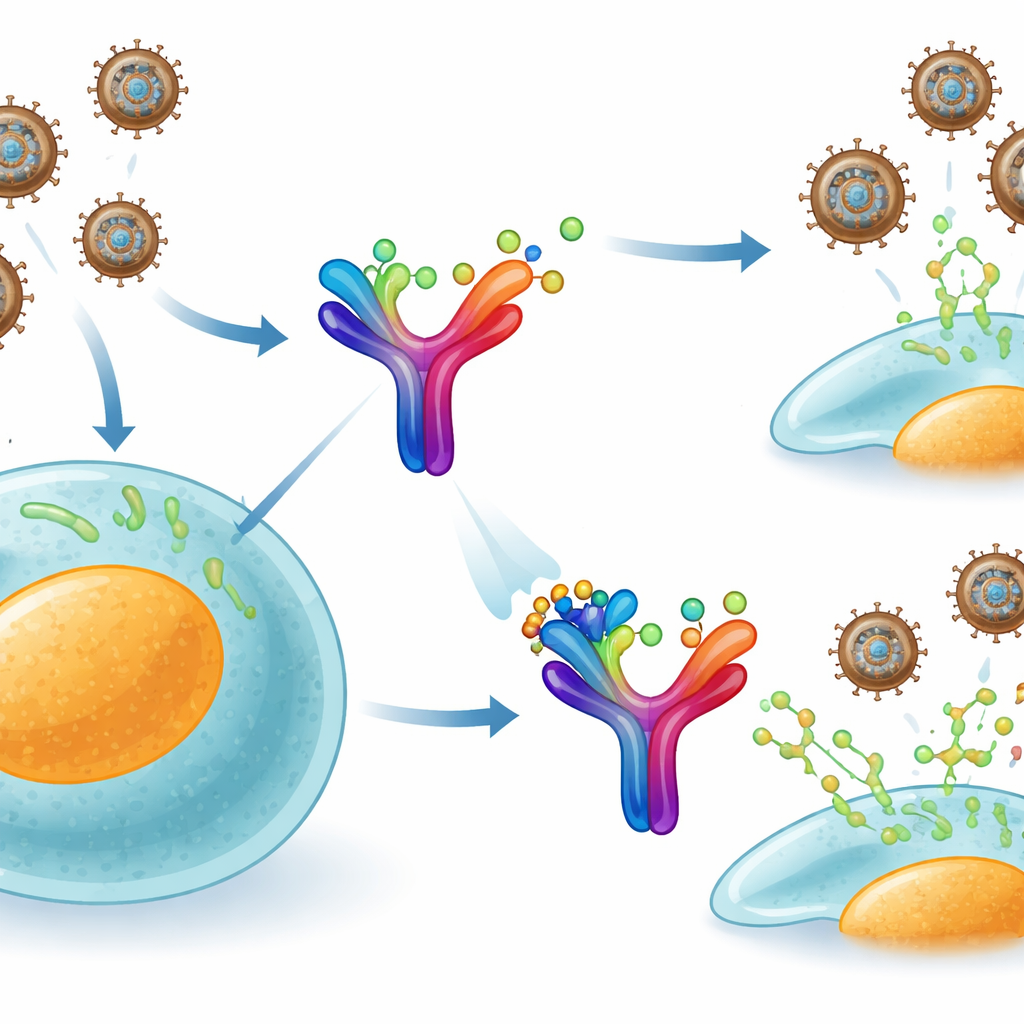
Apkoppor tillhör samma bredare familj som smittkoppor och använder ett smart trick för att undkomma immunsystemet. Våra celler frisätter ett signalprotein som kallas interferon-gamma, vilket normalt varnar närliggande celler och aktiverar antivirala försvar. Viruset producerar dock sitt eget sekretoriska protein, kallat B8R, som flyter utanför infekterade celler. B8R liknar i hög grad vår egen interferon-gamma-receptor och fångar upp dessa immunsignaler innan de når sitt verkliga mål. I praktiken fungerar det som en svamp som suger upp kroppens varningssignaler och förhindrar ett fullständigt antiviralt svar.
Använda datorer för att designa smartare behandlingar
Traditionell läkemedelsupptäckt kan ta många år och kräva enorma resurser. Här vänder sig forskarna till datorstödd läkemedelsdesign för att påskynda processen. Eftersom ingen experimentell 3D-struktur av B8R-proteinet finns tillgänglig använde de först AlphaFold-baserade verktyg för att förutsäga dess atomära form och kontrollerade noggrant kvaliteten på den modellen. Med en tillförlitlig 3D-struktur i hand genomförde de en virtuell screening av ett kemiskt bibliotek med 5000 små molekyler. Regler som beskriver vad som vanligtvis gör ett läkemedel tablettlikt (såsom storlek, form och löslighet) användes för att filtrera bort svaga kandidater, vilket lämnade 2890 lovande föreningar för detaljerade tester mot B8R-protmodellen.
Att hitta en lovande kemisk ”nyckel”
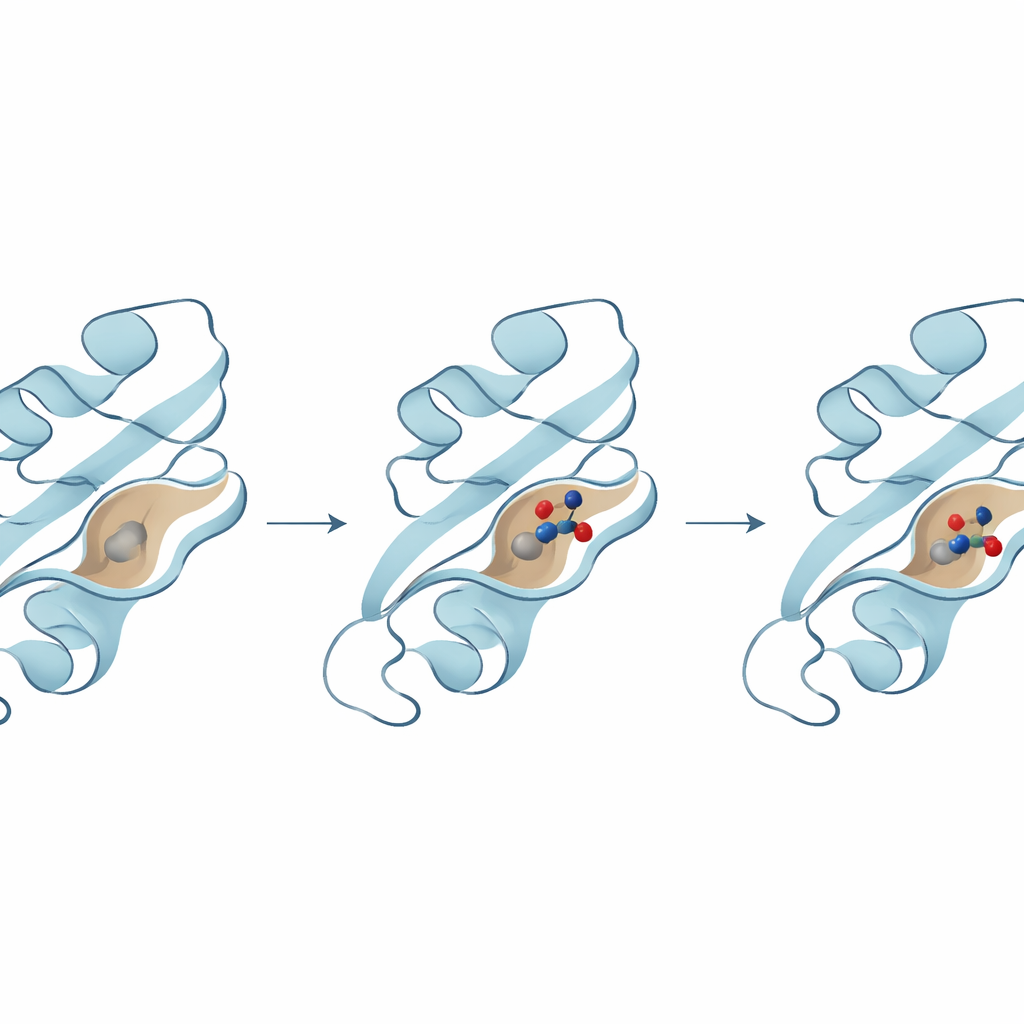
Nästa steg var att se vilka molekyler som kunde passa prydligt in i en viktig ficka på B8R-ytan, där den normalt interagerar med interferon-gamma. Teamet använde molekylär dockning, en teknik som provar miljarder möjliga poser för en molekyl i proteinets ficka och poängsätter hur tätt den skulle binda. Tre toppkandidater framträdde, var och en förutsagd att bilda starka interaktioner med nyckelaminosyror i fickan. En förening i synnerhet visade den starkaste bindningsenergin och skapade flera stabiliserande kontakter med kritiska rester som hjälper till att förankra den på plats, vilket tyder på att den kan vara särskilt effektiv för att blockera B8R:s aktivitet.
Att se molekyler röra sig över tid
Proteiner och läkemedelsmolekyler är inte styva; de rör sig, flexar och ”andas” i ett vattnigt omgivningsskikt. För att fånga detta körde forskarna långa molekylär-dynamik-simuleringar—virtuella filmer som varade hundratals nanosekunder—för att se hur varje protein–föreningspar uppträdde över tid. Dessa simuleringar visade att den bäst presterande föreningen förblev djupt begravd i B8R-fickan, med proteinet som anpassade sig något runt den samtidigt som det förblev strukturellt stabilt. Däremot vandrade de andra två föreningarna mer, skiftade in i alternativa fickor eller visade större fluktuationer, vilket tyder på svagare eller mindre tillförlitlig bindning. Ytterligare analyser av flexibilitet, energi och storskaliga rörelser pekade alla på samma vinnare: en förening som konsekvent gav den mest stabila och energimässigt fördelaktiga komplexbildningen.
Vad detta kan innebära för framtida behandlingar
Studien gör inte anspråk på att ha upptäckt ett färdigt läkemedel, och inga experiment i celler eller djur har ännu utförts. Istället levererar den en stark, databaserad startpunkt: en specifik småmolekyl som verkar vara idealiskt formad för att låsa fast sig i apkoppsproteinets B8R och potentiellt återställa kroppens interferon-alarm. Genom att rikta in sig på virusets immundräneringsstrategi snarare än dess replikationsmaskineri erbjuder detta tillvägagångssätt en ny vinkel för antiviral terapi. Författarna menar att deras ledande förening nu bör testas i laboratoriet, där dess förmåga att blockera B8R och dämpa mpox-infektion kan mätas direkt. Om dessa tester lyckas kan det bana väg för en riktad behandling som hjälper immunsystemet att se och stoppa viruset mer effektivt.
Citering: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Nyckelord: apkopps antiviral, immunsystemets undvikande, läkemedelsupptäckt, beräkningsmodellering, interferon-signalering