Clear Sky Science · sv
Optimering av THP-1-CAR-monocyter med CD32a-signalering för fagocytos och antigen‑specifik T‑cellsaktivering
Lära immunsystemet nya trick
Moderna cellterapier omprogrammerar redan immunceller för att jaga upp cancer, men de flesta bygger på T‑celler som kan ha svårt i den hårda miljön i solida tumörer. Den här studien vänder sig i stället till en annan kraftfull försvarare — makrofager, kroppens professionella ”ätare” — och frågar hur de kan omkopplas så att de inte bara slukar skadliga celler eller virus mer effektivt, utan också rekryterar T‑celler för en mer bestående och riktad attack. Arbetet avslöjar designregler för att bygga bättre chimeriska antigenreceptor (CAR)‑makrofager som kan användas både mot infektioner som COVID‑19 och svårbehandlade solida tumörer.
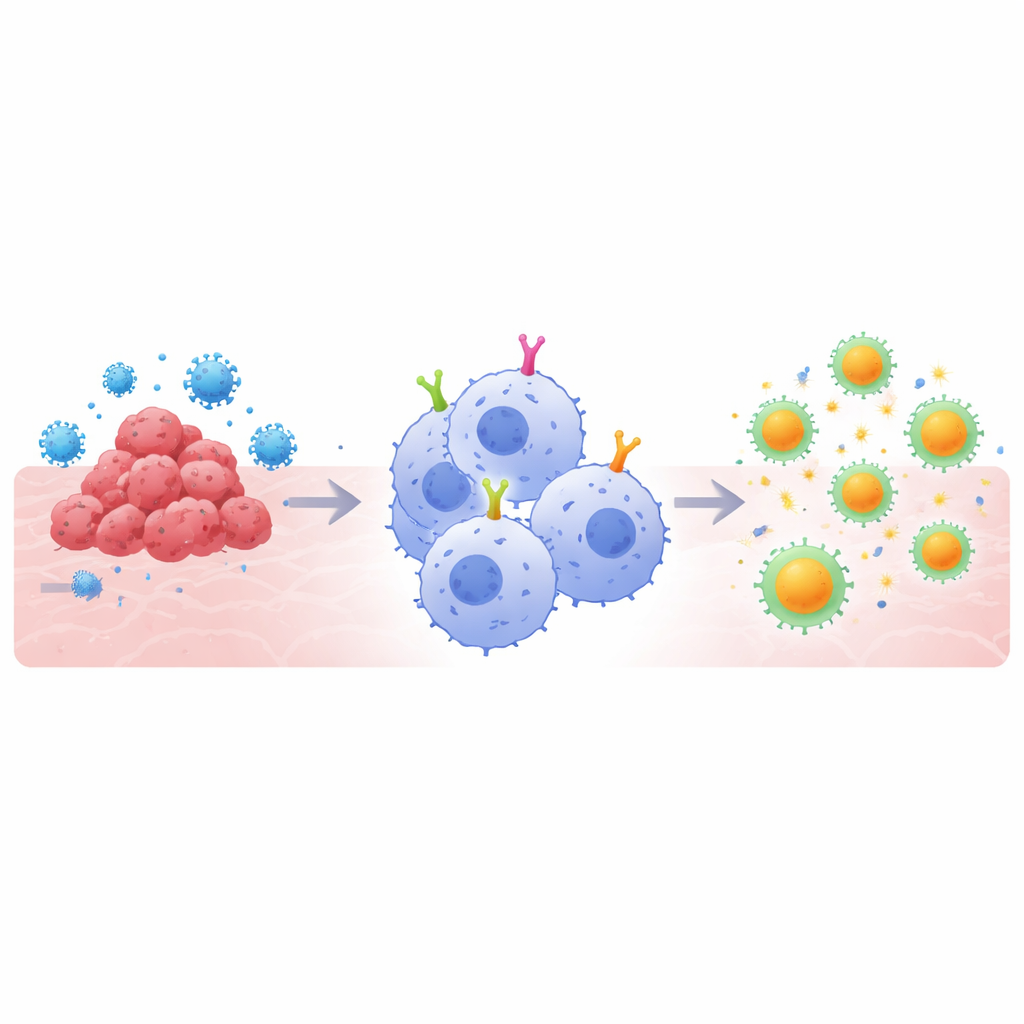
Varför super‑ätarceller spelar roll
CAR‑baserade terapier fungerar genom att utrusta immunceller med skräddarsydda ytreceptorer som känner igen ett valt mål, till exempel ett tumörprotein eller ett viralt spikprotein. T‑cellsvarianter har revolutionerat behandlingen av vissa blodcancerformer, men de stöter på hinder mot solida tumörer och vid vissa infektioner. Makrofager erbjuder en annan vinkel: de omsluter hot naturligt och finfördelar dem så att bitarna kan visas upp för T‑celler, vilket länkar det ”medfödda” och det ”adaptiva” immunsvaret. De flesta CAR‑designer byggdes dock ursprungligen för T‑celler, inte makrofager. Författarna resonerade att för att utnyttja makrofagernas styrkor fullt ut måste de interna signaldelarna i CAR‑erna — segmenten som talar om för cellen vad den ska göra när ett mål är bundet — skräddarsys specifikt för dessa ätarceller.
Att hitta bästa interna kopplingen
Teamet jämförde systematiskt flera interna signaldomäner i CAR:er införda i en mänsklig monocytcellinje (THP‑1) som kan omvandlas till makrofager. De fokuserade på domäner hämtade från receptorer som normalt driver fagocytos och inflammation: CD3ζ (den klassiska T‑cellsmodulen), CD32a (en receptor som binder antikroppsbelagda mål), CR3‑komponenterna CD11b och CD18 (centrala komplementreceptorer) och TLR4 (en sensor för mikrobiell fara). Med hjälp av pärlor och pseudovirus belagda med SARS‑CoV‑2‑spikprotein mätte de hur väl varje CAR‑design möjliggjorde att celler omslöt mål, producerade inflammatoriska molekyler och därefter aktiverade mänskliga CD8‑T‑celler som tidigare exponerats för viruset. De förde sedan över de mest lovande designerna till CAR:er som riktar sig mot mesothelin, ett protein som överproduceras i många solida tumörer, för att se om samma principer gällde i en cancerkontext.
Bygga bättre ätare och signalhöjare
En tydlig bild framträdde: CAR:er baserade på CD32a drev konsekvent starkare och snabbare fagocytos än de som använde den konventionella CD3ζ‑domänen, trots att CD3ζ innehöll fler av de vanliga aktiveringsmotiven. Med andra ord spelade ”passformen” mellan signalen och makrofagernas maskineri större roll än ren signalstyrka. Att lägga till CR3‑deriverade delar (CD11b eller CD18) ovanpå CD32a ökade inte ätkapaciteten under de flesta förhållanden, men det ökade nivåerna av viktiga inflammatoriska cytokiner såsom TNF‑α och IL‑1β. Kombinationer som innehöll TLR4 gick ännu längre i att förstärka inflammatoriska signaler och ytmärket CD86, vilket är kopplat till förmågan att stimulera T‑celler, även om detta kom med avvägningar: lägre CAR‑nivåer på cellytan och något minskad fagocytos.
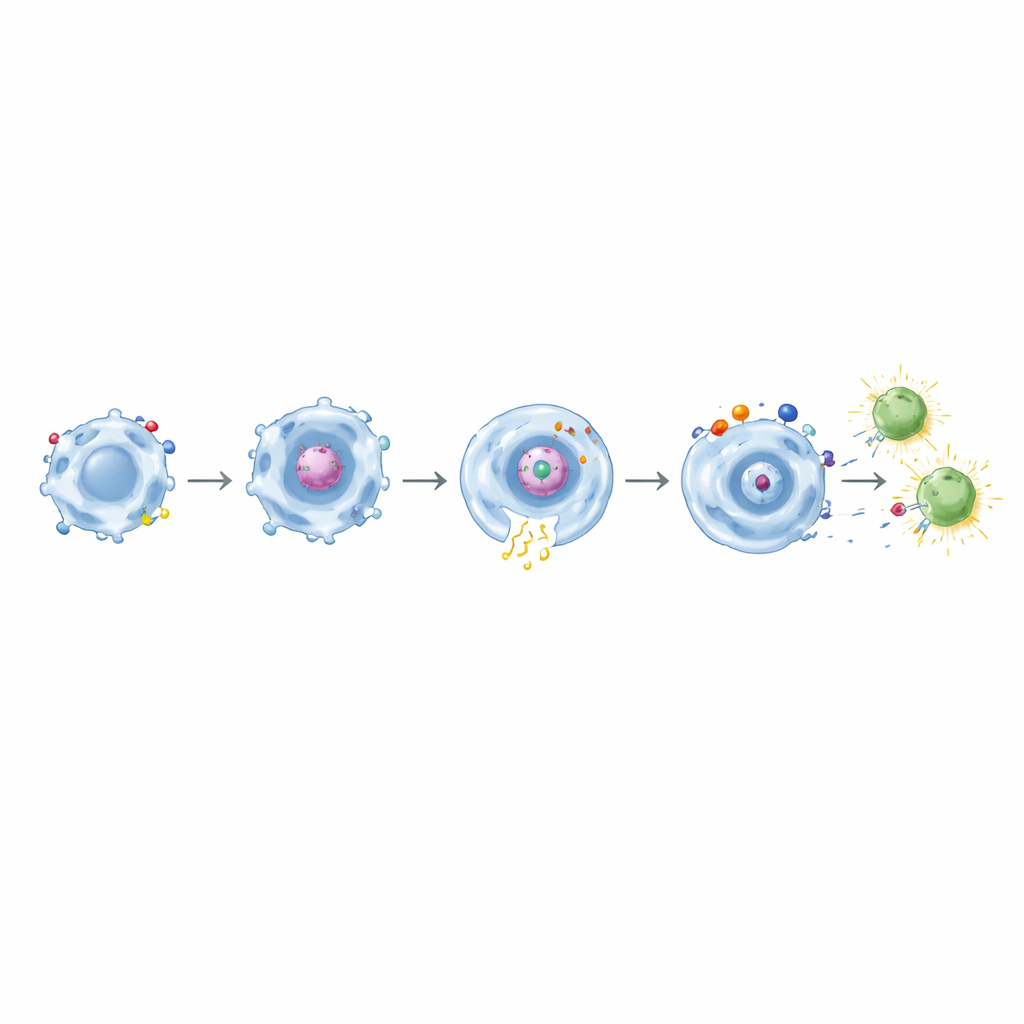
Från att äta till att lära T‑celler
Avgörande var att makrofager bärare av CD32a‑baserade CAR:er, efter att ha fagocyterat spikprotein, kunde aktivera minnes‑CD8‑T‑celler från personer som tidigare vaccinerats mot COVID‑19. Dessa T‑celler uttryckte tidiga aktiveringsmarkörer och producerade effektormolekyler såsom interferon‑γ och TNF‑α. Effekten blev ännu starkare med dubbeldomäns‑CAR:er som parede CD32a med CD11b, CD18 eller TLR4. När liknande designer riktade mot mesothelin testades mot konstruerade tumörceller visade de återigen precis, målberoende fagocytos kombinerad med förhöjd inflammatorisk signalering. Bland dessa utmärkte sig CD32a+TLR4‑kombinationen som ett kraftfullt ”vävnadsalarm”, som mest effektivt ökade cytokinutsöndring och CD86 samtidigt som den bibehöll specifik tumörfagocytos.
Vad detta kan betyda för framtida behandlingar
För en lekmannabetraktare visar studien att programmering av makrofager inte är ett universallösningsproblem. Genom att byta ut och kombinera interna signalmoduler kan forskare skulptera celler som antingen fokuserar på effektiv rensning av sjuka celler eller agerar mer som immunsignalförstärkare som omformar en tumörs undertryckande miljö och rekryterar T‑celler. CD32a‑baserade CAR:er framstod som en stark grund för sådana designer, och överträffade traditionella T‑cellsmoduler i makrofager och fungerade mot både virus‑ och tumörmål. Fastän dessa resultat kommer från laboratoriemodeller och måste bekräftas i primära humana celler och djur, ger de en ritning för nästa generations CAR‑makrofagterapier som bättre kan ta itu med solida tumörer och persistenta infektioner genom att förena snabb fagocytos med precis T‑cellsaktivering.
Citering: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Nyckelord: CAR‑makrofager, CD32a‑signalering, fagocytos, immunterapi mot solida tumörer, T‑cellsaktivering