Clear Sky Science · sv
Mikrobiologisk och reologisk dynamik i blandade biofilmer bildade av bakterier och eukaryotiska virus
Dolda samhällen på sjukhusutrustning
Många sjukhusinfektioner börjar inte med en enda mikrob, utan med slemmiga, osynliga samhällen kallade biofilmer som täcker katetrar och annan medicinsk utrustning. Denna studie ställer en förbisedda fråga med stora konsekvenser för patientsäkerheten: vad händer när inte bara bakterier utan också virus som smittar människor flyttar in i dessa biofilmer samtidigt? Genom att följa hur ett vanligt däggdjursvirus beter sig inne i bakteriella biofilmer visar forskarna hur dessa klibbiga mikrobstäder tyst kan skydda virus och ändra deras beteende.
Klibbiga mikrostäder
Biofilmer är som mikroskopiska städer byggda av mikrober på våta ytor—rör, stenar, tänder eller plastslangar som sätts in i patienter. Bakterier slår sig ner, förökar sig och utsöndrar en limliknande matris som skyddar dem mot uttorkning, kemikalier och immunsystemet. På sjukhus bildas sådana biofilmer ofta på urin- och intravenösa katetrar, där de kan så småningom leda till blodbanespridning och urinvägsinfektioner som är svåra att behandla. Dessa biofilmer innehåller ofta många olika arter och till och med olika livsriken, men de flesta studier har fokuserat på bakterier ensamma och lämnat virusens roll i stort sett outforskad.
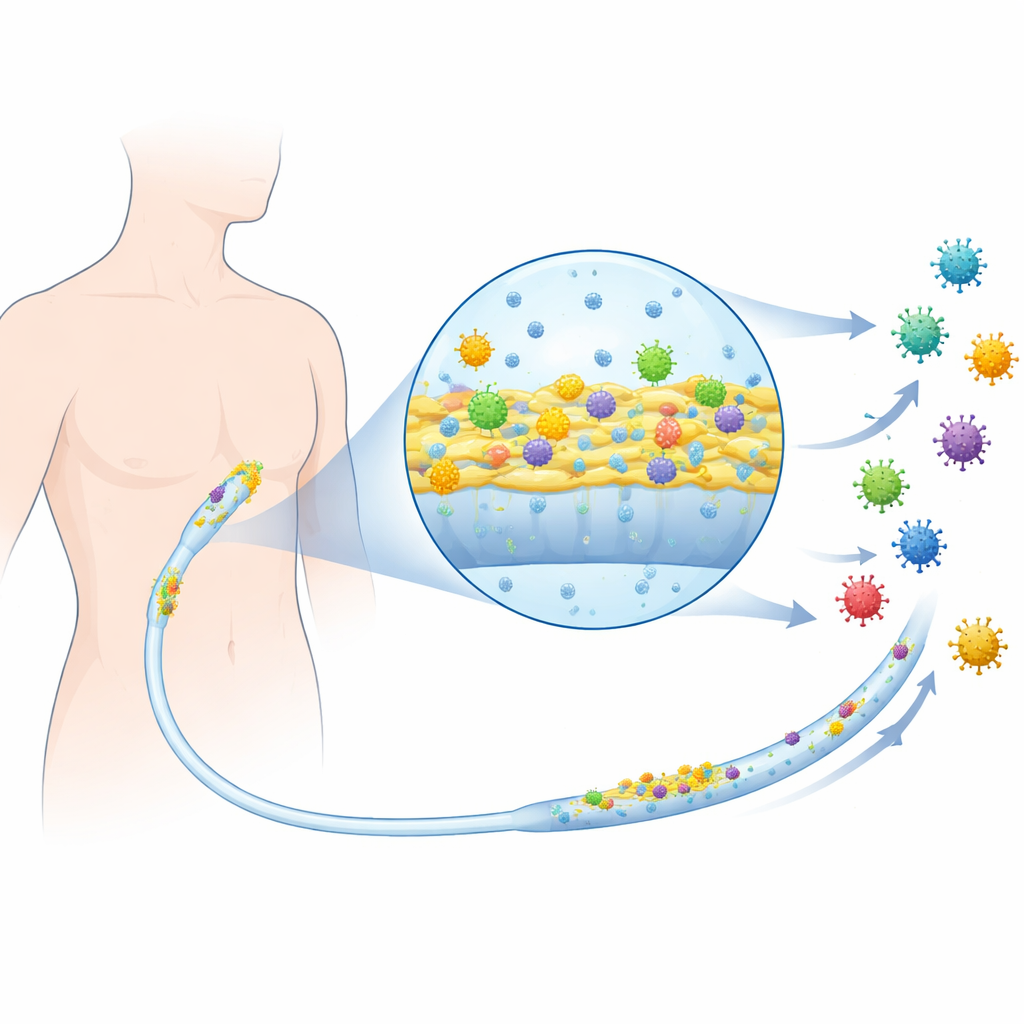
Att föra in ett däggdjursvirus i blandningen
Forskargruppen arbetade med kliniska bakteriella stammar som är kända för att kolonisera katetrar, inklusive uropatogen Escherichia coli från urinvägsinfektioner och andra bakterier som ofta påträffas vid central line-infektioner. De introducerade därefter däggdjursreovirus, ett välstuderat, icke-inkapslat virus som infekterar djurceller, som en modell för virus som infekterar människor mer generellt. Först kontrollerade de om tillsats av virusinnehållande material påverkade normalt, fritt svävande bakteriellt tillväxt. Över många stammar växte och överlevde bakterierna lika bra med eller utan virus, vilket visade att viruset inte direkt dödade bakterierna eller fungerade som ett antibiotikum.
Biofilmer ändrar känsla, inte storlek
När bakterierna slog sig ner i biofilmer blev bilden mer nyanserad. För de flesta stammar förändrades inte den totala mängden biofilm—mätt med en standardfärgning som kvantifierar hur mycket material som täcker en yta—i närvaro av virus. Några stammar producerade dock något mer eller mindre biofilm beroende på om viruspreparat fanns närvarande, vilket antyder stamberoende effekter. För att gå bortom enkel kvantitet lånade forskarna verktyg från materialvetenskap och mätte hur "mjuk" eller "styv" varje biofilm var, ungefär som att undersöka texturen hos en gel. De fann att varje bakteriestam bildade ett eget mekaniskt signum. Viktigt var att tillsats av virus antingen kunde göra dessa biofilmer styvare eller mjukare beroende på stammen: i en E. coli-stam gjorde viruset matrisen mer rigid, medan i en Staphylococcus epidermidis-stam ledde viruset till en svagare, mer följsam struktur.
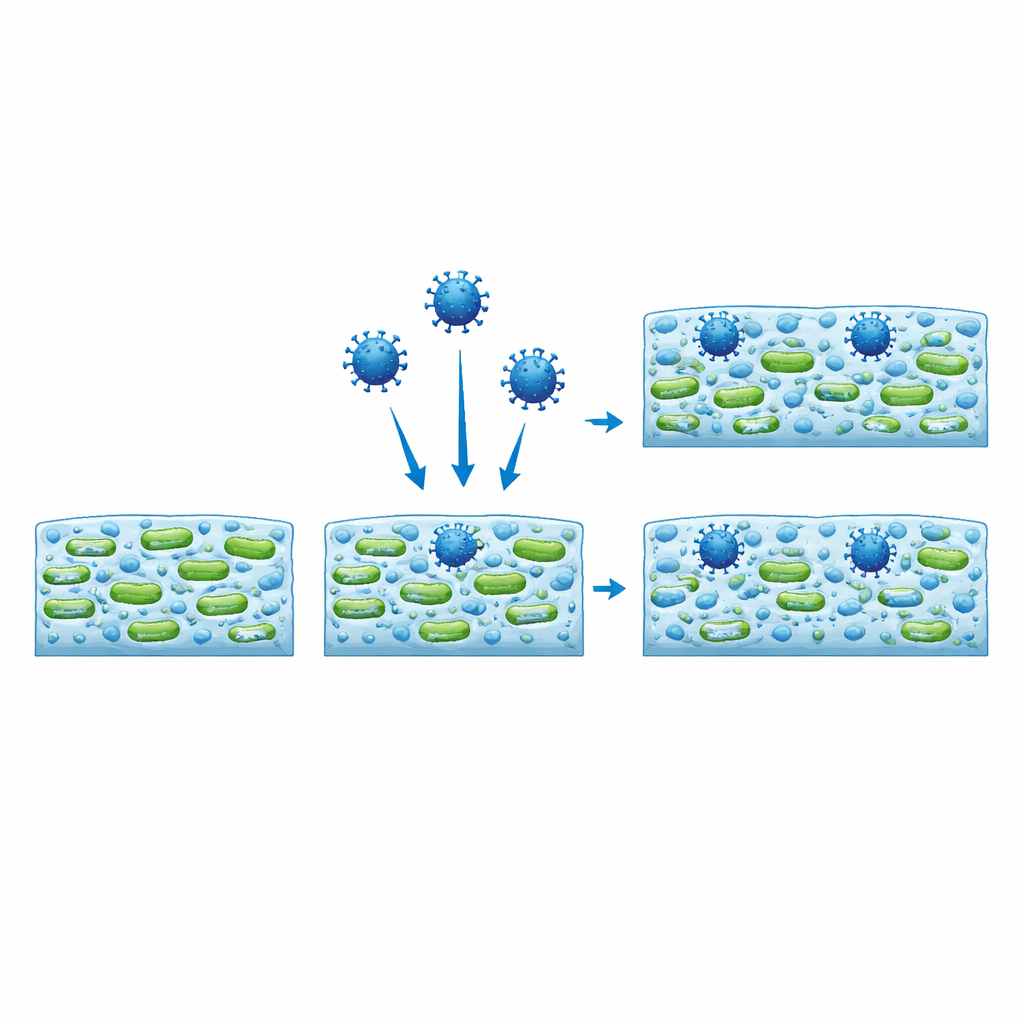
Virus hittar skydd och behåller sin smittkraft
Med fluorescensmikroskopi märkte forskarna upp viruspartiklarna så att de skulle lysa och följde var de hamnade inne i biofilmen. Till skillnad från inert plastpärlor av liknande storlek, som mest stannade i glesa områden och spolades bort, trängde virusen djupt in i matrisen och tenderade att klustra där bakteriecellerna var tätast. I vissa fall förändrade virusets närvaro till och med biofilmens övergripande form, och förvandlade kompakta klumpar till mer nätliknande strukturer eller vice versa, återigen beroende på bakteriestammen. För att testa om dessa fängslade virus fortfarande var farliga återvann författarna dem från biofilmerna och exponerade dem för däggdjursceller. De återvunna virusen förblev infektiösa, trots att de varit inbäddade i det bakteriella slemmet i två dagar.
Varför detta spelar roll för patienter och vidare
För en lekmannanotering är huvudbudskapet att biofilmer på medicinska enheter inte bara kan skydda bakterier från behandling—de kan också dölja och bevara virus som infekterar människa eller djurceller. Studien visar att virus kan inta plats i den bakteriella matrisen, subtilt förändra biofilmens struktur samtidigt som de förblir fullt kapabla att infektera nya celler när de frigörs. Detta antyder att katetrar och andra ytor täckta av biofilmer kan fungera som tysta reservoarer där virus kan bestå, skyddade från uttorkning, desinfektionsmedel och immunsvar. Att förstå dessa blandade mikrobiella samhällen kan vara avgörande för att utforma bättre material, rengöringsstrategier och behandlingsmetoder som riktar sig mot både bakterie- och viruspartners för att minska envisa, enhetsassocierade infektioner.
Citering: Gao, J., Abriat, C., Laekas-Hameder, M. et al. Microbiological and rheological dynamics of mixed biofilms formed by bacteria and eukaryotic virus. Sci Rep 16, 8315 (2026). https://doi.org/10.1038/s41598-026-39314-9
Nyckelord: biofilmer, kateterinfektioner, virus–bakterie-interaktioner, reovirus, mikrobiella samhällen