Clear Sky Science · sv
En polymerfysikalisk modell av interfasens cellkärna för radiobiologiska simuleringar
Varför formen på vårt DNA‑hem spelar roll
Strålning är ett tveeggat svärd inom medicinen: den kan döda cancerceller men också skada frisk vävnad. I centrum för både risker och fördelar ligger vårt DNA, tätt packat inne i cellkärnan. Denna artikel visar hur en detaljerad, fysik‑inspirerad 3D‑modell av den nukleära ”DNA‑staden” kan hjälpa forskare att förutsäga hur strålning orsakar och felreparerar brott i kromosomer, vilket potentiellt kan förbättra cancerbehandlingar och uppskattningar av rymdstrålningsrisker.
Att se genomet som en levande struktur
I varje mänsklig cell är två meter DNA vikt in i en liten kärna bara några mikrometer över i diameter. Denna vikning är inte slumpmässig: varje kromosom tenderar att inta sitt eget territorium, som i sin tur delas in i kvarter och loopade domäner. Nya experimentella verktyg, som superupplösningsmikroskopi och Hi‑C‑kontaktkartor, har blottlagt denna intrikata 3D‑struktur i anmärkningsvärd detalj. Ändå behandlar de flesta strålningsmodeller fortfarande DNA som en förenklad trasslig linje eller idealiserade slingor och förbiser denna högre ordningens organisation. Författarna satte ut för att bygga en helkärnemodell som respekterar vad biologer lärt sig om verklig kromatinarkitektur, samtidigt som den är tillräckligt snabb för att köras på vanliga laboratoriedatorer.
Att bygga en virtuell kärna med polymerfysik
Gruppen modellerade kromosomer som flexibla kedjor, med idéer lånade från polymerfysik — samma fält som används för att förstå plaster och mjuka material. De delade upp problemet i tre relaxationssteg för att tygla den stora beräkningskostnaden. Först placerade de stora byggklossar kallade kromatin‑domäner i kärnan, lät dem repoussera varandra, sträckas längs sina längder och klustra i bredare subkompartment. Därefter zoomade de in i varje domän för att lägga ut finare kromatinfibrer, inklusive loopade regioner hållna ihop av binda proteiner. Till sist lät de alla fibrer interagera fritt igen innanför kärnans gräns för att närma sig en realistisk slutkonfiguration. Genom att dela upp processen på detta sätt och lägga till hierarkisk sökning och parallella beräkningstrick minskade de körtiden från opraktiska fyra månader till cirka tre timmar per virtuell kärna på en 64‑kärnig arbetsstation.
Från strålningsspår till DNA‑brott och reparationer
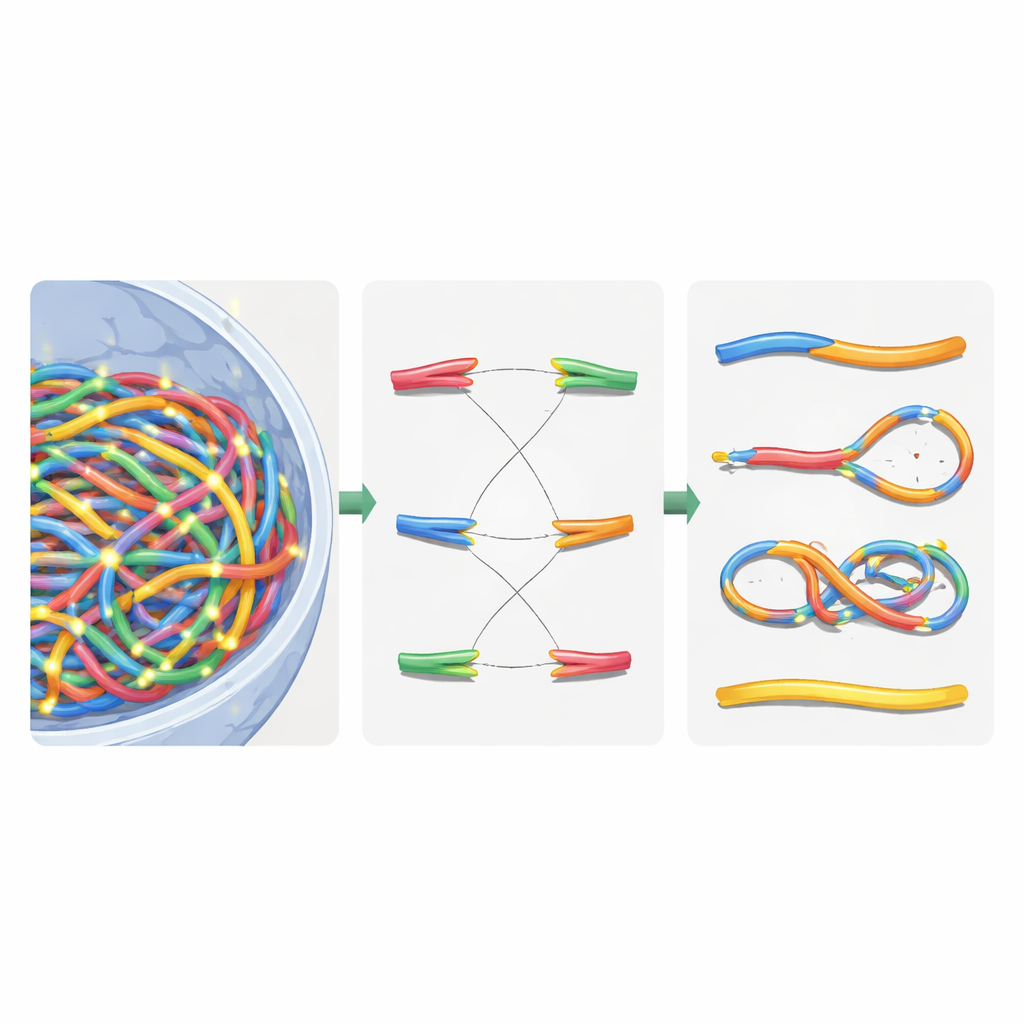
När den virtuella kärnan var uppbyggd lade författarna över detaljerade strålningsspår genererade av Geant4‑DNA‑simulationer. De använde en hierarkisk sökning för att för varje jonisation hända vilken kromatin‑domän, fibersegment och slutligen vilken nukleotid som var närmast, utan att någonsin lagra alla tio miljarder nukleotidpositioner i minnet. Istället behöll de en återanvändbar kromatinmall och tillämpade smarta koordinattransformationer i flykten. Jonisationer i DNA‑ryggraden behandlades som enkelsträngsbrott, och närliggande brott i motsatta strängar blev dubbelsträngsbrott. För att efterlikna cellens reparationsmaskineri introducerade författarna en avståndsbaserad återföreningsregel: fria DNA‑ändar som ligger nära varandra har större sannolikhet att förenas igen. Återföreningsbeslut fattades steg för steg tills alla ändar antingen var parade eller lämnade oåterställda, vilket återskapade både korrekta reparationer och felaktigt hopfogade fragment.
Att sortera brutna kromosomer med nätverkslogik
Efter denna virtuella reparation innehöll kärnan en blandning av återmonterade kromosomer och kvarvarande bitar. För att klassificera vad som hänt översatte författarna det reparerade genomet till en odirigerad graf: kromosomsegment blev kanter, och deras ändar och brytpunkter blev noder. Med en standardalgoritm för sammanhängande komponenter kunde de automatiskt återställa varje nytt kromosomliknande objekt och räkna nyckelfunktioner såsom antalet centromerer (fästpunkter för celldelning) och telomerer (naturliga ändar). Därifrån identifierade de dicentrer (kromosomer med två centromerer), ringar och deletioner. De jämförde sedan sina simuleringar med klassiska experiment i mänskliga hudceller exponerade för gamma‑ och alfastrålning och fann att totala kromosomavvikelser återgavs inom ungefär 20 % av uppmätta värden — en betydande förbättring jämfört med tidigare modeller.
Vad detta betyder för patienter och astronauter
Enkelt uttryckt visar detta arbete att ”var” DNA befinner sig i kärnan och ”hur” det viks starkt påverkar hur strålningsskador summeras till farliga kromosomförändringar. Genom att kombinera realistisk 3D‑genomarkitektur, effektiv fysikbaserad simulering och grafbaserad avläsning av brutna kromosomer erbjuder författarna en kraftfull brygga mellan strukturell biologi och radiobiologi. De argumenterar för att framtida förfiningar — såsom att lägga till detaljerad tidsskala för reparation och använda helgenomssekvenseringsdata — kan göra tillvägagångssättet ännu bättre på att förutsäga den biologiska effekten av högenergetiska partiklar som används i cancerterapi eller möts i djup rymd. I slutändan kan bättre modeller av DNA‑hemmet inne i våra celler hjälpa till att skräddarsy säkrare, mer effektiva strålbehandlingar och förfina vår förståelse av långsiktiga strålningsrisker.
Citering: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Nyckelord: strålningsinducerade DNA‑skador, kromatinets 3D‑arkitektur, kromosomavvikelser, polymerfysikalisk modellering, partikelterapi