Clear Sky Science · sv
Utveckling av mitokondriell funktion i perifera mononukleära blodceller under den tidiga fasen av sepsis hos intensivvårdspatienter
Varför våra cellers kraftverk betyder något vid dödlig infektion
Sepsis, en livshotande reaktion på infektion, skickar hundratusentals människor till intensivvårdsavdelningar (IVA) varje år och dödar miljontals världen över. Läkare vet att många organ sviktar vid sepsis, men den dolda rollen hos de små ”kraftverken” inuti våra immunceller—mitokondrierna—har varit svårare att kartlägga. Denna studie följde IVA‑patienter med sepsis under deras första vecka i intensivvård för att se hur energiproduktionen i centrala blodets immunceller förändrades över tid, och om dessa förändringar var kopplade till överlevnad.
Att titta in i blodet under sepsis
Forskarlaget fokuserade på perifera mononukleära blodceller, en huvudgrupp av vita blodkroppar som driver inflammation och bekämpar mikroorganismer. Eftersom de cirkulerar i hela kroppen och är lätta att ta prov på utgör dessa celler ett användbart fönster till hur immunsystemet hanterar situationen. Teamet jämförde 40 vuxna med sepsis eller septisk chock på en nederländsk IVA med 30 noggrant matchade sjukhuskontroller i samma ålder och kön som inte hade sepsis och i övrigt var metabolt friska. Blod från sepsispatienter togs tre gånger—inom två dagar efter IVA‑intag och sedan ungefär dag tre till fyra och dag fem till sex—medan blod från kontroller togs en gång. Från varje prov isolerade forskarna immunceller, placerade dem i en standardiserad näringslösning och mätte hur snabbt deras mitokondrier förbrukade syre under olika förhållanden, en direkt avläsning av hur hårt cellernas kraftverk arbetade. 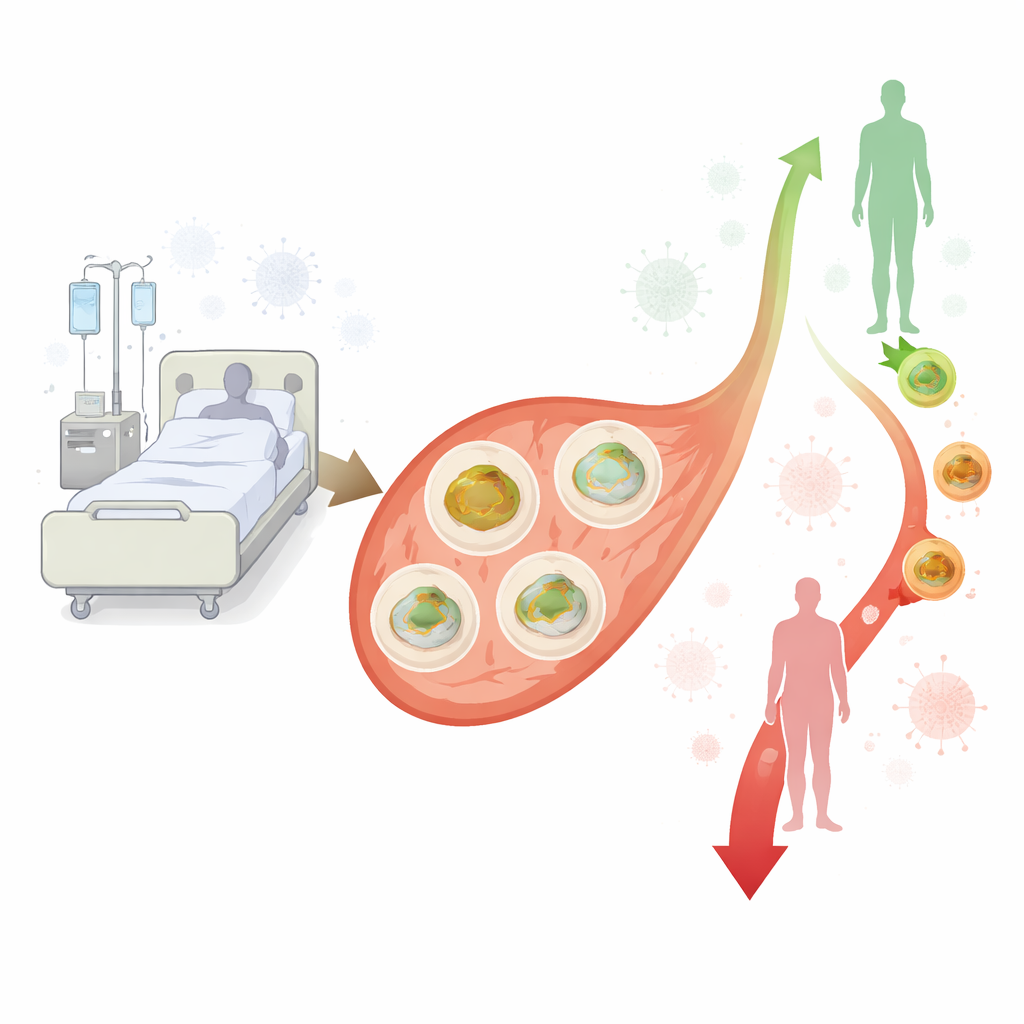
Immuncellernas motorer i högvarv
Motsatt idén att sepsis enkelt ”stänger av” cellernas energiproduktion fann teamet att mitokondriell aktivitet i immunceller konsekvent var högre hos sepsispatienter än hos kontroller. Vid samtliga tidpunkter var basal respiration (grundläggande syreförbrukning i vila) förhöjd. Komponenter kopplade till verklig energiproduktion—ATP‑länkad respiration—liksom mitokondriernas maximala andningskapacitet tenderade också att vara högre, särskilt senare under den första veckan. Även protonläckage, en form av ”slösad” andning där bränsle förbrukas utan att skapa energi, ökade. Tillsammans tyder dessa fynd på att åtminstone i cirkulerande immunceller är energimaskineriet igång och varvtalsökat snarare än förlamat under tidig sepsis, vilket kanske speglar de intensiva kraven från en aktiverad immunrespons.
Gensignaler som matchar den högre aktiviteten
För att se om denna ökade andningsfrekvens understöddes på molekylär nivå undersökte forskarna aktiviteten hos flera gener som kodar för viktiga delar av mitokondriens maskineri. I en delmängd av 10 sepsispatienter och 10 matchade kontroller mätte de genuttryck för delar av oxidativ fosforylering—de proteinkomplex som omvandlar bränsle till ATP. Två gener i synnerhet, SDHB (del av komplex II) och ATP5F1A (del av komplex V, ATP‑synthas), var signifikant mer aktiva hos sepsispatienter vid flera tidpunkter, med ökningar på ungefär 40–50 % jämfört med kontroller. Denna molekylära ”uppväxling” i kärnkomponenter överensstämmer väl med de funktionella data och förstärker idén att mitokondrierna i immunceller pressas att arbeta hårdare under sepsis snarare än att helt kollapsa. 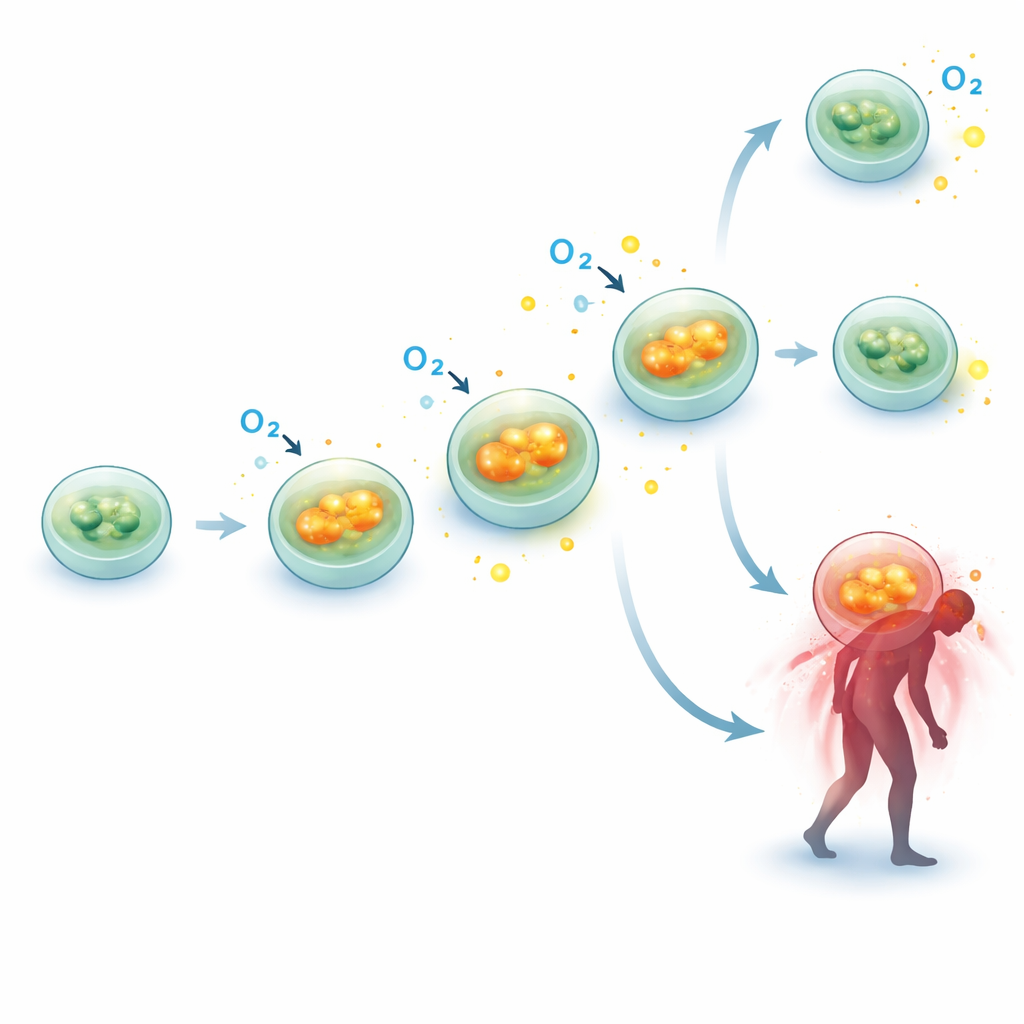
Energiförändringar kopplade till vem som lever och vem som dör
Det mest dämpande fyndet var hur dessa mitokondriella förändringar relaterade till utfall. När teamet jämförde överlevare med icke‑överlevare över tre månader såg de inga stora skillnader i mitokondriell funktion vid den allra första mätningen. Men förändringens riktning under den första veckan berättade en annan historia. Hos överlevare tenderade mitokondriell respiration i immunceller att sjunka något eller förbli stabil. Hos patienter som senare avled ökade samma mått—basal, ATP‑länkad, maximal respiration och reservkapacitet—ytterligare under veckan. Statistisk analys antydde att en starkare ökning i basal respiration mellan första och sista mätningen var associerad med en högre risk att dö inom tre månader, även efter justering för svårighetsgrad i sjukdomen. Eftersom antalet dödsfall var måttligt menar författarna att denna koppling är explorativ och behöver bekräftas, men den antyder att en bestående eskalerande metabolisk drivkraft i immunceller kan vara en varningssignal.
Vad detta betyder för patienter med sepsis
För en icke‑specialist är kärnbudskapet att i tidig sepsis misslyckas inte nödvändigtvis kraftverken inuti cirkulerande immunceller; i stället verkar de gå in i övervarv. Denna extra ansträngning kan bidra till att driva kroppens tidiga försvar mot infektion, men hos vissa patienter fortsätter aktiviteten att stiga istället för att avta, och den bestående överaktiviteten i blodets immunceller kopplades till sämre överlevnad. Studierna visar ännu inte om denna mitokondriella pådrivning är gynnsam, skadlig eller bådadera i olika skeden, men den understryker att sepsis är lika mycket en störning i kroppens energi‑ekonomi som i infektion och inflammation. I framtiden kan noggrann övervakning och kanske försiktig styrning av denna cellulära energianvändning bli en del av hur läkare bedömer risk och skräddarsyr behandling för personer som kämpar mot sepsis på IVA.
Citering: Moonen, H.P.F.X., Slingerland-Boot, R., de Jong, J.C.B.C. et al. Progression of peripheral blood mononuclear cell mitochondrial function during the early phase of sepsis in intensive care unit patients. Sci Rep 16, 8828 (2026). https://doi.org/10.1038/s41598-026-39202-2
Nyckelord: sepsis, mitokondrier, immunceller, kritisk sjukdom, cellulär metabolism