Clear Sky Science · sv
Ökad ateroskleros och uttryck av inflammarafts i makrofag-skumceller hos AIBP-bristfälliga möss.
Varför tilltäppta artärer är mer än bara extra fett
Ateroskleros — den långsamma tilltäppningen och förhårdnaden av våra kärl — är en huvudorsak till hjärtinfarkter och stroke. Vi föreställer oss ofta att det enkelt handlar om fett som byggs upp i blodkärlen, men bilden är mer intrikat: immunceller i kärlväggen kan antingen lugna ner situationen eller elda på inflammationen. Den här studien undersöker varför dessa celler under vissa omständigheter förvandlas från fettförvarande ”städteam” till farliga pådrivare som skjuter plack mot en mer dödlig fas.
Immunceller som hamstrar fett
Inuti utvecklande artärplack tar en typ av vita blodkroppar, makrofager, upp stora mängder kolesterol och blir så kallade skumceller — uppsvällda celler fyllda med oljiga droppar. Tidigare arbete i möss antydde att dessa skumceller, trots sitt ohälsosamma utseende, är förvånansvärt tysta vad gäller inflammation, medan magrare makrofager i närheten tenderar att producera fler inflammatoriska signaler. Den nya forskningen frågar vad som händer om kroppen saknar ett protein som heter AIBP, vilket normalt hjälper till att avlägsna kolesterol från cellsystem och håller vissa membran-”hotspots” i schack.
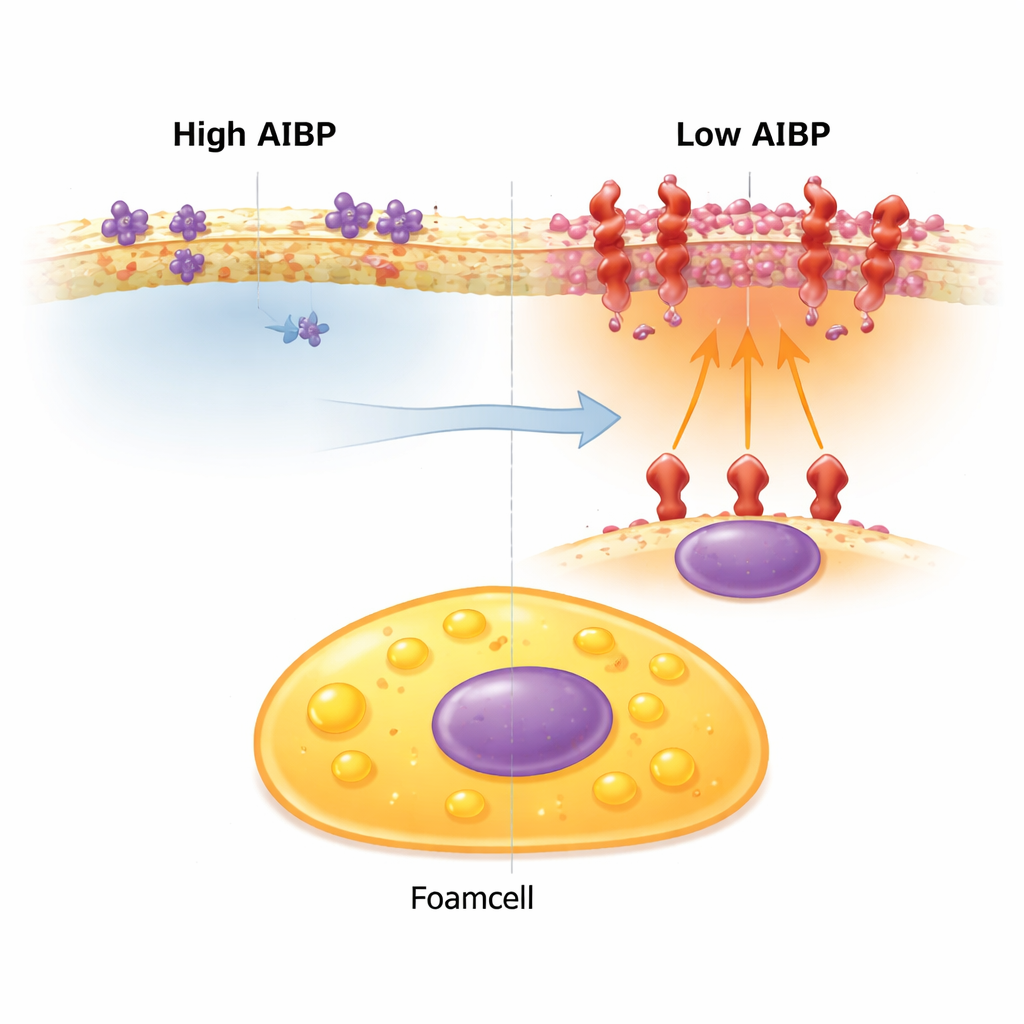
Membran-hotspots som förstärker alarmsignaler
Cellens yta är inte homogen. Kolesterol och vissa fetter klustras i små plattformar där receptorer som känner av fara kan samlas. När dessa plattformar förstoras och packas med inflammatoriska receptorer kallar författarna dem för ”inflammarafts”. En sådan receptor, TLR4, hjälper celler att upptäcka hot men kan driva kronisk inflammation om den överaktiveras. I normala möss som är benägna att få högt kolesterol bär icke-skumiga makrofager vanligen fler av dessa inflammarafts, medan skumcellerna förblir relativt fattiga på dem — en anledning till att skumceller tidigare sett som mindre inflammatoriska.
När fettfyllda celler blir eldhärjade
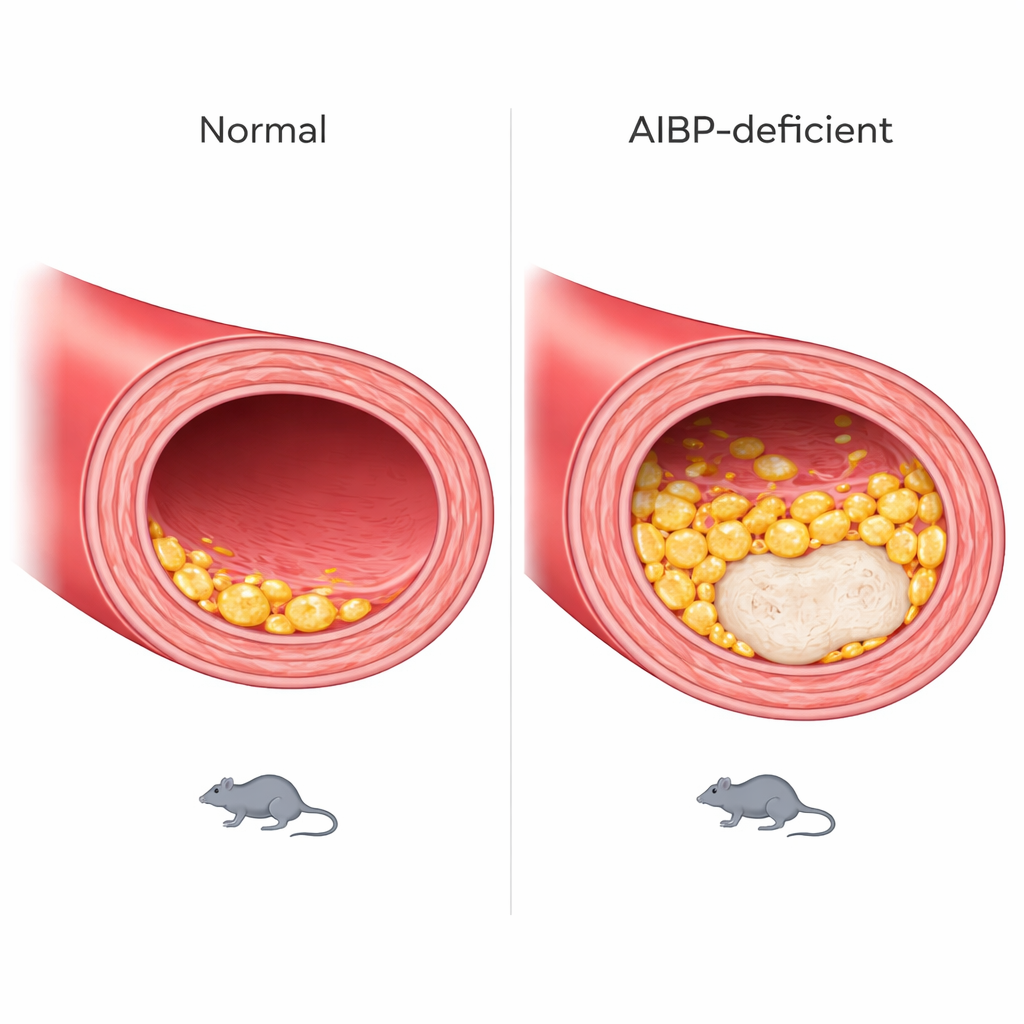
Forskarna jämförde möss som saknade både AIBP och en viktig receptor för kolesterolrengöring (vilket gjorde dem mycket mottagliga för kärlsjukdom) med kontrollmöss som bara saknade receptorn. Efter 16 veckor på en fettrik diet hade AIBP-bristmössen plack med fler skumceller, var och en fylld med mer neutralt fett. Avgörande var att dessa skumceller nu visade höga nivåer av TLR4-par och kolesterolrika membranfläckar — kännetecken för inflammarafts — vilket gjorde dem till den främsta inflammatoriska celltypen i placket snarare än de lugnare, lagringsinriktade cellerna som sågs tidigare. I laboratorieodlingar aktiverade makrofager från AIBP-bristmöss som omvandlats till skumceller med oxiderat kolesterol gener kopplade till inflammation, vävnadsnedbrytning och vaskulär ombyggnad, och visade mer oxidativ stress och stressade mitokondrier.
Växande, instabila plack i kärlväggen
Dessa cellulära förändringar speglades av svårare sjukdom i artärerna. Tvärsnitt av hjärtats stora utflödeskärl visade att AIBP-bristmöss utvecklade större plack och, viktigt, större nekrotiska kärnor — döda zoner i placket kopplade till sprickbenägna, ”sårbara” lesioner. Både han- och honmöss påverkades, även om mönstret för var längs kärlet den värsta skadan uppträdde skilde sig mellan könen. Djuren ökade också i vikt snabbare och hade högre triglyceridnivåer i blodet, vilket tyder på bredare störningar i fettmetabolismen.
Vad detta kan innebära för framtida behandlingar
För en icke-specialist är huvudbudskapet att inte alla kolesterolbelastade celler i ett plack är desamma. När AIBP är närvarande tenderar skumceller att agera mer som lagerenheter, tyst lagra överskott av fett. När AIBP saknas omprogrammerar dessa celler sina ytor, bygger inflammarafts och börjar sända högljudda inflammatoriska signaler som driver plack mot farliga, avancerade stadier. Även om arbetet utförts i möss lyfter det fram AIBP och kontrollen av dessa membranhotspots som potentiella handtag för framtida terapier inriktade på att förhindra att artärplack blir instabila och livshotande.
Citering: Li, S., Nazarenkov, N., Alekseeva, E. et al. Increased atherosclerosis and expression of inflammarafts in macrophage foam cells in AIBP-deficient mice.. Sci Rep 16, 7645 (2026). https://doi.org/10.1038/s41598-026-39113-2
Nyckelord: ateroskleros, makrofag-skumceller, inflammation, kolesterolmetabolism, AIBP