Clear Sky Science · sv
AI-driven diagnosis of acute aortic syndrome based on multi-modal information fusion
Varför detta är viktigt för personer med bröstsmärta
Akut aortasyndrom är ett medicinskt nödläge där kroppens stora artär plötsligt kan rivas sönder, vilket kan leda till döden inom timmar om det förbises. Symptomen liknar ofta en hjärtinfarkt, muskelbristning eller till och med matsmältningsbesvär, vilket gör det särskilt lätt att feldiagnostisera. Denna studie beskriver ett nytt artificiellt intelligenssystem som kombinerar CT-bilder och blodprover för att hjälpa läkare att upptäcka dessa tysta artärkatastrofer tidigare och mer exakt, samt att markera gränsfall som behöver en ny genomgång.
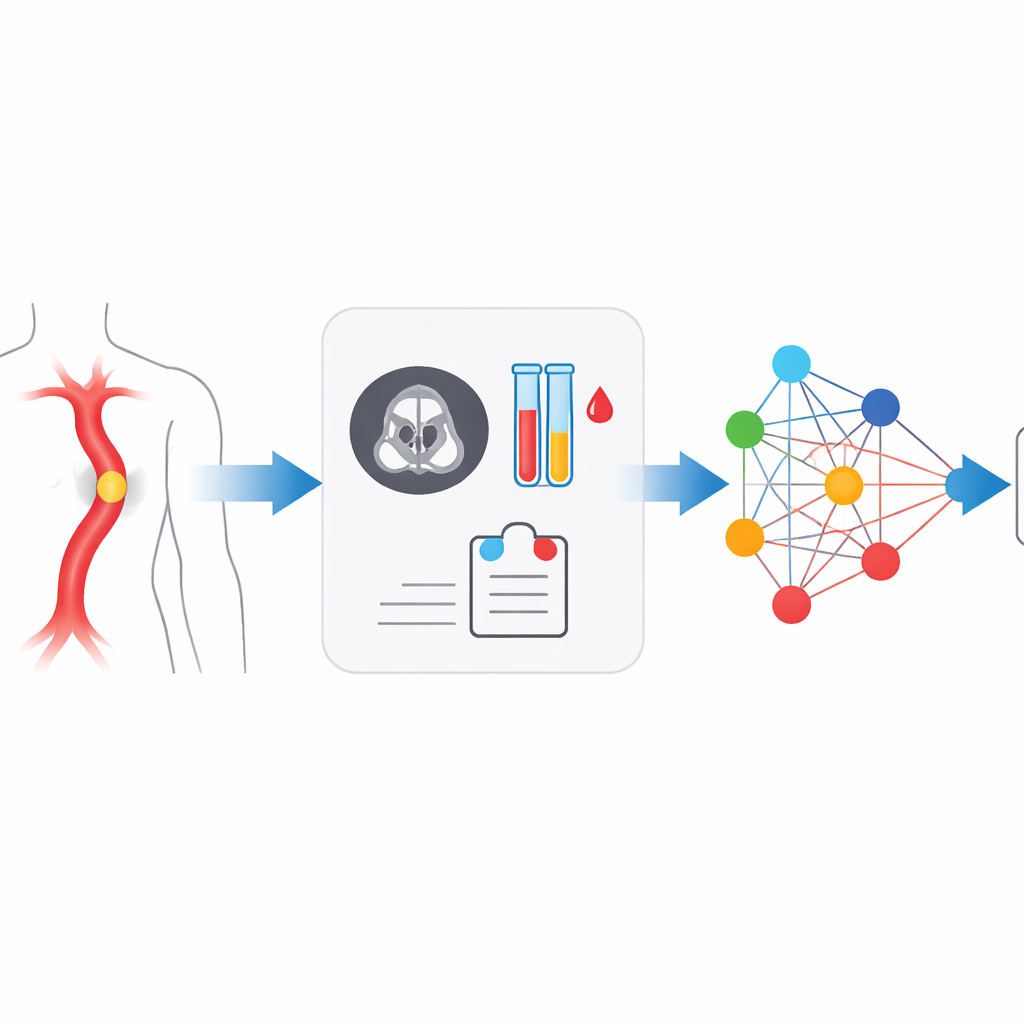
En farlig spricka som döljer sig i fullt dagsljus
Akut aortasyndrom (AAS) omfattar flera besläktade problem i aortaväggen, såsom klassisk dissektion, intramural hematom och penetrerande ulcus. De har alla en gemensam fara: blod tränger in i eller igenom kärlväggen, vilket snabbt kan leda till ruptur eller förlorad blodförsörjning till livsviktiga organ. Risken är som högst under den första dagen eller två efter symtomdebut, då mortaliteten kan närma sig 70 % utan snabb behandling. Läkare använder CT-angiografi för att se aortan och blodprover som D-dimer och inflammationsmarkörer för att bedöma koagulation och immunaktivitet. Men patienternas besvär är ofta vaga, den fysiska undersökningen kan framstå som normal, och CT-bilder kan vara subtila eller försämrade av rörelse eller artefakter, så ungefär en av tre fall missas initialt i rutinmässig praxis.
Vad dagens AI-verktyg missar
De senaste åren har gett kraftfulla bildigenkänningssystem som kan skanna CT- eller röntgenbilder efter tecken på aortaruptur. Men de flesta av dessa verktyg tittar bara på bilder och ignorerar blodprover, eller så kopplar de helt enkelt ihop separata datakanaler utan att verkligen lära sig hur de samspelar. Det står i kontrast till hur kliniker resonerar: de väver ihop vad de ser på bilden med laboratorievärden och patientens historia. Enkel "stapling" av bildfunktioner och laboratorienummer kan till och med förvärra situationen, eftersom blodprovsdata är brusiga, ofullständiga och matematiskt sammanflätade. Många AI-modeller fungerar också som svarta lådor som ger ett utslag utan att visa resonemanget, vilket gör akutläkare tveksamma att lita på dem när liv står på spel.
Ett nytt sätt att förena bilder och blodprover
Författarna byggde en multimodal multiskalefusion (MMMF) modell utformad för att efterlikna hur erfarna radiologer och kardiologer resonerar. Först tittar en tvågrensad bildeencoder på CT-angiografiundersökningen i två detaljnivåer: stora patchar fångar aortas övergripande form och förlopp, medan mindre patchar fokuserar på fina detaljer som små intimalrivningar eller små blodfickor i väggen. Samtidigt omvandlas nyckelblodindikatorer—inklusive D-dimer och ett panel av inflammationsmarkörer härledda från vita blodkroppar och trombocyter—till numeriska funktionspunkter. Dessa bildfunktioner och laboratoriefunktioner blir noder i en graf-liknande struktur, där ett avancerat graf-neuralt nätverk skickar "meddelanden" mellan dem och lär sig hur vissa blodmönster förstärker eller motsäger subtila bildfynd.
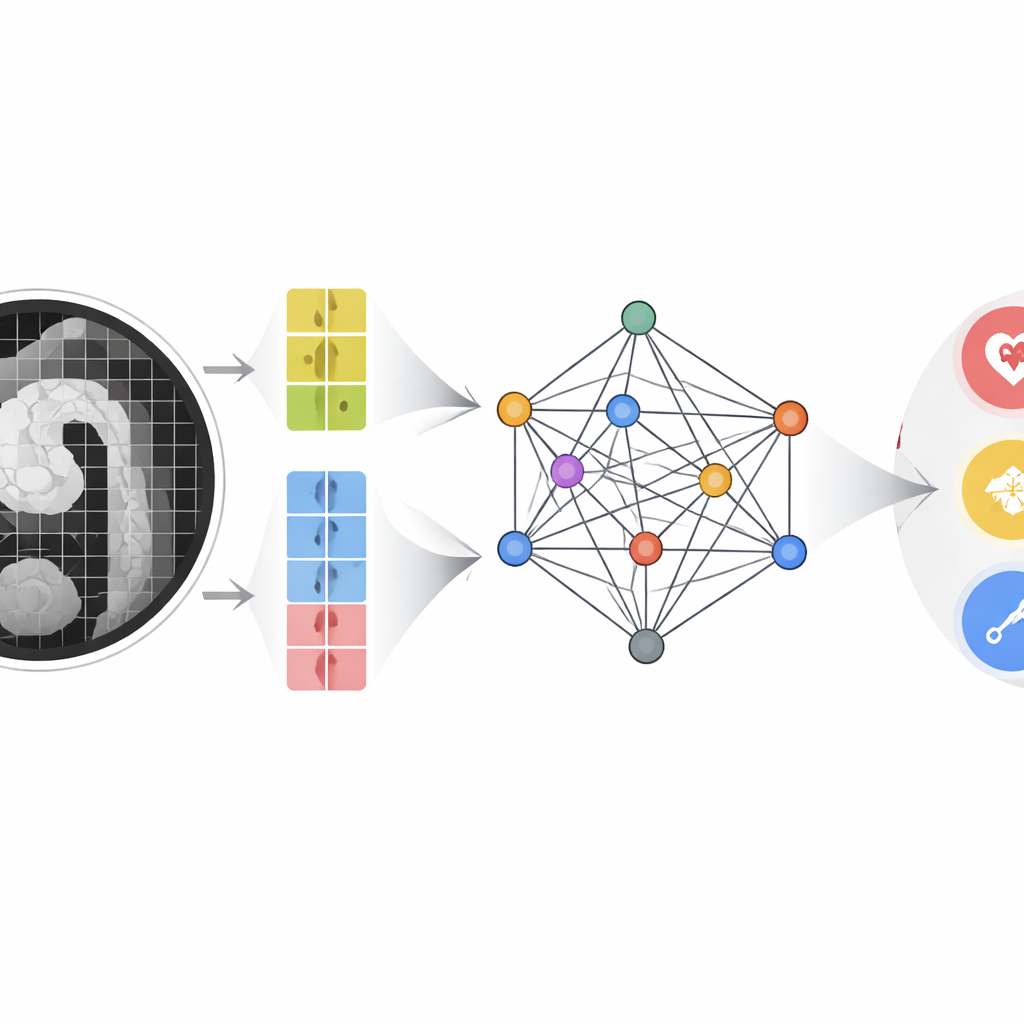
Hur väl systemet presterar
Teamet tränade och testade MMMF-modellen på CT-bilder och samtidiga blodprover från 493 patienter undersökta mellan 2019 och 2024, omfattande bekräftade AAS av olika typer och icke-AAS-kontroller. De jämförde sin metod med välkända bild-endast-modeller, laboratoriedata-endast-modeller och flera toppmoderna multimodala system ursprungligen designade för att para ihop bilder med text. I termer av noggrannhet, precision, återkallning och F1-poäng hamnade MMMF-modellen i topp. Dess totala area under receiver operating characteristic-kurvan översteg 0,9, vilket indikerar stark förmåga att skilja mellan normala aortor, klassiska dissektioner som involverar stigande eller fallande aorta, och atypiska former. Bilddata förblev den enskilt starkaste informationskällan, men noggrant strukturerad fusion med laboratoriedata gav en mätbar förbättring, särskilt för svåra eller gränsfall. Ablationsexperiment visade att två element var avgörande: den tvåskaliga bildvägen och transformatorbaserade grafen som modellerar långräckviddsrelationer mellan funktioner.
Mot ett partnerskap mellan läkare och maskiner
Bortom huvudrubriksiffrorna är ett centralt bidrag i detta arbete dess tonvikt på samarbete snarare än ersättning. Systemet är särskilt skickligt på att snabbt sålla bort uppenbart normala skanningar och klart sjuka atypiska fall och fungerar som en slags intelligent första linjens granskare. Lika viktigt är att det kan känna igen när dess egen säkerhet är låg—ofta i fall som även mänskliga experter finner svåra, såsom tidiga eller mildare former av dissektion—så att det kan markera dessa patienter för brådskande omprövning, kompletterande bilddiagnostik eller senior konsultation. I huvudsak visar studien att när bilddetaljer och blodprovsledtrådar vävs samman på ett strukturerat, kliniskt inspirerat sätt, kan AI både skärpa tidig diagnos av akut aortasyndrom och erbjuda ett säkerhetsnät mot missade akuta tillstånd, samtidigt som läkare behåller det slutgiltiga ansvaret för beslut.
Citering: Yang, Z., Xu, S., Wang, B. et al. AI-driven diagnosis of acute aortic syndrome based on multi-modal information fusion. Sci Rep 16, 8332 (2026). https://doi.org/10.1038/s41598-026-39111-4
Nyckelord: acute aortic syndrome, aortic dissection, medical AI, multimodal diagnosis, graph neural network