Clear Sky Science · sv
Dlgap2‑brist stör synaptisk homeostas genom att främja ubiquitin‑medierad nedbrytning av Itsn1 i en valproinsyra‑inducerad autismliknande modell
Varför ett vanligt läkemedel och hjärnans kopplingar spelar roll
Valproinsyra är ett länge använt läkemedel vid epilepsi och stämningsstörningar, men när det tas under graviditet har det kopplats till ökad risk för autism hos barn. Denna studie ställer en angelägen fråga för familjer och läkare: vad gör detta läkemedel exakt mot den utvecklande hjärnans kopplingar? Genom att följa förändringar ned till specifika molekyler vid synapserna — de kontaktpunkter där nervceller kommunicerar — avslöjar forskarna en ny händelsekedja som kan hjälpa förklara autismliknande beteenden och peka mot framtida behandlingsstrategier. 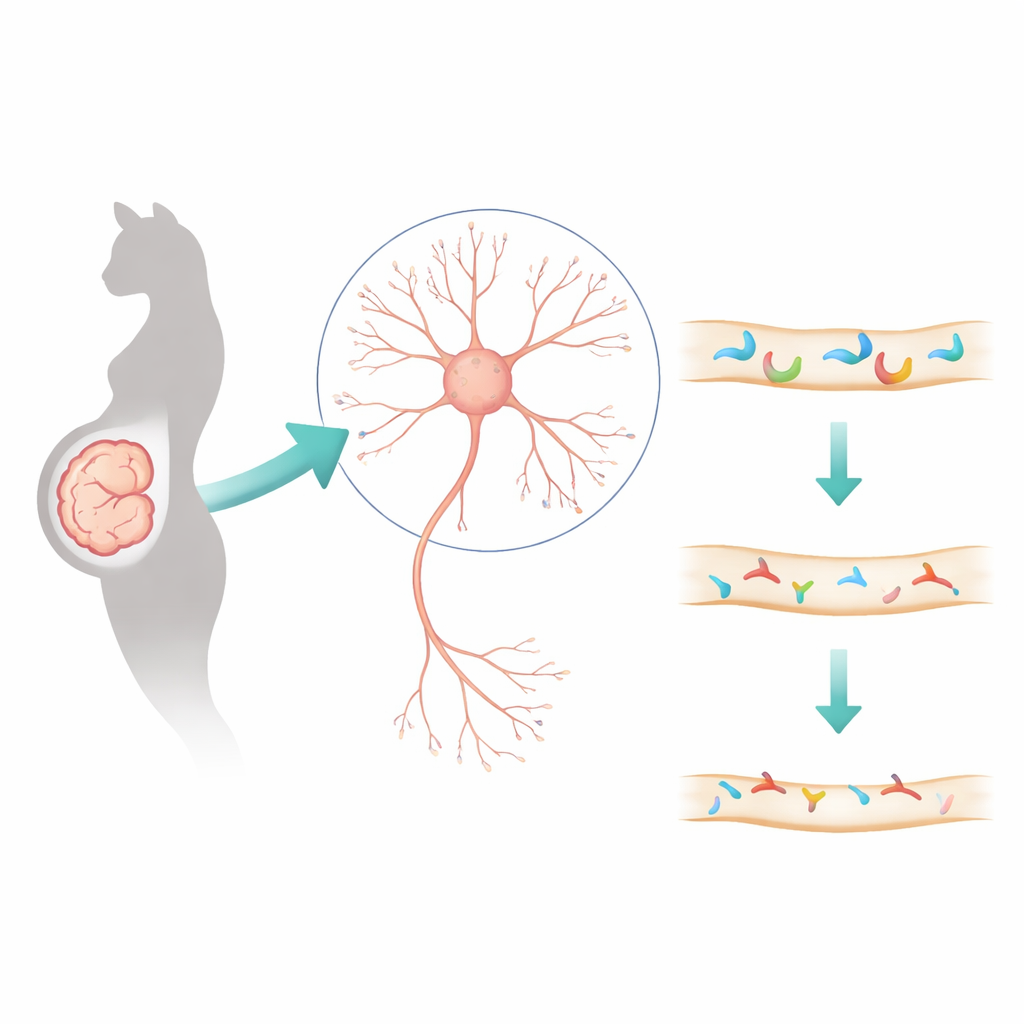
Söker över arter efter gemensamma sårbarheter
För att hitta pålitliga ledtrådar förlitade sig teamet inte på bara en djurmodell. De jämförde hjärnor eller hjärnliknande vävnader från mänskliga kortikala organoider, apor, råttor och möss som hade exponerats för valproinsyra före födseln. Med hjälp av storskaliga gen‑ och proteinstudier identifierade de en liten uppsättning gener som förändrades i alla dessa system och som var kopplade till synapser och isolering av nervtrådar. En av dem stack ut: Dlgap2, ett stomprotein som hjälper till att organisera den postsynaptiska sidan av excitatoriska synapser. Hos möss som fått prenatal valproinsyra föll Dlgap2‑nivåerna i cortex och mer specifikt inne i små synaptiska kompartment, vilket tyder på att detta strukturbevarande protein är en nyckeloffer för läkemedelsexponering.
Från molekylära förändringar till beteendeförändringar
Författarna frågade sedan om förlust av Dlgap2 ensam är tillräcklig för att störa hjärnfunktionen. De använde virus som bar short hairpin RNA för att minska Dlgap2 i odlade musneuroner och hos nyfödda möss. I odlingen växte neuroner med lägre Dlgap2 kortare grenar och hade färre postsynaptiska punkter, tecken på försvagade kopplingar. I levande djur gav riktad nedreglering av Dlgap2 i hjärnan upphov till autismliknande beteenden: unga hanmöss hade svårt att lära sig platsen för en dold plattform i ett vattenlabyrintprov och visade minskat intresse för sociala partners och för social nyfikenhet i ett trekammarsteste. Dessa förändringar efterliknar de inlärnings‑ och sociala brister som ses hos djur exponerade för valproinsyra och stärker argumentet att Dlgap2‑förlust inte bara är en sidoeffekt utan en drivkraft bakom förändrat beteende.
Hittar en sårbar partner i synapsen
För att förstå hur Dlgap2‑förlust sprider sig genom synapsen undersökte forskarna närmare de proteiner som är förankrade i den postsynaptiska densiteten, den täta molekylära plattan som tar emot kemiska signaler. Med hjälp av proteomik fann de att minskat Dlgap2 förändrade mängden av hundratals synaptiska proteiner, särskilt de som är involverade i att organisera synapser och återvinna vesiklar genom endocytos. Ett protein, Intersectin‑1 (Itsn1), föll särskilt kraftigt. Ytterligare biokemiskt arbete visade att Dlgap2 och Itsn1 fysiskt finns i samma proteincomplex i synapsberikade fraktioner och att båda förekommer bland gener kopplade till autism. Detta pekade på ett fokuserat reglerande partnerskap mellan de två molekylerna i ett trångt synaptiskt landskap. 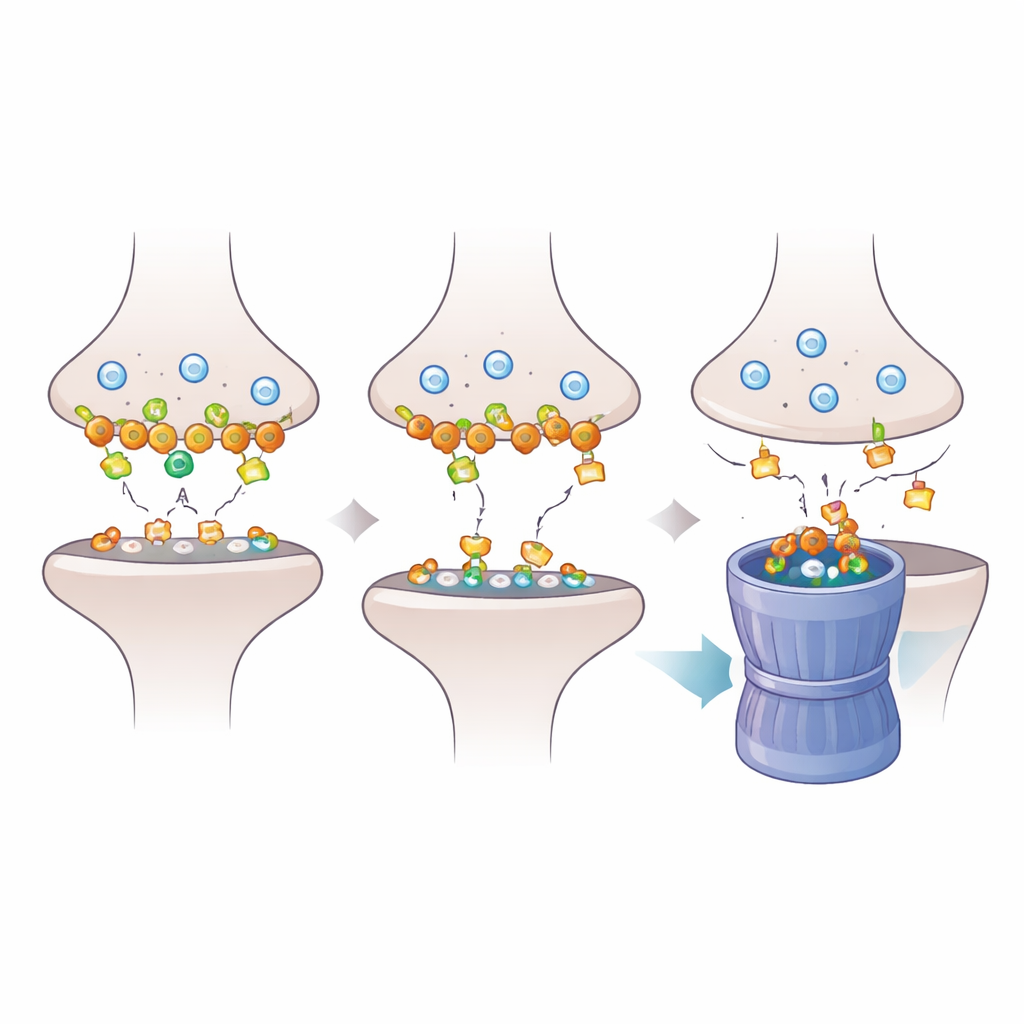
En dold bortskaffningsväg framträder
Teamet undersökte nästa varför Itsn1‑nivåerna sjunker när Dlgap2 saknas. De observerade att i synaptiska kompartment utlöste Dlgap2‑nedreglering en form av proteintaggning känd som K48‑länkad ubiquitinering, vilket markerar proteiner för nedbrytning av cellens proteasom‑”malningsverk”. Att blockera detta bortskaffningssystem med läkemedlet MG132 förhindrade förlusten av Itsn1, vilket indikerar att Dlgap2 normalt skyddar Itsn1 från att bli taggad och förstörd. Utan Dlgap2 blir Itsn1 i allt högre grad taggat, skickas till proteasomen och töms från synapser, vilket underminerar endocytisk återvinning och balansen i synaptisk aktivitet. Studien tyder på att subtila skift i hur snabbt nyckelproteiner omsätts kan destabilisera synapser under hjärnans utveckling.
Vad detta betyder för autism och framtida behandlingar
Tillsammans föreslår studien en enkel men kraftfull idé för icke‑specialister: prenatal exponering för valproinsyra kan försvaga ett strukturellt ”järn”protein (Dlgap2) vid synapser. När det järnet försvinner blir dess partnerprotein (Itsn1) överexponerat för cellulärt sopborttagande, vilket leder till bristfällig återvinning av synaptiska komponenter och i slutändan till felkopplade kretsar och autismliknande beteenden hos möss. Medan många gener och miljöfaktorer bidrar till autism erbjuder denna Dlgap2–Itsn1‑axel en konkret molekylär kedja från prenatal läkemedelsexponering till förändrad hjärnfunktion. I längden skulle strategier som bevarar detta partnerskap eller finjusterar proteinnedbrytningsmaskineriet i synapser kunna hjälpa till att skydda utvecklande hjärnor från liknande former av störning.
Citering: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Nyckelord: valproinsyra och graviditet, synaptiska stomproteiner, mekanismer vid autismspektrum, ubiquitin‑proteasomvägen, musmodeller för autism