Clear Sky Science · sv
In silico‑identifiering av inhalerbara småmolekylära IL‑33/ST2‑antagonister för svåra typ‑2‑höga astmaendotyper
Varför detta spelar roll för andningen
För miljontals människor med svår astma kan även moderna inhalatorer och avancerade injektioner lämna dem andfådda och i riskzonen för farliga attacker. Denna studie undersöker om välkända, tablettliknande läkemedel skulle kunna omdesignas för att fungera som inhalationsbehandlingar som blockerar ett av astmats tidiga ”alarm”‑signaler i lungorna. Med enbart datorbaserade simuleringar sökte forskarna efter små molekyler som kan passa på en nyckelreceptor involverad i svår, allergidriven astma och lade därmed grunden för framtida laboratorietester snarare än att erbjuda ett färdigt läkemedel.
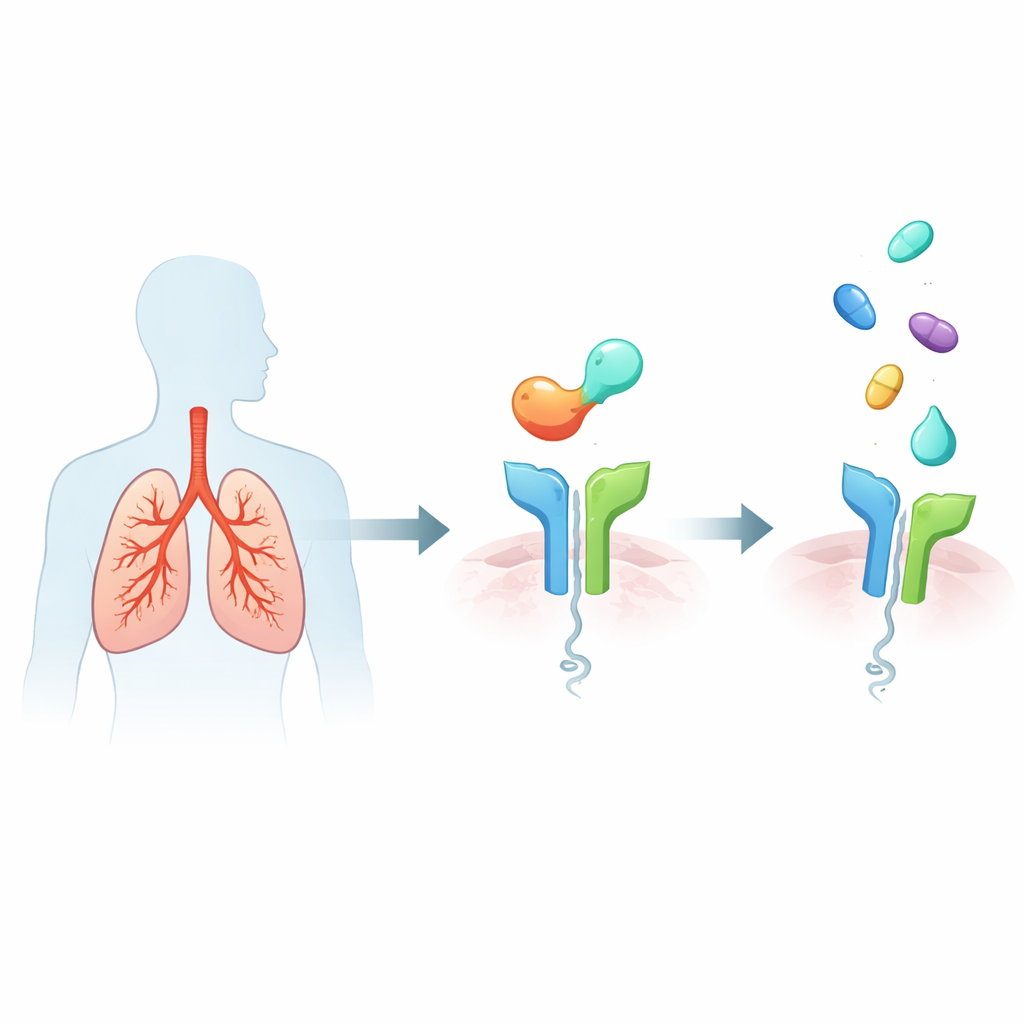
Alarmssystemet inne i astmatiska lungor
Svår typ‑2‑hög astma kännetecknas av ett överdrivet immunsvar som fyller luftvägarna med slem och inflammatoriska celler, smalnar av andningsrören och över tid skadar lungstrukturen. En viktig utlösare är ett protein kallat IL‑33, som frisätts av stressade epitelceller i luftvägarna. IL‑33 binder till en receptor kallad ST2 på olika immunceller, vilka då släpper ut kraftfulla budbärarmolekyler som driver typiska astmasymtom som pipande andning, skov och långvarig ombyggnad av luftvägarna. Eftersom högre IL‑33/ST2‑aktivitet kopplats till sämre symtom och fler attacker har ST2 framträtt som ett attraktivt upstream‑mål: blockera ST2, och du kan dämpa många av de efterföljande inflammatoriska signalerna på en gång.
Från antikroppar till vardagliga läkemedel
Flera nuvarande behandlingar för svår astma använder injicerade antikroppar som fångar upp inflammatoriska proteiner i blodet eller blockerar deras receptorer. Dessa biologiska läkemedel fungerar för vissa, men de är dyra, måste ges med injektion och riktar sig främst mot signaler längre ner i kedjan. I kontrast kan småmolekylära läkemedel — mer liknande traditionella tabletter eller inhalatorer — produceras i större skala, förvaras lättare och potentiellt levereras direkt till lungorna. Utmaningen är att ST2 binder IL‑33 över en vid protein‑protein‑yta, vilket är svårare för små molekyler att störa än en tydlig, djup ficka på ett enzym. Författarna vände sig därför till högupplöst strukturell data för ST2–IL‑33‑komplexet och moderna in silico‑verktyg för att se om några kända antiinflammatoriska läkemedel oväntat skulle kunna greppa en del av denna yta.
Söker över receptorernas yta med datorn
Med hjälp av kristallstrukturen för mänskligt ST2 bundet till IL‑33 tog teamet först bort IL‑33 för att exponera receptor‑bindningsytan och använde ett program för att hitta fickor för att identifiera den mest lovande regionen för en småmolekyl att lägga sig i. De valde sedan tio kliniskt relevanta småmolekyler som redan används vid astma eller relaterade immunsjukdomar — såsom leukotrienblockerarna Montelukast och Zafirlukast, immunmodulerande talidomid‑relaterade föreningar och JAK‑hämmare — plus en tidigare rapporterad ST2‑fokuserad molekyl som referens. Med virtuell dockningsmjukvara positionerades varje förening tusentals gånger på ST2‑ytan, och de bäst passande poserna poängsattes efter förväntad bindningsstyrka. Zafirlukast framträdde som det högst rankade skelettet, något bättre än Montelukast och den kända ST2‑riktade jämförelseföreningen.
Finjustering av en ledande molekyl på skärmen
Eftersom Zafirlukast visade den mest lovande balansen mellan förutsagd bindning och allmän läkemedelsliknande beteende använde författarna ett AI‑styrt designverktyg för att skapa en modifierad version av denna molekyl. Målet var att behålla dess grepp om ST2 samtidigt som dess förutspådda säkerhetsprofil förbättrades. Den omdesignade analogen hade en mycket liknande dockningspoäng och förutspåddes vara mindre toxisk in silico. Detaljerade kontaktkartor föreslog att både moderföreningen och den modifierade föreningen rörde vid flera av samma ST2‑aminosyror som normalt kontaktar IL‑33, vilket antyder att de upptar funktionellt viktiga delar av gränsytan. Utökade molekylära dynamiksimuleringar — en halv mikrosekund av virtuell rörelse i vatten och salt — visade att både receptorn och liganden förblev flexibla, där småmolekylen provade olika positioner längs ytan snarare än att låsa sig stelt. Beräkningar av interaktionsenergier över tid pekade på en meningsfull men dynamisk association, förenlig med en molekyl som sonderar en relativt plan protein‑protein‑yta.
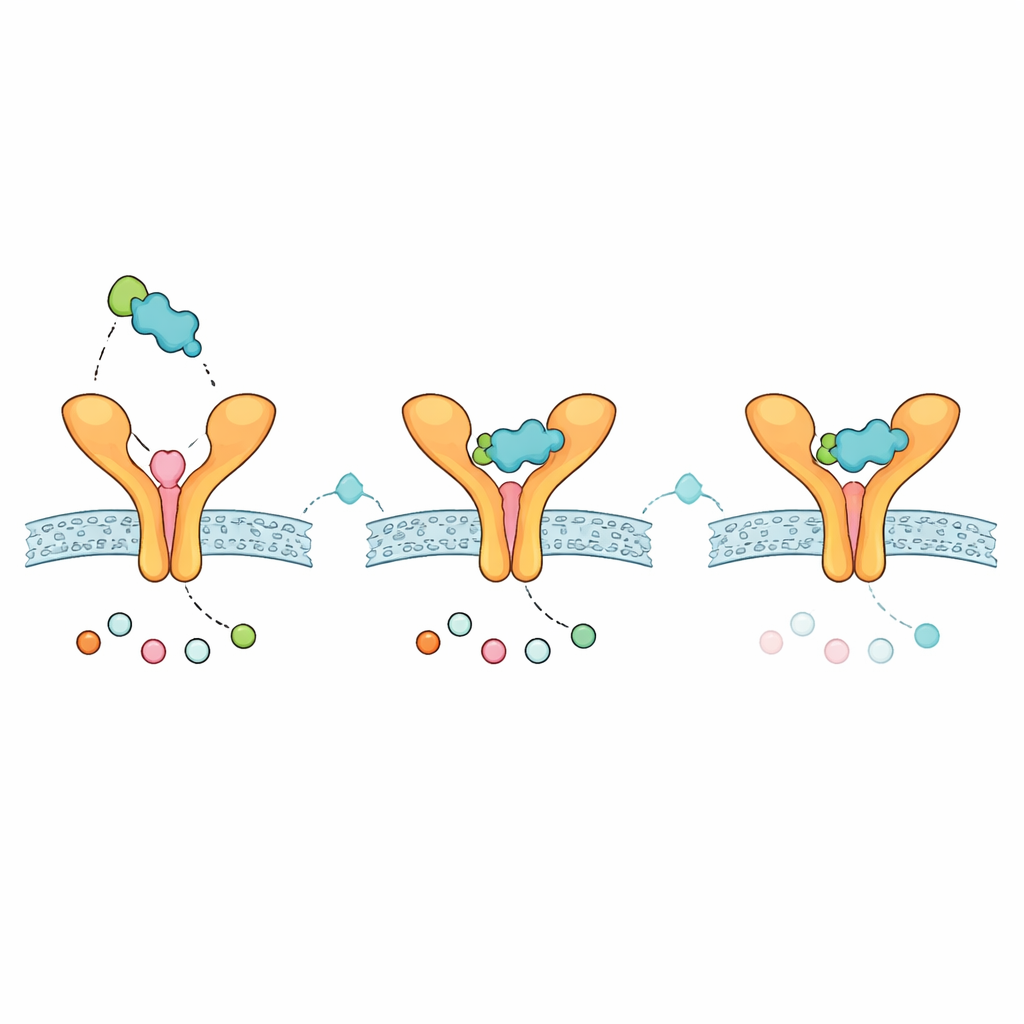
Ledtrådar om hur en framtida inhalator kan bete sig
För att undersöka om den modifierade Zafirlukasten plausibelt kunde fungera som ett läkemedel körde teamet standardiserade beräkningskontroller för absorption, distribution, metabolism, utsöndring och toxicitet. Analogen uppfyllde vanliga regler för oral läkemedelslikhet, visade måttlig storlek och lipofilicitet och förutspåddes hålla sig utanför hjärnan — egenskaper som kan vara fördelaktiga för en lungfokuserad behandling med begränsade systemiska biverkningar. Löslighetsuppskattningar varierade mellan modeller, vilket innebär att noggrann formulering skulle krävas, särskilt för icke‑orala administrationsvägar som inhalation. Föreningen förutspåddes också interagera med vissa leverenzym, vilket antyder att potentiella läkemedelsinteraktioner skulle behöva beaktas om den någonsin skulle användas tillsammans med andra läkemedel.
Vad detta arbete egentligen visar
Istället för att leverera ett nytt astmaläkemedel demonstrerar denna studie en steg‑för‑steg datorbaserad strategi för att hitta och förfina småmolekyler som kan störa IL‑33/ST2‑alarmsystemet vid ytan av luftvägsceller. Den lyfter fram Zafirlukast och en AI‑optimerad släkting som plausibla startpunkter för laboratorieexperiment, visar att de kan inta nyckeldelar av ST2‑gränsytan och har i stora drag acceptabla förutsagda säkerhets‑ och läkemedelsliknande egenskaper. Allt bevismaterial är dock virtuellt: arbetet bevisar inte att dessa molekyler blockerar IL‑33 från att binda ST2, dämpar inflammatorisk signalering eller hjälper patienter att andas lättare. Dessa svar kräver biokemiska tester, cellstudier, djurmodeller och så småningom kliniska prövningar. För nu erbjuder studien en datorbaserad färdplan och en kort lista med kandidat‑skelett för forskare som siktar på att omvandla kroppens eget astmalarm till ett praktiskt, inhalerbart läkemedelsmål.
Citering: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Nyckelord: svår astma, IL‑33 ST2‑signalväg, småmolekylära antagonister, in silico läkemedelsdesign, inhalationsbehandlingar