Clear Sky Science · sv
Strukturbaserad modellering avslöjar molekylär grund för CYP153A6:s nya aktivitet mot toluenderivat
Att överlåta svåra kemiska uppgifter åt naturen
Kemister och industrin är beroende av reaktioner som tillsätter syre till envisa kol–väte‑bindningar, till exempel för att rengöra föroreningar eller bygga komponenter till läkemedel och doftämnen. Att göra detta rent, utan hårda kemikalier eller tungmetallsavfall, är svårt. Denna studie undersöker en naturlig katalysator, ett enzym kallat CYP153A6 från en jordbakterie, och ställer en enkel fråga med stora följder: kan detta enzym vägledas att selektivt ”uppgradera” toluenliknande molekyler — vanliga beståndsdelar i bränslen och lösningsmedel — till mer användbara och miljövänliga produkter?
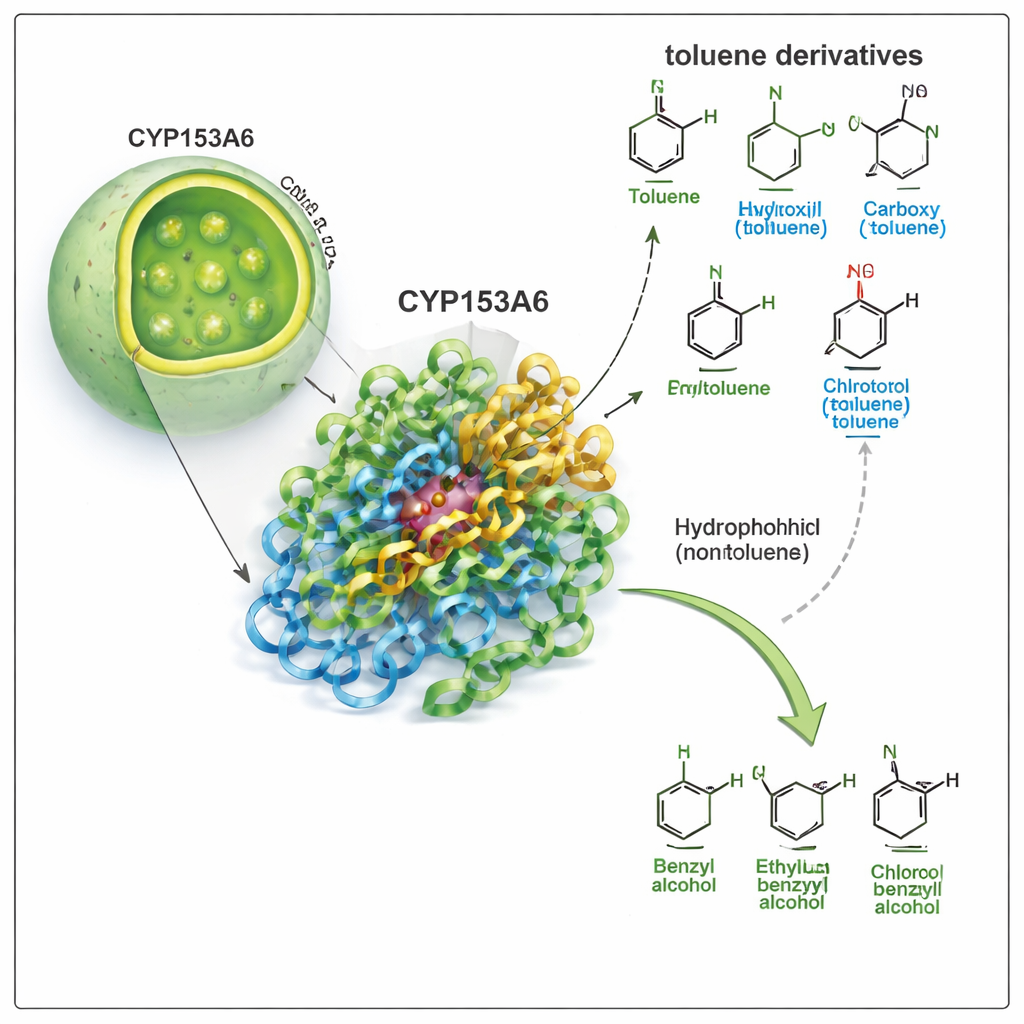
Ett enzym som väljer en enda plats
CYP153A6 tillhör den stora cytochrom P450‑familjen, naturens mångsidiga oxidationsexperter. Till skillnad från många industriella katalysatorer fungerar detta enzym i vatten, vid måttliga temperaturer, och väljer mycket specifika positioner på en molekyl. Tidigare arbete visade att CYP153A6 lägger till syre i ändarna på enkla kolvätekedjor och i vissa växtbaserade doftmolekyler. Här frågar författarna om det också kan angripa den så kallade ”benzylica” positionen — den lilla sidokedjan som sitter på en bensenring — i toluen och besläktade föreningar. Den omvandlingen förvandlar toluenderivat till benzylalkoholer, värdefulla byggstenar för läkemedel, smaker och fina kemikalier.
Testa vilka molekyler enzymet gillar
Forskargruppen genomförde först biotransformationsförsök med modifierade E. coli-celler som producerar CYP153A6, antingen som hela celler eller som cellfria extrakt. De utsatte enzymet för ett panelprov av toluenderivat och varierade gruppen som sitter på aromatringen (såsom metyl, klor, metoxi, hydroxyl eller nitro) och dess position (para, meta eller orto). Enzymet presterade mycket väl på apolära eller bara svagt polära föreningar, såsom p‑cymen, p‑xylene, p‑metylanisol och p‑klorotoluen, och omvandlade konsekvent den benzylica metylgruppen till en benzylalkohol. Slående nog ignorerade det helt starkare polära molekyler som p‑cresol, p‑metylbenzylalkohol och p‑nitrotoluen, trots att dessa är strukturellt likartade. Detta mönster antyder att enzymets ficka är starkt hydrofob och ogillar polära grupper.
Bygga en tredimensionell karta över den molekylära maskinen
Eftersom den tredimensionella strukturen för CYP153A6 inte hade lösts experimentellt, byggde forskarna en högkvalitativ datormodell med hjälp av en närbesläktad P450 vars struktur är känd. De validerade modellen genom att kontrollera dess geometri och köra långa molekylärdynamiska simuleringar för att se om proteinet förblev stabilt över tid — vilket det gjorde. Simuleringarna avslöjade en begravd aktiv yta kopplad till utsidan via smala tunnlar genom vilka substrat kommer in och produkter lämnar. Dessa tunnlar formas och slussas av flexibla slingor på proteinets yta, vilket hjälper till att förklara hur enzymet kan styra hydrofoba molekyler ner mot den reaktiva hemjärn‑centra samtidigt som vatten och oxiderade produkter kan undkomma.
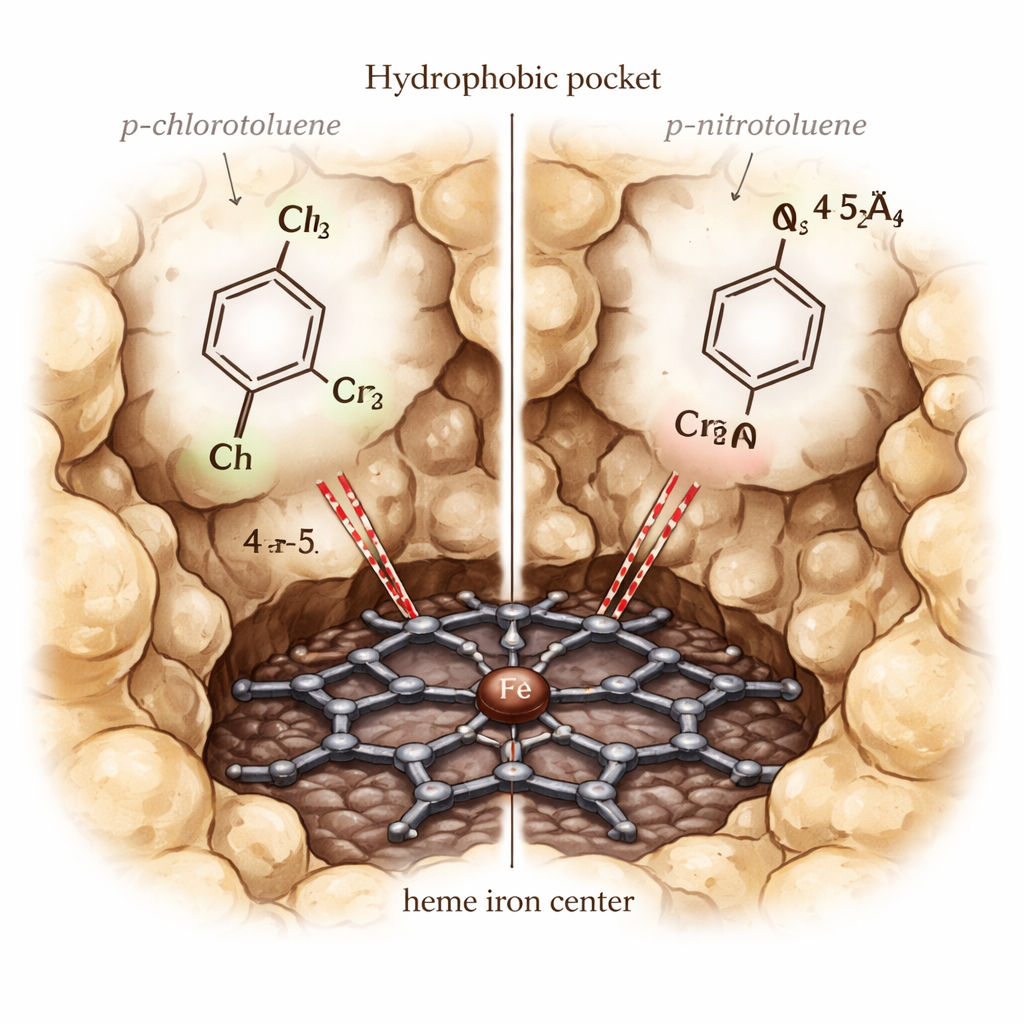
Se hur molekyler dockar, rör sig och reagerar
Med modellen i hand simulerade författarna hur olika toluenderivat binder inne i CYP153A6. De använde en metod kallad ensemble‑dockning, där man prövar många subtilt olika proteinformer och flera elektroniska tillstånd hos hemjärnet, för att identifiera vilka kombinationer som bäst särskiljer verkliga substrat från icke‑substrat. Den vinnande konfigurationen använde järnet i dess vilotillstånd (ferriskt) och inga extra vattenmolekyler i fickan, och den favoriserade korrekt kända substrat. Uppföljande simuleringar följde, bild för bild, hur varje molekyl positionerade sig i förhållande till hemet. Bra substrat som p‑cymen och p‑xylene låg nära järnet med sin benzylica metylgrupp riktad mot det, och deras förutsagda bindningsenergier var starkt fördelaktiga. Dåliga substrat tenderade att driva bort, anta klumpiga orienteringar eller interagera ogynnsamt med de mest oljiga sidokedjorna som klär fickan.
Varför en likartad molekyl reagerar medan en annan inte gör det
En gåta stack ut: p‑klorotoluen oxideras effektivt av CYP153A6, medan p‑nitrotoluen inte gör det, trots att båda får plats i fickan och binds med liknande styrka i simuleringarna. För att lösa detta genomförde författarna mer detaljerade kvantmekanik/molekylmekanik (QM/MM)‑beräkningar på enzymets högreaktiva ”Compound I”‑tillstånd. Dessa beräkningar visade att nitrogruppen drar så mycket elektronisk täthet bort från den benzylica kolet att det blir mycket svårt att oxidera, trots att det geometriskt ligger tillräckligt nära. I kontrast tillåter klorgruppen bättre elektronisk kommunikation mellan hemet och substratet, vilket återspeglas i högre spintäthet på aromringen och metylgruppen och en mer reaktiv inriktning för det kritiska väteabstraktionssteget.
Vad detta betyder för renare kemi
I vardagliga termer beter sig CYP153A6 som en liten, oljig handske som håller vissa bränsleliknande molekyler på ett sätt som möjliggör att syre kan adderas på en bestämd punkt — och förvandla dem till mer vattenlösliga, användbara och i slutändan mer nedbrytbara produkter. Studien visar att enzymet föredrar icke‑polära substituenter och att både form och elektronflöde avgör om ett givet toluenderivat kommer att omvandlas. Genom att klargöra hur CYP153A6 känner igen och aktiverar dessa molekyler lägger arbetet en ritning för att konstruera förbättrade varianter som skulle kunna hjälpa till att sanera aromatiska föroreningar eller tillverka komplexa kemikalier på ett mer hållbart sätt.
Citering: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Nyckelord: biokatalys, cytochrom P450, toluenshydroxylering, enzymteknik, grön kemi