Clear Sky Science · sv
Transplastomiskt biobruk för produktion av funktionell human α‑laktalbumin för nutritions‑ och terapeutiska tillämpningar
Att göra växter till mjölkproteinfabriker
Moderna kostvanor är starkt beroende av mjölkproteiner, men nötkötts‑ och mjölkproduktion i global skala medför miljökostnader och etiska frågeställningar. Denna studie undersöker ett mycket annorlunda sätt att framställa ett centralt humanmjölksprotein—genom att lära växtblad att producera det. Arbetet visar att tobaksväxter kan omprogrammeras för att tillverka human α‑laktalbumin, ett protein som är viktigt för spädbarnsnutrition och som har potentiella anti‑canceregenskaper, vilket öppnar en väg mot ingredienser till djurfri barnmat och nya cancerbekämpande livsmedelskomponenter.
Varför detta mjölkprotein är viktigt
Humant bröstmjölk är mer än bara näring; det är en finjusterad blandning av proteiner, fetter och sockerarter som förändras efter spädbarnets behov. Ett av de viktigaste proteinerna är α‑laktalbumin, som hjälper till att bygga laktos, huvudsockret i mjölk och en avgörande energikälla för barn. α‑Laktalbumin är rikt på essentiella aminosyror, inklusive tryptofan, en byggsten för hjärnans ”må‑bra”kemikalie serotonin, och har kopplats till bättre stressresiliens och potentiellt skydd mot vissa cancerformer. Eftersom det är lättsmält, har mild smak och är stabilt över ett brett pH‑intervall används det i stor utsträckning i modersmjölksersättningar och näringsdrycker—och efterfrågan ökar.
Problemet med traditionell mjölkproduktion
Att förlita sig på kor för att leverera mjölkproteiner har nackdelar. Boskap står för en betydande andel av de globala växthusgasutsläppen, och stora mejeriverksamheter kräver omfattande mark, vatten och foder. Därtill kan djurhållning medföra oro kring hormoner, antibiotika och patogener som hamnar i mjölkflödet. Dessa påfrestningar har ökat intresset för ”cellulär jordbruk” där mjölkproteiner framställs av mikrober eller odlade celler istället för djur. Många av dessa system är dock fortfarande dyra, svåra att skala upp eller producerar proteiner som inte är helt identiska med de mänskliga versionerna. Växter, särskilt deras kloroplaster—de små gröna fabrikerna som driver fotosyntesen—erbjuder en lovande alternativ plattform.
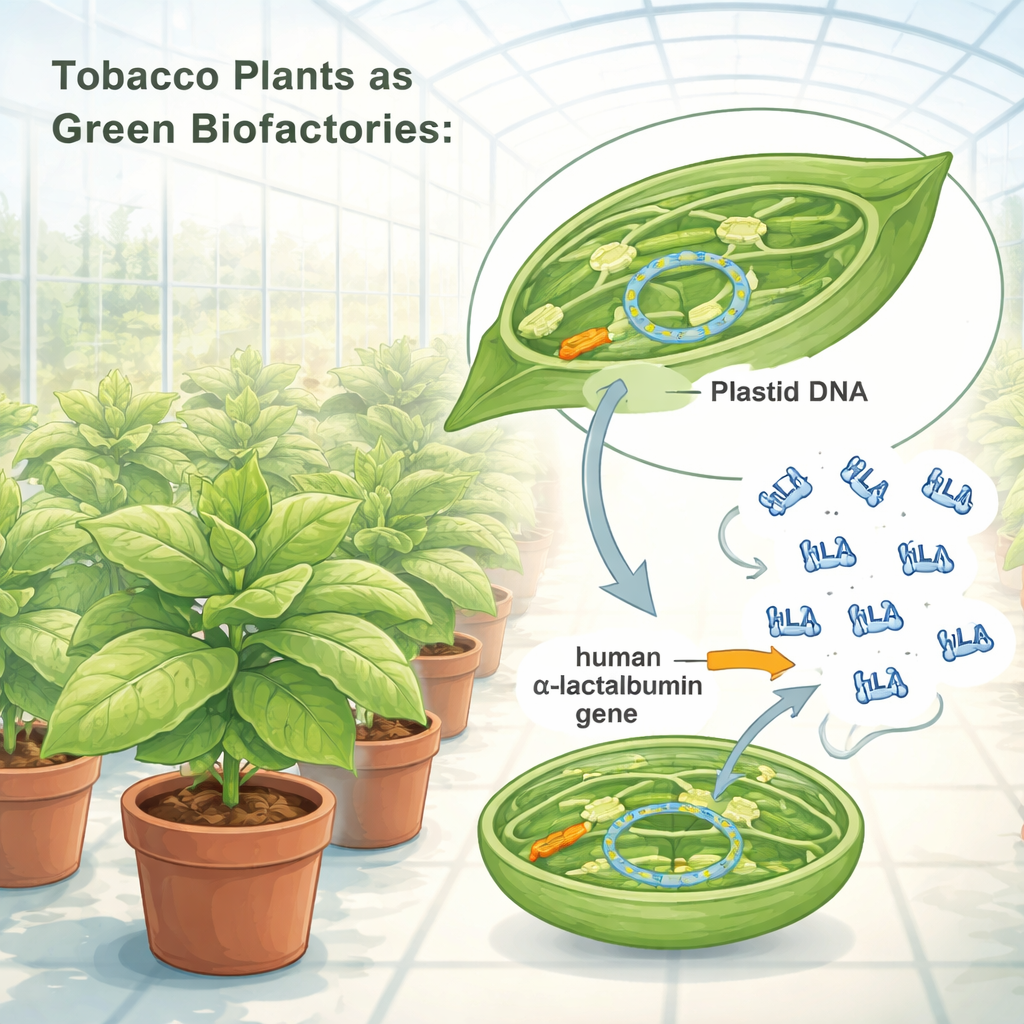
Omprogrammering av kloroplaster till biobruk
Forskarna redesignade de genetiska instruktionerna för human α‑laktalbumin så att tobakskloroplaster effektivt kunde läsa dem. De infogade denna optimerade gen i kloroplast‑DNA med en ”genkassett” byggd av starka växtregulatoriska element som fungerar som kraftfulla på/av‑strömbrytare. Med en partikel‑bombardementsmetod levererade de kassetten till tobaksbladceller och selekterade sedan plantor vars kloroplaster fullständigt antagit den nya genen. Genetiska tester bekräftade att alla kopior av kloroplast‑DNA i dessa växter nu bar den mänskliga proteinens ritning. De modifierade växterna växte normalt i växthusförhållanden, producerade frön och visade inga synliga nackdelar i storlek, form eller fertilitet, vilket antyder att den extra proteinbelastningen inte skadade växtens hälsa.
Att bevisa att växtframställt protein fungerar
Nästa fråga var om det växtframställda α‑laktalbuminet uppträdde som det mänskliga proteinet. De extraherade lösliga proteiner från bladen, renade α‑laktalbuminet och undersökte dess struktur med en teknik som berättar hur proteiner veckas. Den spektrala ”fingeravtrycket” för det växtframställda proteinet överlappade nästan helt med kommersiellt human α‑laktalbumin, vilket indikerar liknande veckning. Funktionellt aktiverade det växtframställda proteinet laktossyntetiserande enzym nästan lika effektivt som den nativen versionen och drev laktosbildning i ungefär 93 % av takten hos standardproteinet. Anmärkningsvärt ackumulerade α‑laktalbumin till cirka 23 % av allt lösligt protein i bladen—bland de högsta nivåerna rapporterade för humanproteiner framställda i växtkloroplaster—vilket tyder på att detta system kan leverera industriellt relevanta avkastningar.
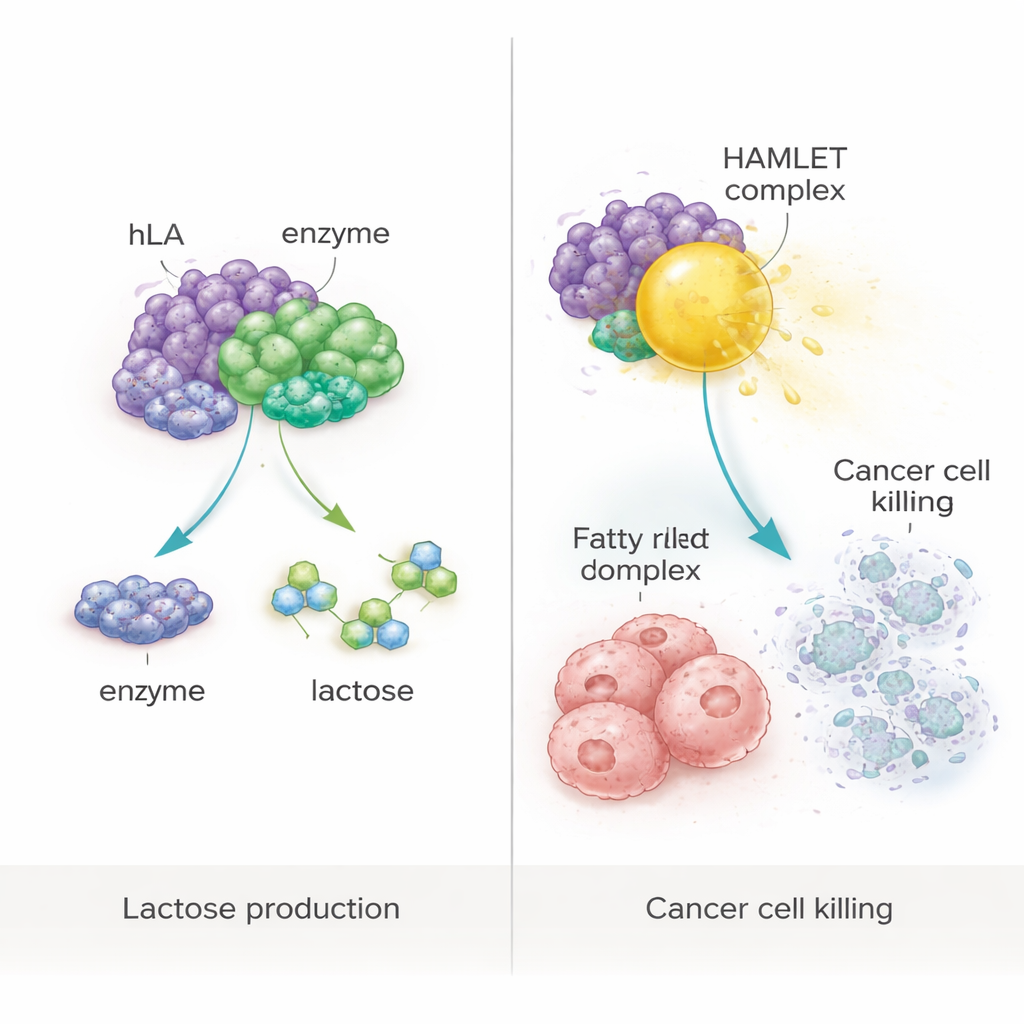
Från näring till cancerbekämpande komplex
Studien testade också en mer ambitiös idé: att använda det växtframställda proteinet som byggsten i ett känt anti‑cancerkomplex kallat HAMLET, som bildas när α‑laktalbumin binder tätt till oljesyra, en vanlig fettsyra. Genom att försiktigt värma det renade växtproteinet med oljesyra under kontrollerade förhållanden skapade forskarna ett HAMLET‑liknande komplex. När detta applicerades på humana kolorektalceller (WiDr) och bröstcancerceller (MCF‑7) i odling minskade komplexet dramatiskt cellöverlevnaden till under 10 %. Uppföljande analyser visade att majoriteten av de påverkade cellerna genomgick apoptos, en form av programmerad celldöd snarare än okontrollerad ruptur. Viktigt är att varken proteinet ensamt, fettsyran ensam eller extrakt från omodifierade växter utlöste betydande celldöd, vilket bekräftar att den cancer‑dödande effekten berodde på det specifika komplexet.
Vad detta kan innebära för framtida livsmedel och läkemedel
Sammanfattningsvis visar arbetet att växtkloroplaster på ett tillförlitligt sätt kan producera stora mängder av ett humanmjölksprotein som både är näringsmässigt relevant och terapeutiskt aktivt. För en icke‑specialist innebär detta att framtida modersmjölksersättningar, funktionella livsmedel eller kosttillskott en dag kan framställas med proteiner odlade i blad snarare än hämtade från kor, vilket minskar miljöpåverkan samtidigt som man närmar sig människans egen biologi. Samtidigt kan samma växtframställda protein omvandlas i laboratoriet till ett riktat anti‑cancerkomplex, vilket antyder växtbaserade produktionslinjer för prisvärda bioterapeutika. Mer forskning krävs för att bekräfta säkerhet och prestanda i djur och människor—och för att överföra teknologin till ätbara grödor—men studien ger en övertygande inblick i hur växter kan fungera som mini‑fabriker för nästa generations nutrition och medicin.
Citering: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Nyckelord: mjölkproteiner gjorda i växter, klyvoplaster som biobruk, human alpha‑laktalbumin, hållbara mejerialternativ, HAMLET cancerterapi