Clear Sky Science · sv
Integrin αv bidrar till regleringen av stelhet i vaskulära glattmuskelceller
Varför artärernas ”fjädring” spelar roll
När vi åldras eller utvecklar högt blodtryck förlorar våra stora artärer gradvis sin naturliga fjädrande förmåga och blir stelare. Denna förändring gör att hjärtat måste arbeta hårdare och ökar risken för hjärtinfarkt, stroke och andra hjärt‑kärlproblem. Forskare har länge vetat att de material som bygger upp artärväggarna — proteiner som elastin och kollagen — påverkar stelheten. Denna studie ställer en mer subtil fråga: kan muskelcellerna inne i artärväggarna själva bli stelare, och bidrar en liten familj av ytreceptorer kallade integrin αv till att hålla dessa celler, och därmed våra artärer, mer flexibla?
Muskelcellerna som formar blodflödet
Stora artärer är inte bara passiva rör. Deras mellanskikt är fyllt med vaskulära glattmuskelceller som kan dra ihop sig och slappna av för att finslipa blodflöde och tryck. Dessa celler är förankrade i en omgivande stomme som kallas extracellulär matrix. Forskarna fokuserade på en grupp förankringsmolekyler, integrin αv, som sträcker sig över cellsytan och fysiskt länkar cellens inre skelett till den yttre stommen. Tidigare arbete föreslog att integrin αv var inblandat i ärrbildning och ombyggnad av blodkärl, men det var oklart om det också styrde hur stel själva muskelcellerna blir, särskilt under påverkan av hormoner som angiotensin II som höjer blodtrycket och främjar fibros.
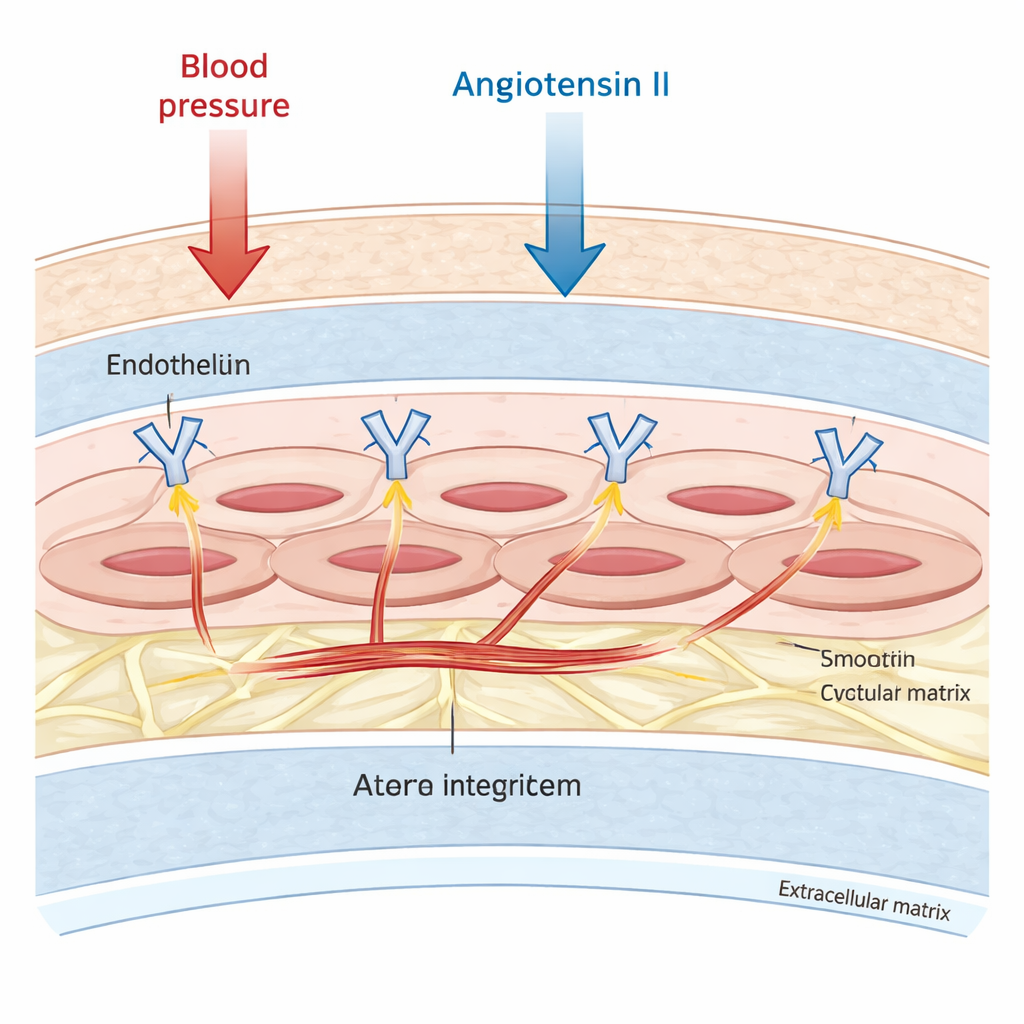
Mätning av stelhet en cell i taget
För att undersöka detta använde teamet musglattmuskelceller odlade i labb och möss som genetiskt modifierats för att sakna integrin αv specifikt i sina vaskulära muskelceller. De mätte cellernas stelhet med atomkraftsmikroskopi, en teknik där en ultrafink spets försiktigt trycker mot cellsytan och registrerar hur mycket kraft som krävs. Celler utan integrin αv var mer än två gånger så stela som kontrollceller under lugna förhållanden. När de utsattes för angiotensin II under två dagar blev dessa bristfälliga celler ungefär tre gånger stelare igen, medan normala celler knappt förändrades. Eftersom deras mätningar använde mycket ytliga intryck byggde författarna en detaljerad datormodell av en glattmuskelcell och simulerade djupare tryck. Simulationerna visade att ytliga tester betonar bidraget från cellens yttre skal och kortikala region, och ändå hamnade inom det intervall som sågs i de stela mutantcellerna, vilket stödde de biologiska fynden.
Omformat inre skelett
Nästa steg var att titta inuti cellerna. Med fluorescerande färgningar och mikroskopi undersökte forskarna aktin, ett nyckelfilament som bildar cellens interna stomme. Kontrollmuskelceller visade ett relativt diffust aktinnätverk, även efter behandling med angiotensin II. Däremot bildade celler som saknade integrin αv tjocka stressfibrer tvärs över cellen och, efter hormonpåverkan, ett intensivt band av aktin precis under cellmembranet, känt som kortikalt aktin. En kvantitativ mätning av hur mycket aktin som ansamlades nära cellkanten bekräftade att detta kortikala skikt var starkt berikat endast i de integrin‑deficienta cellerna. Dessa celler utvecklade också ovanligt långa adhesionstrukturer där de greppar kring den omgivande matrixen, förenligt med en övergång mot mer spänningsbärande, fibrillära adhesioner som kan låsa cellen i ett stelt tillstånd.
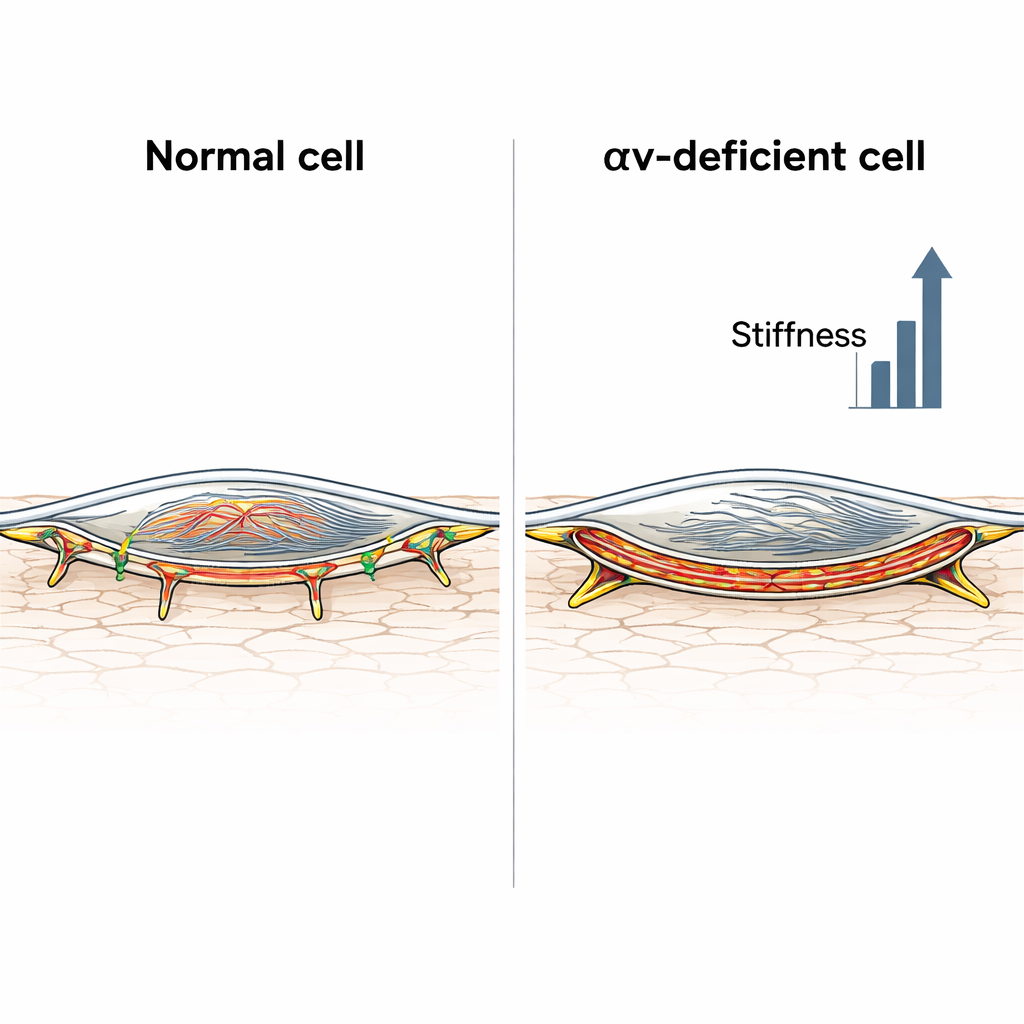
När väggen ser likadan ut men beter sig annorlunda
Etttersom artärer är mer än bara sina muskelceller mätte forskarna också mekaniska egenskaper hos carotisartärer i levande möss, med och utan integrin αv i sina vaskulära muskelceller, och med eller utan kronisk infusion av angiotensin II. Förvånande nog var det totala artärtrycket och väggstelheten — uppskattad från ultraljudsbaserade tryck‑diameterkurvor — liknande i båda musextyperna, både vid baslinje och efter hormonbehandling. Ändå skilde sig den mikroskopiska sammansättningen av väggen. Vid angiotensin II visade kontrollmöss lägre elastin och högre kollagen, klassiska tecken på en stelare matrix, medan integrin‑deficienta möss hade relativt mindre kollagenförändring men mycket stelare muskelceller. Med andra ord, i normala möss gjorde matrixen det mesta av stelningen; i integrin‑deficienta möss blev muskelcellerna själva så styva att de i praktiken kompenserade för deras mer blygsamma matrixförändringar.
Vad detta betyder för åldrande artärer
För en lekmannaläsare är huvudbudskapet att artärstelhet inte bara handlar om utslitna elastiska fibrer; det beror också på hur muskelcellerna i väggen organiserar sina små inre kablar. Integrin αv hjälper normalt till att hindra dessa celler från att bli för styva när de utsätts för hormoner som angiotensin II. När denna kontroll förloras omorganiserar cellerna sitt aktincytoskelett — särskilt i kortex precis under membranet — och låser sig i ett stelare tillstånd som kan driva artärstelhet även utan dramatiska förändringar i den omgivande matrixen. Denna insikt pekar mot nya behandlingsidéer: läkemedel som varsamt löser upp eller omorganiserar det kortikala aktinnätverket, eller som modulerar integrin‑länkad signalering, skulle en dag kunna komplettera blodtryckssänkande behandlingar för att mer direkt återställa artärernas ”fjädring”.
Citering: Bascetin, R., Belozertseva, E., Regnault, V. et al. Integrin αv contributes to the regulation of vascular smooth muscle cell stiffness. Sci Rep 16, 7682 (2026). https://doi.org/10.1038/s41598-026-38948-z
Nyckelord: arteriell stelhet, vaskulära glattmuskelceller, integrin alfa v, aktin cytoskelett, angiotensin II