Clear Sky Science · sv
Autofluorescens och FTIR-analyser spårar dietära fluoroforer och påvisar plastkontaminering i tarmen hos mygglarver
Varför denna myggstudie är viktig
Myggor är ökända för att sprida sjukdomar, men innan de någonsin suger blod tillbringar de flera dagar som små larver som äter i vattenfyllda behållare. Dessa tidiga stadier är myggans arbetsstinna tillväxtfas och ett viktigt mål för kontrollåtgärder. Denna studie visar hur forskare kan ”se” vad larverna äter — utan att tillsätta färgämnen — och till och med upptäcka spår av plast som tyst läcker från vanliga laboratoriebehållare in i deras tarmar. Resultaten är viktiga både för att utforma säkrare myggbekämpningsmetoder och för att förstå hur mikroplastföroreningar kan röra sig genom små vattenlevande djur.
Glödande ledtrådar inuti små kroppar
Många naturliga molekyler lyser svagt när de belyses med vissa ljusfärger, en egenskap som kallas autofluorescens. Forskarna utnyttjade denna inneboende glöd för att spåra föda i larver av den asiatiska tigermyggan, en viktig vektor. Med kraftfulla mikroskop och spektral avbildning undersökte de kommersiellt larvfoder, larvtarmar och tunna vävnadsskivor. Fodret visade två huvudsakliga glödsignaler: ett brett blåaktigt band från proteinrikt material och ett skarpt rött band från klorofyllrelaterade pigment härstammande från växter och alger. När larverna åt detta foder visade deras tarminnehåll samma signaturer, vilket bekräftar att dessa ljussignaler kan fungera som naturliga markörer för vad de har intagit.
Föda pigment läcker ut ur tarmen
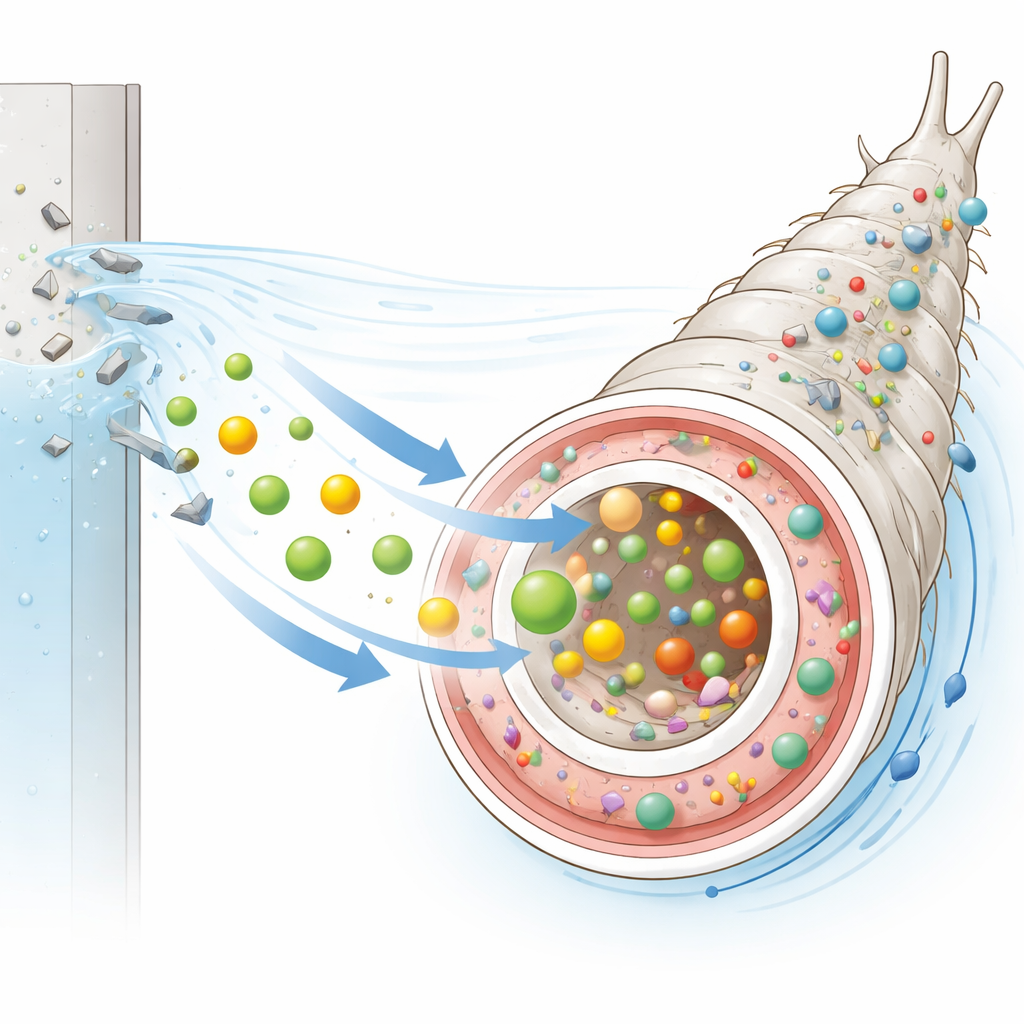
Genom att zooma in med konfokalmikroskopi fann teamet något mer överraskande: den röda klorofyll-liknande signalen var inte begränsad till tarmens lumen. Den förekom också i den omgivande kroppshålan, men inte i den yttre kutikulan. Detta mönster tyder på att vissa födoderiverade pigment överlever nedbrytning och rör sig in i interna kroppsvätskor, med potentiell ackumulering i andra vävnader. Samma röda emission detekterades även i vattnet där larverna hade fötts upp, trots att den saknades i vatten som innehöll enbart foder. Detta indikerar att larver tar upp klorofyllrelaterade föreningar och senare släpper tillbaka en del till sin omgivning, vilket ger ett sätt att följa hur naturligt fluorescerande dietkomponenter cirkulerar genom djuret och dess livsmiljö.
Behållarmaterial påverkar vad larver tar upp
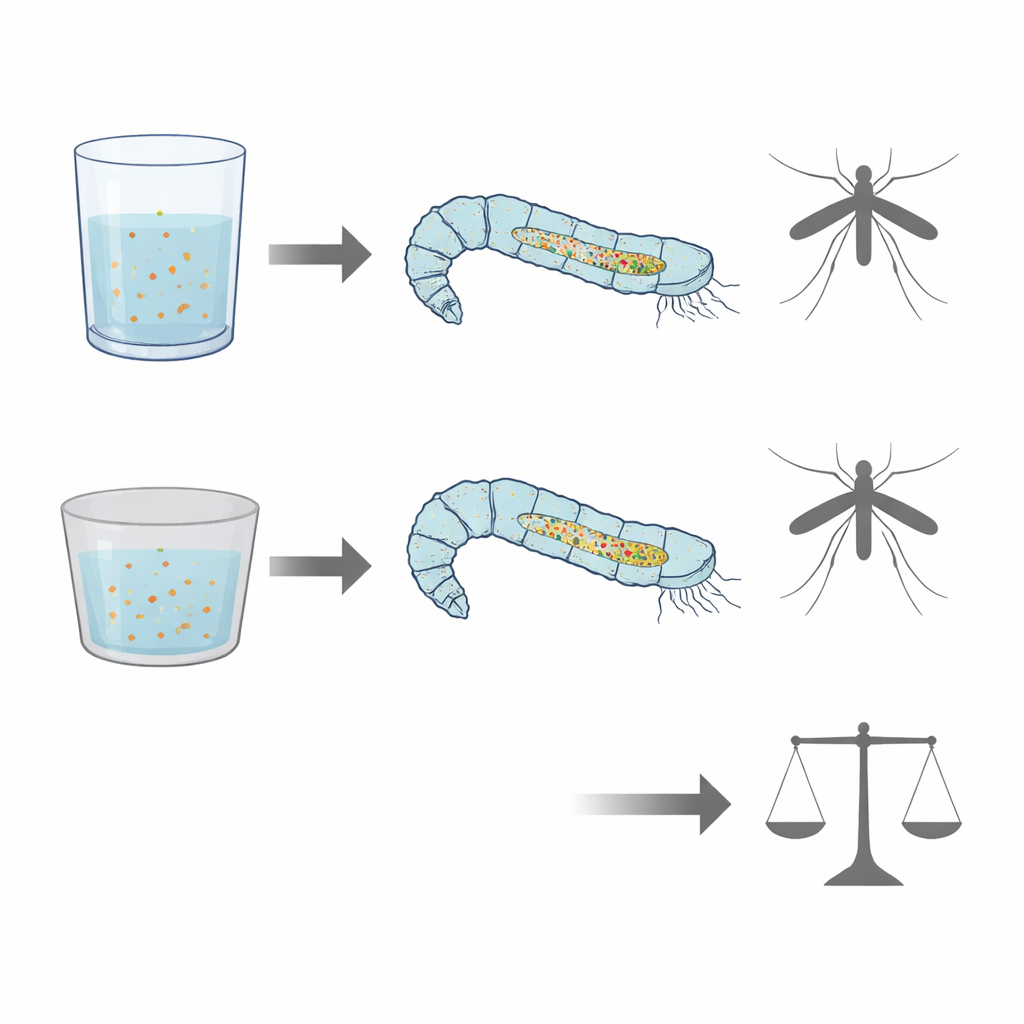
För att testa hur uppfödningsmiljön kan påverka födointaget odlades larver antingen i glasskålar eller i polystyrenplastskålar under identiska förhållanden. Den totala glöden från föda i tarmen var konsekvent starkare och mer omfattande hos larver från plastbehållare än hos dem från glas, vilket antyder skillnader i hur mycket eller hur effektivt de åt eller bearbetade sin diet. Spektrofluorimetri av omgivande vatten visade förändringar i en annan grupp lysande föreningar, flaviner, som är kopplade till energimetabolism och B-vitaminer. Dessa förändringar tyder på att larver uppfödda i olika behållarmaterial kan hantera vissa näringsämnen olika, även när deras foder är detsamma.
Dolda plastfingeravtryck i tarmen
Utöver ljusbilder använde forskarna en teknik kallad ATR-FTIR-spektroskopi för att läsa kemiska ”fingeravtryck” från larvtarmar och uppfödningsmaterial. Tarmar från larver uppfödda i plastskålar visade en distinkt signal i det infraröda området som nära matchade ett kännetecken för polystyren och av larver experimentellt exponerade för polystyrenkulor. Denna topp saknades i tarmar från larver uppfödda i glas och i själva fodret, vilket starkt talar för närvaron av plastderiverat material i larver som fötts upp i plastbehållare. Även om svepelektronmikroskopi inte visade uppenbara bettspår eller skrapskador på insidan av skålarna, har tidigare arbete visat att plast kan avge mikroskopiska och till och med nanoskiktfragment vid normal användning, vilka kan tas upp av vattenlevande organismer.
Vad detta betyder för myggkontroll och föroreningar
Trots dessa subtila kemiska och optiska skillnader förändrades standardmått som larvöverlevnad, utvecklingstid och vuxen kroppsstorlek lite mellan grupperna uppfödda i glas respektive plast, förutom en blygsam förskjutning i larvens utvecklingstid. För en oinvigd observatör skulle myggorna framstå som nästan identiska. Ändå berättar deras tarmar en mer komplex historia: de skiljer sig i hur mycket födoanknutet sken de bär, hur de bearbetar vissa vitaminer och växtpigment, och huruvida plastfragment har trängt in i deras vävnader. För vektorkontrollprogram som förlitar sig på massuppfödning av myggor — särskilt de som använder steril insekt-teknik — kan sådana dolda effekter påverka långsiktig prestanda och hälsa. Mer generellt visar arbetet att naturlig fluorescens och infraröd spektroskopi kan fungera som känsliga, icke-destruktiva verktyg för att övervaka diet, uppfödningsförhållanden och plastförorening i små vattenlevande djur. Dessa metoder kan bidra till att förfina grönare larvkontrollstrategier och fördjupa vår förståelse av hur mikroplaster tyst rör sig genom sötvattens-ekosystem.
Citering: Soldano, S., Weththimuni, M.L., Oldani, A. et al. Autofluorescence and Fourier transform infrared analyses trace dietary fluorophores and reveal plastic contamination in the gut of mosquito larvae. Sci Rep 16, 7841 (2026). https://doi.org/10.1038/s41598-026-38938-1
Nyckelord: mygglarver, autofluorescens, mikroplaster, klorofyllpigment, vektorkontroll