Clear Sky Science · sv
Encells‑differensmätningar av massdensitet med hjälp av mikrokanalgradient‑centrifugering
Varför det spelar roll att väga pyttesmå celler
Varje levande cell är mer än bara en säck med molekyler; dess vikt och hur kompakt den är berättar något om dess tillstånd. Subtila förändringar i hur tätt packad en cell är kan signalera om den växer, dör, bekämpar en infektion eller håller på att bli cancerös. Trots denna potential har mätningar av massdensiteten hos tusentals individuella celler varit långsamma, tekniskt krävande och kostsamma. I den här artikeln presenteras ett nytt, mycket enklare sätt att " väga" enstaka celler genom att observera hur de flyter eller sjunker i en kontrollerad vätska inne i en hårfin glaskanal som snurras i en centrifug.
En ny variant på ett gammalt labbtrick
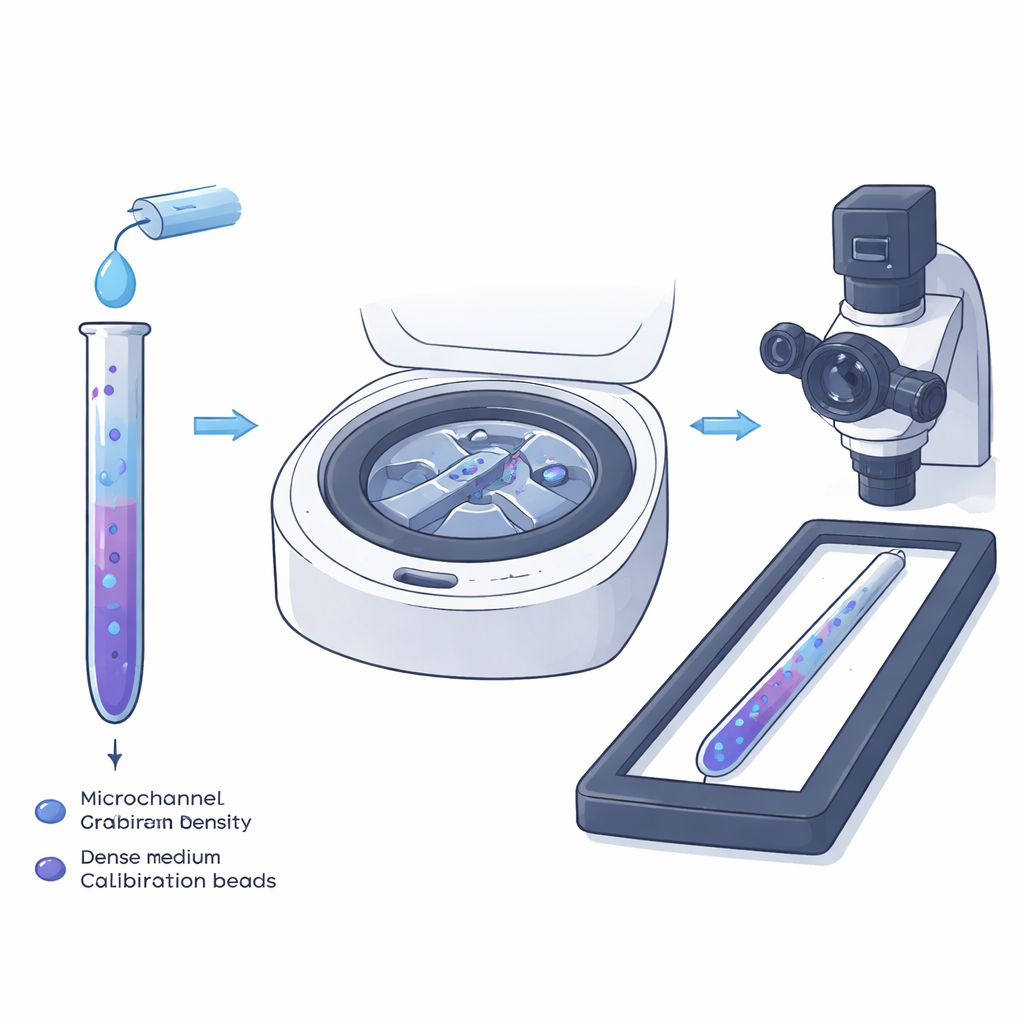
Traditionell densitetsgradientcentrifugering har länge använts i provrör för att separera blandningar av celler: när de snurras sjunker cellerna till den plats i ett lagerat vätskasystem där deras egen densitet matchar omgivande vätska. Författarna miniaturiserar idén till en smal mikrokanal så att enskilda celler, inte bara lager, kan mätas direkt i ett mikroskop. De fyller kanalen först med en lätt vätska innehållande cellerna och därefter med en tyngre vätska innehållande små plastpartiklar med exakt kända densiteter. När dessa två vätskor möts och flyter i den lilla kanalen bildas naturligt en jämn, endimensionell densitetsgradient längs kanalens längd.
Skapa en jämn lutning av densitet
I sådana tunna kanaler flyter vätskan långsamt och jämnt, utan turbulens. Under dessa förhållanden blandar parabolprofilen i flödet den lätta och den tunga vätskan precis så mycket att en gradvis övergång, snarare än en skarp gräns, bildas mellan dem. Teamet studerade denna process både experimentellt med en fluorescerande färg och genom datorsimuleringar. De fann att en nästan linjär densitetsgradient som sträcker sig flera millimeter kan formas inom sekunder. Kanalhöjden visade sig vara avgörande: grunda kanaler håller gradienten stabil och förhindrar tyngdkraftsdriven gungning av den tyngre vätskan, vilket annars skulle sudda ut sambandet mellan position och densitet och introducera fel i de slutliga cellmätningarna.
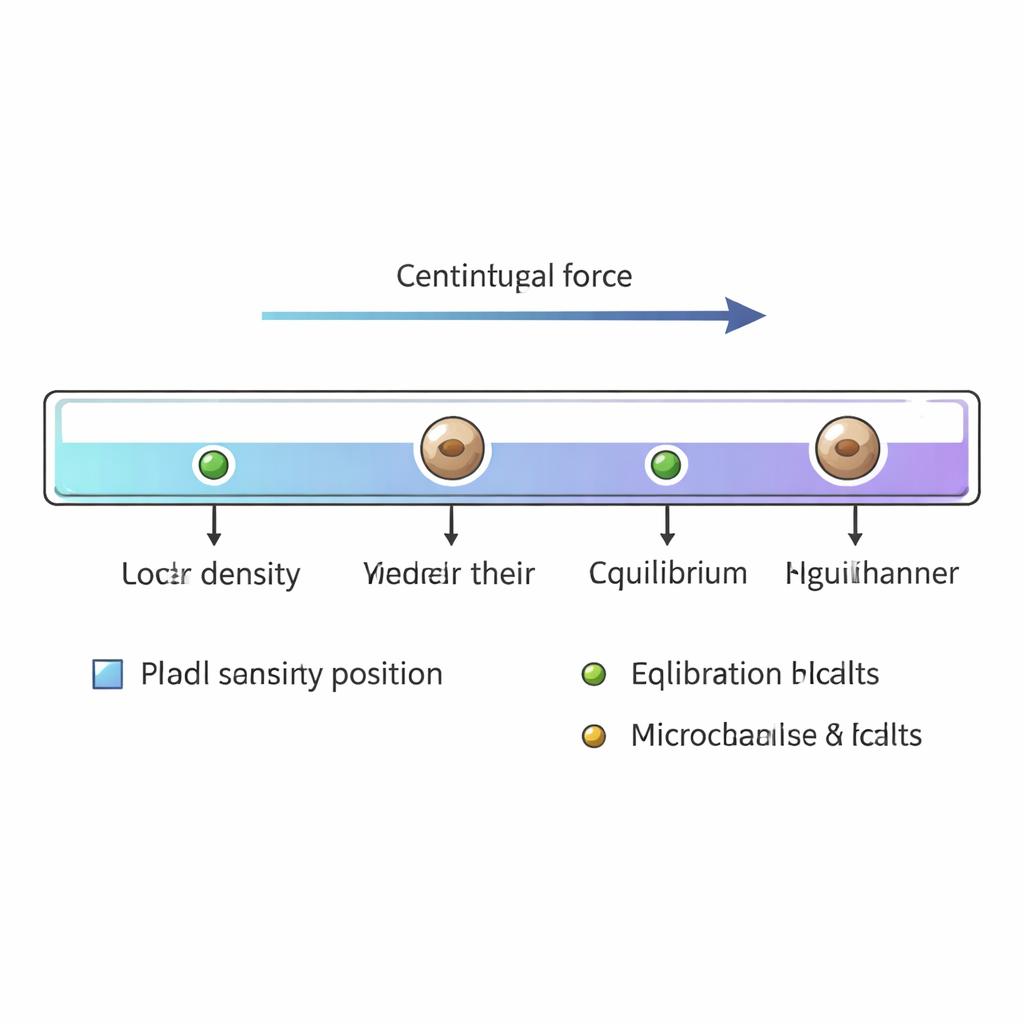
Snurra cellerna till deras balanspunkt
När kanalen är fylld förseglas ändarna och den placeras i en liten centrifug. Vid ungefär 12 000 varv per minut rör sig celler och kalibreringspärlor längs kanalen tills den utåtriktade kraften från snurrningen är exakt balanserad av lyftkraften vid deras specifika densitet. Jästceller större än cirka tre mikrometer i diameter når detta jämviktstillstånd på under 20 sekunder. Efter ungefär en och en halv minut snurrning tas kanalen ut och skannas i ett vanligt mikroskop. Forskarna registrerar positionerna för tusentals enskilda jästceller och referenspärlorna, och omvandlar sedan varje position längs gradienten till ett massdensitetsvärde med hjälp av pärlornas kända densiteter som ankare.
Läsa av cellhälsa från små skillnader
Med denna metod mätte författarna densiteterna hos mer än 20 000 jästceller över flera kanaler. Den typiska mätosäkerheten för en enskild cell var ungefär 3,3 kilogram per kubikmeter—tillräckligt liten för att urskilja verkliga biologiska skillnader, som i deras prover var ungefär dubbelt så stora. Under många timmar observerade de att huvudpopulationen av jäst höll en stabil densitet, medan en andra, tätare och något mindre population gradvis dök upp. Denna tätare grupp bestod sannolikt av döda eller skadade celler som tagit upp den tunga vätskan och blivit mer kompakta. De uppmätta värdena överensstämde väl med resultat från avsevärt mer komplexa och långsamma tekniker såsom suspended microchannel resonators, optiska metoder och magnetisk levitation.
Från labbprototyp till praktisk biomarkör
Studien visar att en enkel kombination av glasmikrokanaler, vanliga centrifuger och standardmikroskop kan leverera höggenomströmning, encelliga densitetsmätningar vid hastigheter runt 16 000 celler per timme. Även om metoden ännu inte är tillräckligt känslig för att fånga de allra minsta läkemedelsinducerade förändringarna, är den redan kraftfull nog att skilja olika celltyper åt eller levande från döda celler baserat på hur tätt packade de är. Genom att göra precis cell"vägning" mer tillgänglig och prisvärd kan denna mikrokanalgradientmetod bidra till att göra cellmassdensitet till en rutinmässig biomarkör för övervakning av sjukdom, utvärdering av behandlingar och utforskning av hur celler reglerar sitt inre innehåll.
Citering: Soller, R., Augustsson, P. & Barnkob, R. Single-cell mass-density measurements using microchannel gradient centrifugation. Sci Rep 16, 6501 (2026). https://doi.org/10.1038/s41598-026-38872-2
Nyckelord: densitet hos enstaka celler, mikrofluidik, centrifugering, jästceller, cell‑biomarkörer