Clear Sky Science · sv
Konformationsdynamik och analyser av bindningsfri energi avslöjar en stabil flavonoidhämmare av denguevirusets NS5-polymeras
Varför ett myggburet virus behöver växtbaserad hjälp
Denguefeber har exploderat globalt de senaste åren, smittat miljontals och dödat tusentals. Ändå saknar vi fortfarande en allmänt effektiv, prisvärd antiviral tablett för att behandla infekterade personer. Denna studie ställer en förrädiskt enkel fråga med stora konsekvenser: kan naturligt förekommande växtkemikalier förvandlas till precisa molekylära "hylsnycklar" som sätter igen en av denguevirusets viktigaste maskiner?
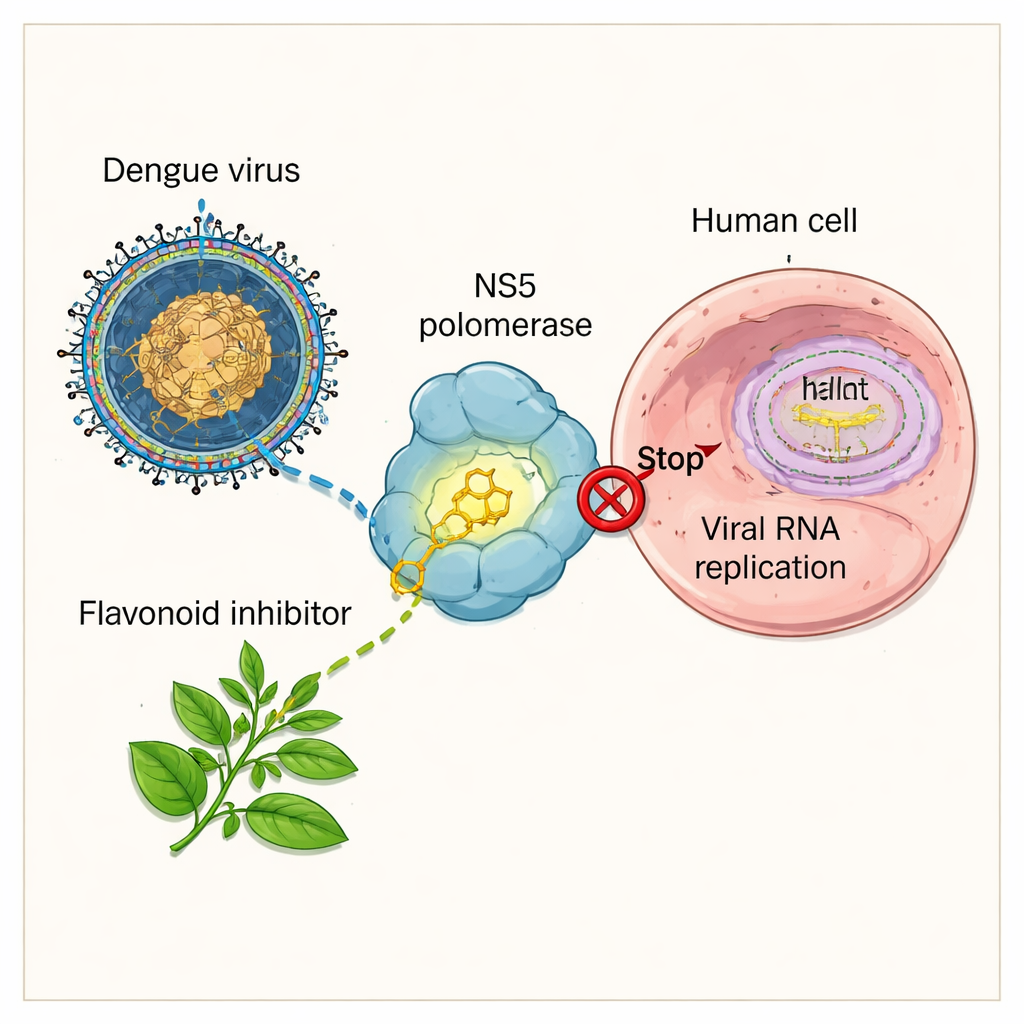
Virusmotorn som forskarna vill stänga av
Denguevirus överlever genom att kopiera sitt genetiska material inne i våra celler. För detta litar det på ett nyckelprotein kallat NS5, som fungerar som en liten kopieringsmotor för virusets RNA. Om NS5 slutar fungera kan viruset inte göra nya genom och infektionen avstannar. Läkemedelsutvecklare ser därför NS5—särskilt dess RNA-kopierande region, känd som RNA-beroende RNA-polymeras—som ett primärt mål för nya läkemedel. Flera syntetiska kemikalier och växtextrakt har redan visat att NS5 kan blockeras, men många av dessa tidiga kandidater binder svagt, är ostadiga eller väcker frågor om säkerhet och hur väl de distribueras i kroppen.
Att söka i växter efter lovande kemiska nålar i en höstack
Forskarna fokuserade på flavonoider, en stor familj av växtföreningar som finns i livsmedel som bär, te och örter, och som länge varit kända för antivirala och antiinflammatoriska effekter. Från en kurerad databas över växters sekundära föreningar plockade de ut 326 flavonoider och förberedde tredimensionella modeller av både virusets NS5-enzym och varje kandidatmolekyl. Genom stegvis datorbaserad dockning frågade de: vilka former passar bäst in i en specifik "bakdörr"-region på NS5 kallad N-fickan—en allosterisk plats som kan stänga av enzymet när den upptas, och som tenderar att mutera mindre än det huvudsakliga aktiva stället?
Vid varje steg i denna virtuella screening gallrades föreningar bort som passade dåligt eller verkade osannolika att uppföra sig som verkliga läkemedel i kroppen. De kvarvarande molekylerna poängsattes sedan inte bara på geometrisk passform, utan också på uppskattad bindningsstyrka med en metod som approximerar de energier som är involverade när en förening fäster vid NS5 i vattenliknande, celllika förhållanden. Denna process begränsade fältet till ett fåtal toppflavonoider, där en kandidat, märkt PSCdb01560, stod ut för sin särskilt starka förutsagda bindningsenergi.
Att iaktta molekyler röra sig i ett virtuellt mikroskop
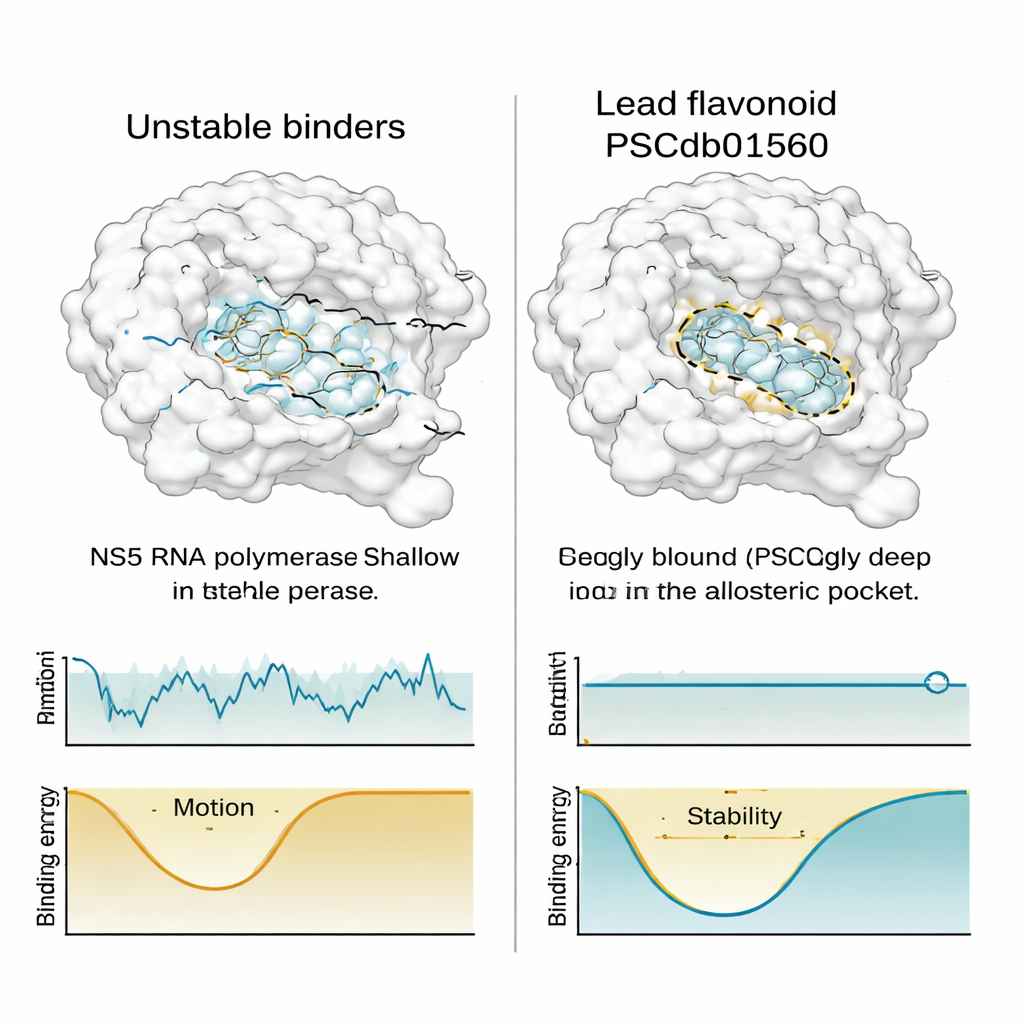
Att passa bra i en statisk ögonblicksbild räcker inte; ett användbart läkemedel måste också stanna kvar när allt skakar i verkligheten. För att testa detta körde teamet långa, detaljerade molekylärdynamiksimuleringar—datorfilmer motsvarande en halv mikrosekund—för NS5 ihop med de bästa flavonoiderna och en känd referenshämmare. De följde hur mycket proteinet och varje förening svajade, hur tätt packat komplexet förblev, hur utsatt det var för omgivande vatten och hur ofta viktiga kemiska kontakter bildades och bröts. PSCdb01560 visade anmärkningsvärt stabilt beteende: det satt djupt i N-fickan, rörde sig mycket lite jämfört med rivalerna och verkade stabilisera NS5:s övergripande form snarare än rubba den.
Tvärtom började två andra flavonoider som initialt verkade lovande driva iväg inom fickan eller bli mer exponerade för lösningsmedlet över tid—tecken på svagare, mindre tillförlitlig bindning. När forskarna kartlade varje kompleks "frienergimlandskap"—ett sätt att visualisera vilka konformationer som är termodynamiskt gynnade—fann de att PSCdb01560 intog en djup, väl definierad energidal, medan de mindre stabila föreningarna hoppade mellan flera grundare bassänger. När de jämförde de lägsta energins ögonblicksbilder med de ursprungliga dockade positionerna förändrades PSCdb01560:s läge knappt, vilket understryker dess konformationslojalitet.
Siffror som antyder läkemedelslik styrka
Slutligen använde teamet ett energiberekningsramverk för att uppskatta hur starkt varje flavonoid skulle binda efter att all simulerad rörelse tagits i beaktande. PSCdb01560 uppnådde en bindningsfri energi som var mer fördelaktig än den etablerade referensföreningen, drivet av en kombination av tätt formkomplement, attraktiva elektriska interaktioner och olje-liknande kontakter inne i fickan. Det här mönstret—stark beräknad affinitet, stabil position över tid, begränsad intern flexibilitet och engagemang av viktiga NS5-residuer som delas över dengue-stammar—utpekar PSCdb01560 som en särskilt övertygande startpunkt för läkemedelsdesign.
Vad detta kan innebära för framtida denguebehandlingar
Dessa resultat levererar ännu inte en tablett mot dengue, men de snävar av sökandet avsevärt. Arbetet identifierar en växtbaserad flavonoidskallett som i datoranalyser presterar bättre än flera konkurrenter och till och med en känd referenshämmare vad gäller både stabilitet och förutsagd bindningsstyrka. Nästa steg är experimentella: att testa om PSCdb01560 verkligen blockerar NS5 i provrör, stoppar dengue från att replikera i infekterade celler och visar sig säker i djurmodeller. Om dessa hinder klaras kan kemister finjustera denna flavonoid till ett kliniskt användbart antiviral. För nu ger studien ett hoppfullt budskap: naturens eget kemiska bibliotek rymmer fortfarande lovande verktyg för att avväpna ett av världens snabbast växande myggburna hot.
Citering: Alsaady, I.M., Gattan, H.S., Aljahdali, S.M. et al. Conformational dynamics and binding free energy analyses unveil a stable flavonoid inhibitor of dengue virus NS5 polymerase. Sci Rep 16, 7761 (2026). https://doi.org/10.1038/s41598-026-38864-2
Nyckelord: denguevirus, NS5-polymeras, flavonoidhämmare, upptäckt av antivirala läkemedel, molekylär dockning