Clear Sky Science · sv
Kadmium framkallar ferroptos i musens spermatocyter genom att aktivera ROS–TCA‑vägen
Varför ett vanligt metall spelar roll för mäns hälsa
Kadmium är en mjuk metall som används i batterier, pigment och andra industriprodukter. Den kan ansamlas i jord, vatten och mat och tyst ta sig in i våra kroppar över tid. Många studier har kopplat kadmiumexponering till lägre spermieantal och sämre spermiekvalitet hos män, men exakt hur det skadar cellerna som bildar spermier har förblivit oklart. Denna studie zoomar in på problemet och avslöjar hur kadmium driver musens spermatocyter in i en särskild dödsväg kopplad till järn och ett stressat energisystem inne i mitokondrierna, cellens kraftverk.
Från förorening till sårbara spermieceller
Kadmium är en välkänd miljöbov för det manliga reproduktionssystemet. Män som utsätts på jobbet eller bor i förorenade områden visar ofta minskat spermieantal, sämre rörlighet och avvikande form, och till och med DNA‑skador i sperman. Djurstudier speglar dessa fynd och visar förminskade testiklar, läckande skyddande barriärer, låga testosteronnivåer och utbredd förlust av könsceller. Författarna observerade tidigare att kadmium kan utlösa en ovanlig, järnavhängiga form av celldöd kallad ferroptos i testikulär vävnad. I det nuvarande arbetet fokuserade de på musens spermatocyter — celler mitt i spermieutvecklingen — för att se exakt hur kadmium skadar dem och om denna järnkopplade dödsväg är inblandad.
Järnöverskott och en speciell form av celldöd
För att undersöka detta odlade teamet en cellinje av mus‑spermatocyter i petriskålar och exponerade dem för kadmium, med eller utan läkemedel som är kända för att blockera ferroptos. Kadmium halverade cellöverlevnaden ungefär och saktade ner celldelningen. Inne i cellerna ökade nivåerna av fritt järn och en markör för fettförstörelse kallad malondialdehyd kraftigt, medan ett viktigt skyddande enzym, GPX4, sjönk. Andra proteiner som är involverade i järnlagring och export ökade, vilket signalerade att järnhanteringen var kraftigt rubbad. När forskarna tillsatte ferroptos‑hämmare — ett järnbindande ämne och en lipid‑skyddande molekyl — lindrades många av dessa skadliga förändringar och cellöverlevnaden förbättrades. Tillsammans motsvarar dessa skift signaturen för ferroptos och visar att kadmium inte bara dödar celler på ett vagt sätt, utan driver dem in i detta särskilda järn‑ och lipiddrivna dödsprogram.
Mitokondrier under belägring
Berättelsen fördjupades när forskarna riktade uppmärksamheten mot mitokondrierna, energicentra som också genererar reaktiva syreföreningar, eller ROS, som biprodukter. Under mikroskopet visade friska spermieceller långa, trådliknande mitokondrier, men kadmiumexponerade celler uppvisade korta, fragmenterade mitokondrier, ett tecken på strukturell skada. Mätningar bekräftade att mitokondriell ROS skjöt i höjden, medan den elektriska laddningen över mitokondriemembranet — en nyckelindikator på funktion — sjönk. Cellerna svarade genom att skruva upp interna försvarssystem, inklusive proteiner styrda av stressens sensor Nrf2, men dessa försvar räckte inte till. Viktigt är att ferroptos‑hämmarna minskade mitokondriell ROS och delvis återställde mitokondriernas hälsa, vilket kopplar de skadade kraftverken direkt till den järnavhängiga dödsvägen.
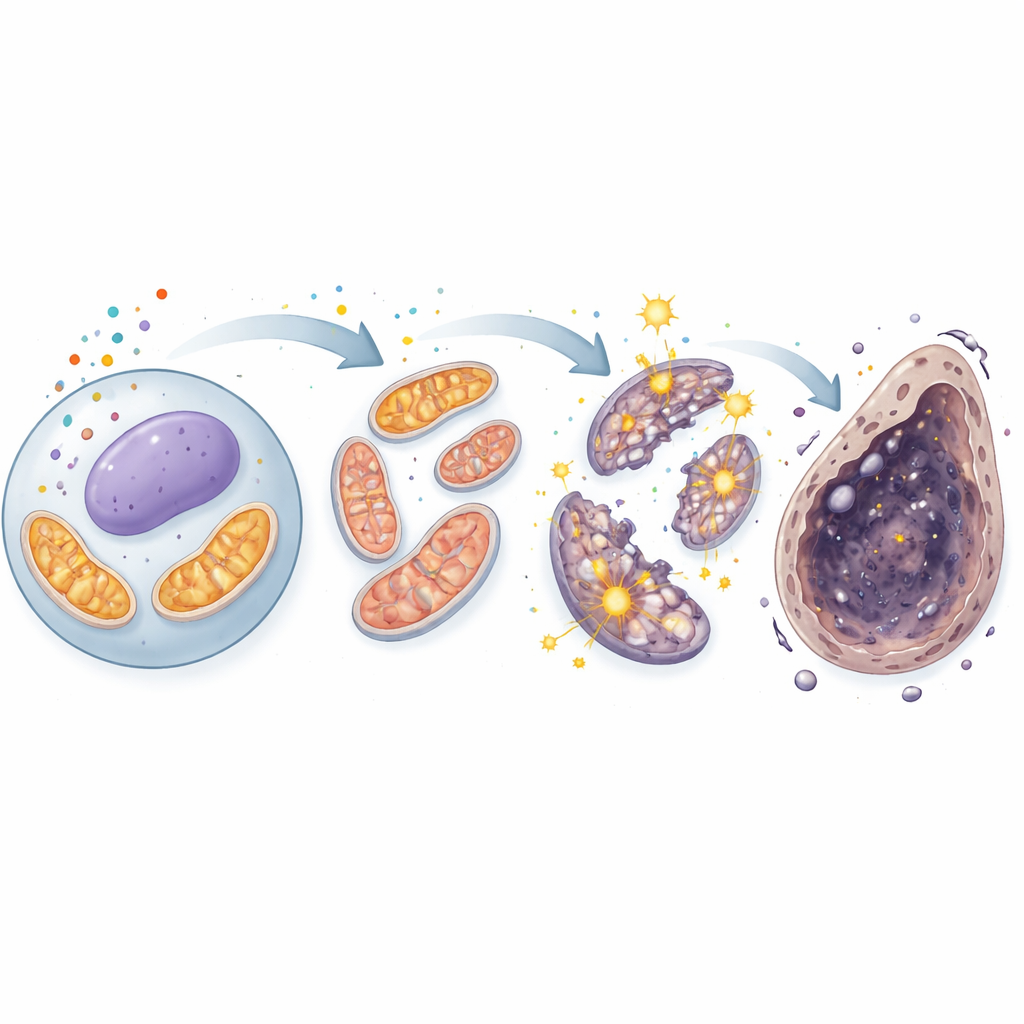
En ond cirkel i cellens kraftverk
Med en kombination av genuttrycksprofilering och mätningar av metaboliter såg forskarna att kadmium gjorde mer än att bara skada mitokondrierna — det verkade kapa deras grundläggande energikrets, trikarboxylsyracykeln (TCA‑cykeln). Nivåerna av två centrala TCA‑intermediärer, alfa‑ketoglutarat och succinat, ökade signifikant, och aktiviteten hos pyruvatkarboxylas, ett enzym som matar ny bränsle in i cykeln, var uppreglerad. Detta tyder på att TCA‑cykeln paradoxalt nog blev överaktiv i de skadade cellerna, vilket pressade fler elektroner genom andningskedjan och läckte mer ROS i processen. Den extra ROS:en matade sedan tillbaka in i järnkemin och membranskador, vilket förstärkte ferroptos. Återigen dämpade ferroptos‑hämmare dessa metabola störningar, vilket underströker den täta kopplingen mellan kadmium, mitokondriell överdrift och järnavhängigt celldöd.
Vad detta betyder för fertilitet och framtida forskning
Enkelt uttryckt visar studien att kadmium angriper spermiebildande celler genom att direkt skada deras mitokondrier och sätta deras energicykel i skadlig övervarvning. Denna kombination översvämmar cellerna med reaktiva syremolekyler och rubbar järnbalansen, vilket pressar dem in i ferroptos. Eftersom spermatocyter är nödvändiga för att producera friska spermier kan deras förlust bidra till att förklara varför kadmiumexponering är så starkt kopplad till minskad manlig fertilitet. Även om dessa experiment utfördes i musceller i odlingsskålar ger de en tydlig mekanistisk karta som framtida djur‑ och humanstudier kan pröva. Arbetet lyfter också fram potentiella skyddsstrategier: läkemedel eller näringsämnen som lugnar mitokondriell stress, finjusterar TCA‑cykeln eller förhindrar järn‑driven membranskada kan hjälpa till att skydda det manliga reproduktionssystemet från miljömetaller som kadmium.
Citering: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
Nyckelord: kadmiumtoxiskhet, manlig fertilitet, mitokondriell stress, ferroptos, reaktiva syreföreningar