Clear Sky Science · sv
Restnivåbestämmande faktorer för termisk stabilitet hos den extremofila Ts2631-endolisynen
Varför värmekärleksfulla virus spelar roll för framtida antibiotika
När antibiotikaresistensen ökar tävlar forskare för att hitta nya sätt att döda farliga bakterier. En lovande metod lånar vapen från virus som infekterar bakterier, så kallade bakteriofager. Dessa virus producerar enzymer, kallade endolysiner, som gör hål i bakteriens cellväggar. Studien som här diskuteras fokuserar på en anmärkningsvärt värmetålig endolisyn, Ts2631, från ett virus som lever i isländska varma källor. Genom att kartlägga vilka enskilda byggstenar i detta protein som gör det stabilt vid nästan kokpunkten hoppas forskarna kunna utforma tåligare, mer långlivade antibakteriella enzymer för medicin och bioteknik. 
Ett viralt verktyg smitt i kokande varma källor
Ts2631 kommer från en bakteriofag som infekterar den värmekärleksfulla bakterien Thermus scotoductus, som trivs i vatten som når långt över 60 °C. Ts2631-enzymet klyver en specifik bindning i peptidoglykanet, det tåliga nätverk som omger bakterieceller. Det som gör Ts2631 särskilt är dess extrema termostabilitet: det förblir vikt tills ungefär 100–105 °C, beroende på lösningen. Det är långt över de temperaturer där de flesta proteiner faller sönder. Författarna jämförde Ts2631 med dess mest studerade släkting från ett måttligt temperaturvirus, T7-lysozym, för att lista ut vilka strukturella knep naturen använt för att hålla Ts2631 intakt under så hårda förhållanden.
Kortare slingor och en annorlunda sammansättning av byggstenar
Proteiner är kedjor av 20 typer av aminosyror som viks till intrikata former. När forskarna lade 3D-strukturerna för Ts2631 och T7-lysozym ovanpå varandra fann de att den övergripande arkitekturen är mycket lik: båda har en kompakt kärna av helixar och strängar. Nyckelskillnaden ligger i de flexibla slinga-regionerna som förbinder dessa element. I Ts2631 är dessa slingor kortare och visar lägre flexibilitet, medan T7-lysozym har längre, mer sladdriga slingor. Ts2631 innehåller också fler av vissa aminosyror som ofta kopplas till värmetålighet: den styva prolinen; aromatiska resternas som tyrosin och tryptofan; och den positivt laddade argininen. Samtidigt har det färre serin-, asparaginsyra- och glutaminsyrarester, som kan göra proteiner mer sårbara vid höga temperaturer. Detta mönster gäller inte bara i jämförelse med T7-lysozym utan även när Ts2631 ställs mot hundratusentals virala och många miljoner bakteriella proteiner.
Byta enstaka aminosyror för att testa deras betydelse
För att gå från korrelation till orsakssystematik bytte teamet systematiskt ut 55 individuella aminosyror i Ts2631 och mätte hur varje mutation påverkade smältpunkten (Tm) och enzymets förmåga att bryta ner bakteriens cellvägg. Vissa förändringar kring det zinkinnehållande aktiva sätet var särskilt skadliga. När de ändrade tre zinkkoordinerande rester (H30, H131 och C139) sjönk proteinets Tm med upp till ungefär 20 °C, och aktiviteten försvann. Två konserverade tyrosiner (Y60 och Y69) bidrog också till stabiliteten. Överraskande nog ökade borttagandet av en disulfidbindning — en typ av kovalent länk mellan cysteinerna C80 och C90 — smältpunkten, även om det förstörde aktiviteten. Det visar att mycket hög stabilitet i ett provrör inte alltid innebär att ett protein fungerar bättre under verkliga förhållanden. 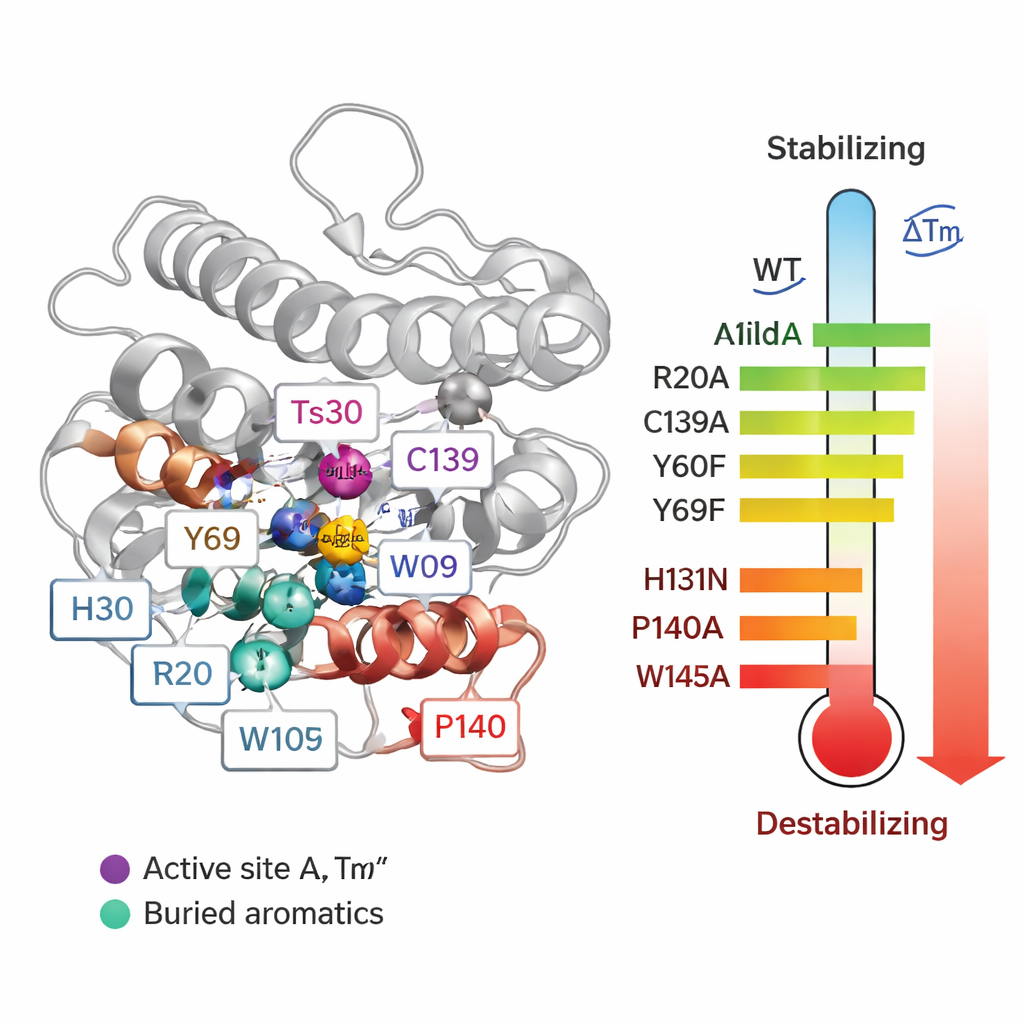
Dolda aromatiska ”ankare” och ett viktigt grepp om bakterieväggen
De mest slående resultaten kom från mutationer av prolin- och tryptofanrester. Att byta en enda prolin (P140), belägen intill zinkbindande C139, minskade Tm med över 21 °C och försvagade aktiviteten efter upphettning, eftersom mutationen störde en speciell bindningsgeometri som krävs för korrekt metallbindning. Flera djupt begravda tryptofaner (W102, W109 och särskilt W145) visade sig också vara kritiska: att ersätta dem med alanin orsakade Tm-fall på 14–24 °C och gjorde enzymet mycket mer värmekänsligt i aktivitetstester. Dessa aromatiska rester fungerar som interna ankare som låser proteinets kärna på plats. Bland argininerna hade de flesta liten effekt på stabiliteten, men R20 visade sig vara avgörande för att greppa peptidoglykanet. När R20 ersattes band enzymet dåligt till bakterieväggen och förlorade aktivitet vid upphettning, vilket visar att vissa rester bidrar mer till funktion än till ren termisk robusthet.
Från varmkällorsenzymer till tåligare antibakteriella medel
Sammantaget visar studien att Ts2631:s extraordinära värmetålighet vilar på en handfull välplacerade aminosyror snarare än en jämn förstärkning av hela proteinet. Zinkbindande rester, en konserverad prolin nära det aktiva sätet och begravda aromatiska sidokedjor bildar en stabiliserande kärna, medan några klassiska stabiliserande egenskaper, som disulfidbindningar eller saltbryggor, spelar mindre roll här än väntat. För det bredare fältet antyder detta arbete att mesofila (medeltempererade) endolysiner kan göras mer hållbara genom att omsorgsfullt byta ut utvalda positioner till tryptofan eller prolin utan att offra antibakteriell aktivitet. Med andra ord, genom att lära sig hur naturen bygger enzymer som tål nästan kokande temperaturer får forskare en praktisk ritning för att konstruera mer pålitliga, långlivade proteinbaserade antibiotika.
Citering: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Nyckelord: termostabil endolisyn, bakteriofag-enzymer, proteintermostabilitet, antibiotikaresistens, proteinengineering