Clear Sky Science · sv
Studie om biomarkörer för homocysteininducerad omvandling av vaskulära glattmuskelceller till fluffceller
Varför tilltäppta artärer börjar med små cellförändringar
Ateroskleros — de långsamma tilltäppningarna och förhårdnaderna i artärerna — är en ledande orsak till hjärtattacker och stroke. Vi hör oftast om kolesterol och kost, men mindre om hur enskilda celler i kärlväggen förändras när sjukdomen utvecklas. Denna studie granskar noggrant en sådan utlösare, en blodmolekyl som kallas homocystein, och visar hur den kan driva normalt välordnade muskelceller i artärerna att lagra fett och omvandlas till så kallade skumceller, byggstenarna i farliga plack.
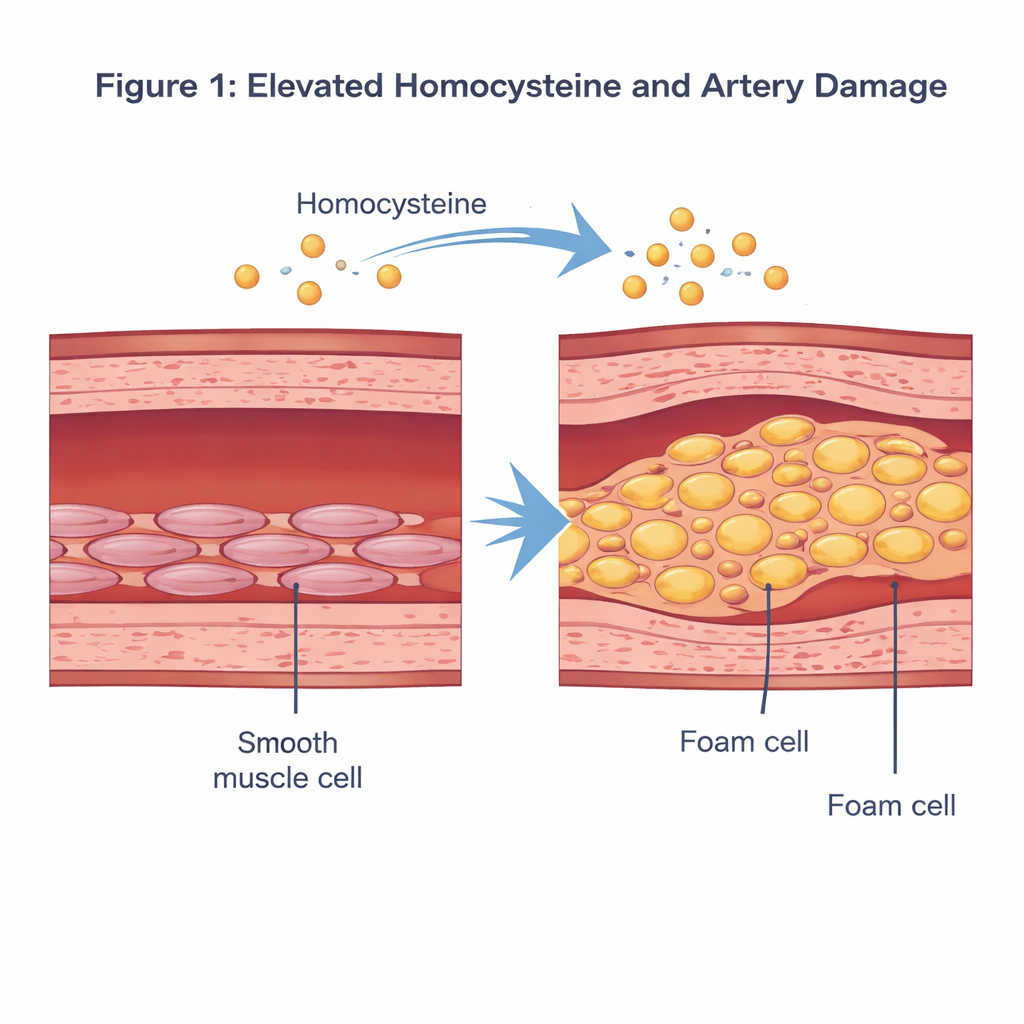
En aminosyra som ställer till det i blodomloppet
Homocystein är en svavelhaltig aminosyra som bildas när kroppen bearbetar den kostrelaterade näringsämnet metionin. Under normala förhållanden är dess nivå i blodet låg. När den stiger över cirka 15 mikromol per liter — ett tillstånd som kallas hyperhomocysteinemi — har epidemiologiska studier kopplat det till ökad risk för hjärt-kärlsjukdom. Tidigare forskning har föreslagit att överskott av homocystein kan skada det inre kärlskiktet, sätta igång inflammation och förändra beteendet hos vaskulära glattmuskelceller, som ligger i kärlets mellanskikt och hjälper till att reglera blodtrycket genom att dra ihop och slappna av.
Hur artärens muskelceller blir fettfyllda skumceller
Forskarna koncentrerade sig på hur homocystein omformar dessa glattmuskelceller. I odlingsskålar exponerade de humana vaskulära glattmuskelceller för en dos homocystein som skulle efterlikna ett sjukdomsliknande tillstånd och jämförde dem med obehandlade celler. Med standardfärgningar och biokemiska tester såg de att homocysteinbehandlade celler fylldes med rödfärgade fettdroppar och att deras kolesterol- och triglyceridnivåer ökade markant. Samtidigt sjönk proteinmarkörer för deras vanliga ”kontraktiva” identitet, medan markörer för ett mer syntetiskt, plackbildande tillstånd ökade. Sammanlagt visar dessa förändringar att homocystein kan driva glattmuskelceller bort från deras normala roll och mot ett skumcells‑liknande, fettfyllt fenotyp som bidrar direkt till plackbildning.
Jakten på molekylära fingeravtryck inne i cellerna
För att förstå vilka proteiner som förändras under denna omvandling vände teamet sig till modern proteomik, en teknik som kan mäta tusentals proteiner samtidigt. De jämförde proteinnivåer i homocysteinbehandlade celler med kontroller och kvantifierade tillförlitligt nästan 4 800 proteiner. Bland dessa stack 54 ut som signifikant förändrade: 13 ökade och 41 minskade. Många av de förändrade proteinerna är involverade i lipidhantering, cellsurvival, oxidativ stress och strukturell ombyggnad av celler. Författarna använde sedan bioinformatiska verktyg för att gruppera dessa proteiner i funktionella vägar och kartlägga hur de interagerar med varandra, med särskild betoning på nätverk kopplade till kolesterolmetabolism och stressrespons i kärlväggen.
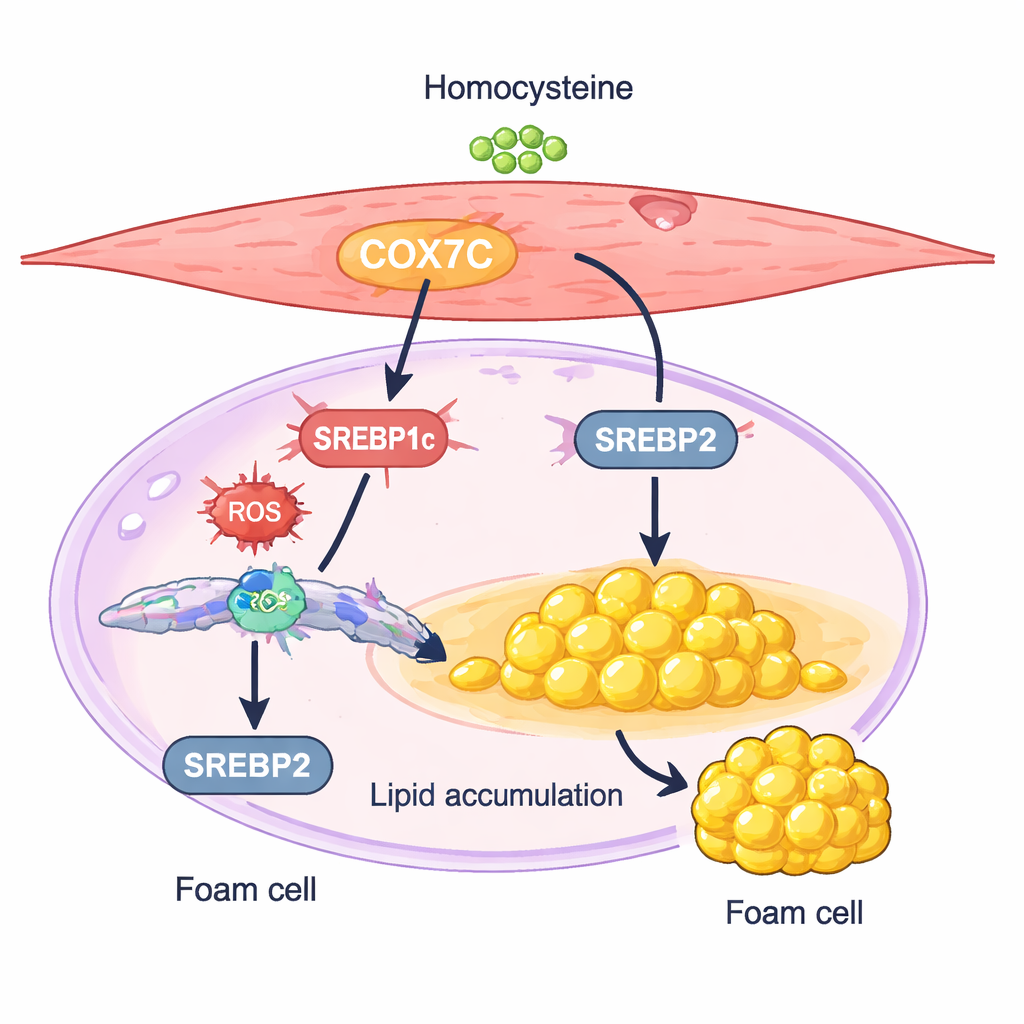
En mitokondriell växel som får celler att lagra fett
Ett protein, kallat COX7C, framträdde som en särskilt intressant misstänkt. COX7C är en komponent i cellens kraftverk, mitokondrierna, där det hjälper till att hantera energi‑produktionen. I de homocysteinbehandlade glattmuskelcellerna var COX7C‑nivåerna högre än i kontrollerna. Forskarna visade att en ökad uttrycksnivå av COX7C gjorde att cellerna ackumulerade ännu mer fett och uttryckte högre nivåer av två huvudregulatorer för lipidsyntes, SREBP1c och SREBP2. Tystande av COX7C gav motsatt effekt: det dämpade SREBP‑aktiviteten, minskade kolesterol- och triglyceriduppbyggnaden och mildrade skumcells‑liknande förändringar. Dessa resultat stöder en modell där homocystein höjer COX7C i mitokondrierna, ökar cellulära stressignaler och därigenom aktiverar SREBP‑driven fettsyntes, vilket skjuter glattmuskelceller mot ett lipidhållande tillstånd.
Vad detta betyder för hjärthälsa och framtida terapier
Denne studie bevisar ännu inte vad som händer i mänskliga artärer, och den utfördes i odlade celler snarare än i patienter. Men den ger ändå en detaljerad bild av hur förhöjt homocystein kan bistå i omvandlingen av hjälpande artärmuskelceller till skadliga skumceller, och identifierar COX7C och relaterade proteiner som potentiella biomarkörer eller läkemedelsmål. För en lekmannaläsare är huvudbudskapet att utöver ”bra” och ”dåligt” kolesterol kan små skiftningar i blodkemi — som överskott av homocystein — omprogrammera kärlväggen inifrån. Genom att peka ut molekylära aktörer som COX7C och SREBP‑vägen lägger studien grunden för framtida strategier som syftar till att stoppa plack innan de bildas, genom att hindra artärceller från att bli små fettlager.
Citering: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Nyckelord: ateroskleros, homocystein, skumceller, vaskulära glattmuskelceller, COX7C